
【题目】在下列物质中:
①H2O②NH3③NH3H2O④乙醇⑤乙烯⑥CO2⑦CuSO45H2O⑧甲烷⑨H2O2
含非极性键的极性分子有( )
A.①②⑥B.③④⑦C.④⑨D.③④⑧⑨
【答案】C
【解析】
①H2O是共价化合物,正负电荷中心不重合,由极性键构成的极性分子;
②NH3是共价化合物,结构不对称,正负电荷中心不重合,由极性键构成的极性分子;
③NH3和H2O都是极性键构成的极性分子,则NH3H2O中正负电荷中心不重合,属于只含极性键的极性分子;
④乙醇分子中含有碳碳单键,是非极性键,结构不对称且正负电荷中心无法重叠,故乙醇是含非极性键的极性分子;
⑤乙烯中含有碳碳双键,是非极性键,碳氢键是极性键,其结构对称,正负电荷中心重合,属于含非极性键和极性键的非极性分子;
⑥CO2含有碳氧极性键,其结构对称,正负电荷中心重合,属于只含有极性键的非极性分子;
⑦CuSO45H2O的结构为 ,其中铜离子和硫酸根离子之间存在离子键,硫原子和氧原子间存在极性共价键,铜原子和氧原子间存在配位键,氧原子和氢原子间存在氢键,结构中不存在非极性键;
,其中铜离子和硫酸根离子之间存在离子键,硫原子和氧原子间存在极性共价键,铜原子和氧原子间存在配位键,氧原子和氢原子间存在氢键,结构中不存在非极性键;
⑧甲烷中碳氢键为极性键,其结构对称,正负电荷中心重合,属于只含有极性键的非极性分子;
⑨H2O2含有氧氢键和氧氧键,氧氧键是非极性键,氧氢键是极性键,H2O2不是直线形分子,是半开书页形的,两个氧原子在书脊,两个氢原子分别在两个书页上,正负电荷中心不重合,是含有极性键和非极性键的极性分子;
符合题目要求的为④⑨,答案选C。


科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. BaSO4难溶于水,其属于弱电解质
B. 强电解质的导电能力一定比弱电解质的导电能力强
C. 弱电解质一定是共价化合物
D. H2O能发生微弱电离,是一种弱电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系有下列图示四种情况,且(2)、(3)、(4)图中分别有OA﹕AB=2﹕3, OA=AB, OA﹕AB=3﹕2,则下列分析与判断不正确的是(忽略CO2的溶解)( )

A. M中只有一种溶质的有(1)和(3)
B. M中有两种溶质的有(2)和(4)
C. (2)图显示M中的溶质为NaHCO3和Na2CO3,二者的物质的量之比为2:1
D. (4)图显示M中的溶质为NaOH和Na2CO3,二者的物质的量之比为1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)硅酸盐可以改写成氧化物的形式,将下列硅酸盐改写成氧化物的形式:
①镁橄榄石(Mg2SiO4):____。
②高岭石[Al2(Si2O5)(OH)4]:____。
(2)写出下列反应的方程式:
①漂白粉露置于空气中较长时间后失效的化学方程式: _________________________。
②Cl2通入NaOH溶液中,发生反应的离子方程式:________________________。
③NO2与水反应的化学方程式为___________,该反应中氧化剂与还原剂的物质的量之比为_____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成具有良好生物降解性的有机高分子材料是有机化学研究的重要课题之一。聚醋酸乙烯酯(PVAc)水解生成的聚乙烯醇(PVA),具有良好生物降解性,常用于生产安全玻璃夹层材料PVB。有关合成路线如图(部分反应条件和产物略去)。
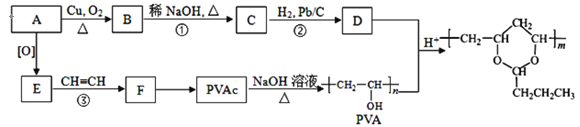
已知:Ⅰ.RCHO+R’CH2CHO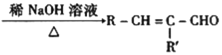 +H2O
+H2O
Ⅱ.![]() (R、R′可表示烃基或氢原子)
(R、R′可表示烃基或氢原子)
Ⅲ.A为饱和一元醇,其氧的质量分数约为34.8%,请回答:
(1)C中官能团的名称为_____,该分子中最多有_____个原子共平面。
(2)D与苯甲醛反应的化学方程式为_____。
(3)③的反应类型是____。
(4)PVAc的结构简式为____。
(5)写出与F具有相同官能团的同分异构体的结构简式____(任写一种)。
(6)参照上述信息,设计合成路线以溴乙烷为原料(其他无机试剂任选)合成 。____。
。____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
A.标准状况下,22.4L氦气含有所含的原子数约为6.02×1023
B.标准状况下,aL的二氧化碳和氮气的混合物含有的分子数约为![]() ×6.02×1023
×6.02×1023
C.22 g二氧化碳与标准状况下11.2 L 氯化氢气体含有的分子数相同
D.标准状况下,2.24L CCl4中含有的原子数约为0.5×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)天然气是一种清洁高效的能源,其主要成分为甲烷。
CH4的摩尔质量为_____________, 4.8 g CH4的物质的量为______________,在标准状况下的体积约为_______________,所含氢原子数为_______________。
(2)某化学兴趣小组对某矿泉水进行检测, 发现0.5 L该矿泉水中含有10.8 mg Mg2+,则Mg2+的物质的量浓度为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用图甲装置制取氨气并探究氨气的有关性质。

(1)装置A中烧瓶内试剂可选用__(填序号)。
a.碱石灰 b.浓硫酸 c.五氧化二磷 d.氯化钙
(2)若探究氨气的溶解性,当装置D中集满氨气后,关闭K1、K2,打开K3,引发喷泉的实验操作是__。不能在K2的导管末端连接图乙中的__装置(填序号)。
(3)若探究氨气的还原性,需关闭K1、K3,K2连接纯净、干燥氯气的装置。
①用二氧化锰与浓盐酸制取氯气,生成的气体必须依次通过盛有__试剂和__试剂的洗气瓶。
②D中氨气与氯气反应产生白烟,同时生成一种无色无味的气体,该反应的化学方程式为__。
③尾气可用C装置处理,若尾气中含有少量Cl2,则C装置中应盛放__溶液(填化学式),反应的离子方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应不仅有物质变化,同时还伴随着能量的变化,化学反应的反应热通常用实验进行测定,也可进行理论推算。
(1)在25℃、101KPa下,1gCH3OH与氧气充分反应,生成二氧化碳气体和水时释放出22.68kJ的热量,则表示甲醇燃烧热的热化学方程式为:_____。
(2)已知已知葡萄糖的燃烧热是2804kJ/mol,当它氧化生成1g液态水时放出的热量是__________ kJ(结果保留两位小数)
(3)已知热化学方程式C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) △H=-2220 kJ/mol,2H2(g)+O2(g)=2H2O(l) △H=-571.6 kJ/mol
①现有H2和C3H8的混合气体共5mol,完全燃烧时放热3472.9kJ,则混合气体中H2和C3H8的体积比为__________。
②1mol H2和2 mol C3H8组成的混合气体共完全燃烧时放热_________ kJ。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com