
【题目】将500 mL 0.1mol·L-1CuSO4和1 mol·L-1NaC1混合溶液,用石墨为电极电解。一段时间后在阳极收集到4.48 L(标况下)气体,溶液体积几乎没有变化。
计算: (已知:lg2=0.3,lg3=0.5)
(1)阴极析出铜的质量为多少克?__________
(2)计算电解后溶液的pH__________
【答案】3.2g 13.8
【解析】
溶液中所含离子为Cu2+、Na+、H+、SO42-、Cl-、OH-,电解池中阳极发生氧化反应,氯离子先于氢氧根放电,发生反应2Cl--2e-==Cl2↑,当氯离子完全反应后,氢氧根放电发生反应:4OH--4e-==O2↑+4H+;阴极发生还原反应,铜离子先于氢离子放电,发生Cu2++2e-==Cu,当铜离子完全反应后,氢离子放电发生反应:2H++2e-==H2↑;
(1)溶液中n(Cl-)=cV=0.5L×1 mol·L-1=0.5mol,完全反应可生产n(Cl2)=0.25mol,标况下的体积V(Cl2)=nVm=0.25mol×22.4L·mol-1=5.6L,所以当阳极收集到4.48 L(标况下)气体时,溶液中的氯离子未完全反应,阳极只发生2Cl--2e-==Cl2,4.48L氯气的物质的量为0.2mol,根据电极方程式可知转移电子为0.4mol;溶液中的n(Cu2+)= cV=0.5L×0.1 mol·L-1=0.05mol,根据阴极方程式Cu2++2e-==Cu可知,当铜离子完全反应时转移0.1mol电子,所以当转移0.4mol电子时铜离子已完全反应,即生成铜单质的物质的量为0.05mol,铜单质的质量=nM=0.05mol×64g·mol-1=3.2g,故答案为:3.2g;
(2)根据(1)可知当当阳极收集到4.48 L(标况下)气体时,转移0.4mol电子,且铜离子完全反应,铜离子完全反应后,阴极发生反应2H++2e-==H2,且该过程转移0.4mol-0.1mol=0.3mol电子,根据电极方程式可知消耗0.3mol氢离子,该溶液中氢离子由水电离产生,消耗0.3mol氢离子,则产生0.3mol氢氧根,所以此时溶液中c(OH-)=![]() ,则溶液中c(H+)=
,则溶液中c(H+)=![]() ,pH=-lg c(H+)= 13.8,故答案为:13.8;
,pH=-lg c(H+)= 13.8,故答案为:13.8;


科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的化工原料,有着重要的用途和应用前景。请回答下列问题:
(1)工业生产甲醇的常用方法是CO(g)+2H2(g)![]() CH3OH(g) ΔH=-90.8 kJ·mol-1。
CH3OH(g) ΔH=-90.8 kJ·mol-1。
已知:2H2(g)+O2(g)==2H2O(l) ΔH=-571.6 kJ·mol-1;
2CO(g)+O2(g)=2CO2(g) ΔH=-566.0 kJ·mol-1;
CH3OH(g)=CH3OH(l) ΔH=-37.3 kJ·mol-1。
计算液体CH3OH的燃烧热为_______________。
(2)甲醇不完全燃烧产生的CO可利用I2O5来除去,其反应为5CO(g)+I2O5(s)![]() 5CO2(g) +I2(s)。不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得的CO2体积分数随着时间t变化曲线如图所示。则:
5CO2(g) +I2(s)。不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得的CO2体积分数随着时间t变化曲线如图所示。则:

①T2温度时,0~0.5 min的反应速率v(CO)=___________。
②T1温度时,反应达到平衡,CO的转化率为_______,化学平衡常数K=_______(用具体数值表示)。
③下列说法正确的是_________(填编号)。
A.容器内压强不变,表明反应达到平衡状态
B.容器内气体密度不变,表明反应达到平衡状态
C.单位时间内,消耗a mol CO,同时消耗2a mol CO2, 表明反应v(正)<v(逆)
D.两种温度下,c点时体系中混合气体的压强相等
E.反应5CO(g)+I2O5(s)![]() 5CO2(g)+I2(s)为吸热反应
5CO2(g)+I2(s)为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域.在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C![]() 2AlN+3CO.下列叙述正确的是( )
2AlN+3CO.下列叙述正确的是( )
A.在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中每生成2 mol AlN,N2得到3 mol电子
C.氮化铝中氮元素的化合价为﹣3
D.氮化铝晶体属于分子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同温度下(T=500K),有相同体积的甲、乙两容器,且保持体积不变,甲容器中充入1gSO2和1gO2,乙容器中充入2gSO2和2gO2。下列叙述中错误的是( )
A.化学反应速率:乙>甲B.平衡时O2的浓度:乙>甲
C.平衡时SO2的转化率:乙>甲D.平衡时SO2的体积分数:乙>甲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,不能按![]() (“→”表示一步完成)的关系相互转化的是 ( )
(“→”表示一步完成)的关系相互转化的是 ( )
选项 | a | b | c |
A | Fe | FeCl3 | FeCl2 |
B | Cl2 | NaClO | NaCl |
C | Si | SiO2 | H2SiO3 |
D | HNO3 | NO | NO2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1和-1366.8kJ·mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为( )
A. -44.2kJ·mol-1 B. +44.2kJ·mlo-1
C. -330kJ·mol-1 D. +330kJ·mlo-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: 2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+ ![]() O2(g)△H=-226kJ/mol
O2(g)△H=-226kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
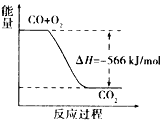
A. CO 的燃烧热为566kJ/mol
B. 上图可表示由CO生成CO2的反应过程和能量关系
C. 2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) △H<-452 kJ/mol
D. CO2(g)与Na2O2(s)反应放出452kJ 热量时,电子转移数为1.204×1024 (个)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铍铜是力学、化学综合性能良好的合金,广泛应用于制造高级弹性元件。以下是从某废旧铍铜元件(含BeO25%、CuS71%、少量FeS和SiO2)中回收铍和铜两种金属的流程。

已知:I.铍、铝元素处于周期表中的对角线位置,化学性质相似
Ⅱ.常温下:Ksp[Cu(OH)2]=2.2×10-20 Ksp[Fe(OH)3]=4.0×10-38 K sp[Mn(OH)2]=2.1×10-13
(1)滤液A的主要成分除NaOH外,还有__(填化学式)。写出反应I中含铍化合物与过量盐酸反应的离子方程式__。
(2)①溶液C中含NaCl、BeCl2和少量HCl,为提纯BeCl2,选择合理步骤并排序__。
a加入过量的 NaOH b.通入过量的CO2 c加入过量的氨水 d.加入适量的HCl e.过滤 f洗涤
②从BeCl2溶液中得到BeCl2固体的操作是__。
(3)MnO2能将金属硫化物中的硫元素氧化为单质硫,若用浓HNO3代替MnO2溶解金属硫化物,缺点是__(任写一条)。
(4)溶液D中含c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.008mol·L-1、c(Mn2+)=0.01mol·L-1,逐滴加入稀氨水调节pH可依次分离,首先沉淀的是__(填离子符号),为使铜离子开始沉淀,常温下应调节溶液的pH值大于__。
(5)取铍铜元件1000g,最终获得Be的质量为81g,则产率是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是利用盐桥电池从某些含碘物质中提取碘的两个装置,下列说法中正确的是( )
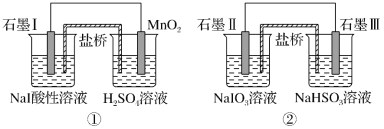
A.两个装置中,石墨I和石墨Ⅱ均作负极
B.碘元素在装置①中被还原,在装置②中被氧化
C.装置①中MnO2的电极反应式为MnO2+2H2O+2e-=Mn2++4OH-
D.装置①、②中的反应生成等量的I2时,导线上通过的电子数之比为1∶5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com