
【题目】氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域.在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C![]() 2AlN+3CO.下列叙述正确的是( )
2AlN+3CO.下列叙述正确的是( )
A.在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中每生成2 mol AlN,N2得到3 mol电子
C.氮化铝中氮元素的化合价为﹣3
D.氮化铝晶体属于分子晶体
【答案】C
【解析】
试题分析:在一定条件下,合成氮化铝的反应为Al2O3+N2+3C![]() 2AlN+3CO.反应中氮、碳元素化合价变化,Al、O元素的化合价不变,AlN中N的化合价为﹣3价.
2AlN+3CO.反应中氮、碳元素化合价变化,Al、O元素的化合价不变,AlN中N的化合价为﹣3价.
解:A.根据氧化还原反应的规律:(还原剂)升(化合价升高) 失(失去电子) 氧(发生氧化反应);(氧化剂)降(化合价降低) 得(得到电子) 还(发生还原反应)若说剂正相反.可以分析出,在氮化铝的合成反应中,N2的化合价由0→﹣3,发生改变,N2是氧化剂;Al2O3 中Al、O元素的化合价不变,既不是氧化剂也不是还原剂.故A错误;
B.在氮化铝的合成反应中,N2的化合价由0→﹣3,每生成2 mol AlN,N2得到的电子是3×2=6mol电子.故B错误;
C.氮化铝中Al的化合价为+3价,氮元素的化合价为﹣3价.故C正确;
D.氮化铝晶体是由Al3+和N3﹣构成的离子化合物.故D错误;
故选C.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在恒容绝热的容器中进行反应:2A(g)+B(g)![]() 3C(g)+D(s)△H=-akJ·mol-1(a>0),下列说法不正确的是
3C(g)+D(s)△H=-akJ·mol-1(a>0),下列说法不正确的是
A.容器中压强不变,表明反应达到平衡状态
B.反应过程中A、B的转化率始终相同
C.增加A的浓度,平衡时B的体积分数减少
D.容器中气体的密度不变,表明反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式和离子方程式书写不正确的是( )
A. 甲苯和液溴可以发生如下的反应:![]() +Br2
+Br2![]()
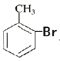 +HBr
+HBr
B. 甲酸溶液与足量的银氨溶液共热的化学方程式:HCOOH +2Ag(NH3)2OH![]() (NH4)2CO3+H2O+ 2Ag↓ +3NH3
(NH4)2CO3+H2O+ 2Ag↓ +3NH3
C. 苯酚钠溶液中通入少量二氧化碳反应的离子方程式:![]()
D. 尼泊金酸(![]() )与碳酸氢钠溶液反应的离子方程式
)与碳酸氢钠溶液反应的离子方程式![]() +HCO3-→
+HCO3-→![]() +H2O+CO2↑
+H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某样品甲为仅含有三种元素的纯净物,不溶于水,能溶于稀盐酸,为探究其组成和性质,设计并完成如下实验:
①将 21.5g 该物质溶解于 600mL 1mol·L-1 盐酸中,得到黄色溶液乙,将溶液乙分成两等份;
②将其中一份加热蒸干、灼烧,得到 8.0g 红棕色固体丙;
③向另一份溶液中加入足量硝酸酸化的硝酸银溶液,过滤、洗涤、干燥得到白色沉淀 57.4g。请回答:
(1)写出实验③中检出离子的结构示意图_____。
(2)样品甲中所含的三种元素为_____。
(3)写出实验①中反应的离子方程式_____。
(4)写出实验②中,检出固体丙中所含阳离子的实验方法_____。(写出实验操作、现象及结论)。
查看答案和解析>>
科目:高中化学 来源: 题型:
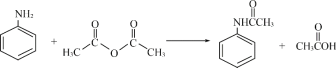
【题目】酰苯胺作为一种常用药,具有解热镇痛的效果。实验室制备乙酰苯胺时,可以用苯胺与乙酸酐或与冰醋酸加热来制取,苯胺与乙酸酐的反应速率远大于与冰醋酸反应的速率,现选用苯胺与乙酸酐为原料制取和提纯乙酰苯胺,该放热反应的原理:
密度(g/mL) | 相对分子质量 | 颜色、状态 | 溶解性 | |
苯胺 | 1.04 | 93 | 无色油状液体 | 微溶于水, 易溶于乙醇、乙醚 |
乙酸酐 | 1.08 | 102 | 无色透明液体 | 遇水缓慢反应生成乙酸 |
乙酰苯胺 | 135 | 无色片状晶体, 熔点 114℃ | 不溶于冷水,可溶于热 水、乙醇、乙醚 |
实验步骤
①取 5.00mL 苯胺,倒入 100mL 锥形瓶中,加入 20mL 水,在旋摇下分批加入 6.00mL 乙酸酐,搅拌均匀。若有结块现象产生,用玻璃棒将块状物研碎,再充分搅拌;
②反应完全后,及时把反应混合物转移到烧杯中,冷却后,抽滤,洗涤,得粗乙酰苯胺固体;
③将粗产品转移至 150mL 烧杯中,加入适量水配制成 80℃的饱和溶液,再加入过量 20%的水。稍冷后,加半匙活性炭,搅拌下将溶液煮沸 3~5min,趁热过滤,冷却结晶,抽滤、洗涤、晾干得乙酰苯胺纯品。
请回答:
(1)苯胺与冰醋酸反应制备乙酰苯胺的化学反应方程式____________________________________。
(2)反应温度过高会导致苯胺挥发,下列操作可控制反应温度,防止反应温度升高过快的是____________。
A.反应快结束时的充分搅拌 B.旋摇下分批加入 6.0mL 乙酸酐
C.玻璃棒将块状物研碎 D.加 20mL 水
(3)在步骤②中对粗产品进行洗涤可能需要用到以下操作:a.加入洗涤剂至浸没固体;b. 洗涤剂缓慢通过;c.洗涤剂快速通过;d.关小水龙头;e.开大水龙头;f.重复 2~3 次。请选出正确的操作并排序_____。(操作可重复使用)
(4)加入过量 20%的水的目的是_____。
(5)下列关于步骤③说法不正确的是__________________________。
A. 活性炭吸附有色物质,可以提高产率
B. 冷却时,冰水浴冷却比室温冷却更易得到大颗粒晶体便于抽滤
C. 抽滤用如图装置,为防止倒吸,结束时可先关闭抽气泵,后打开活塞 a
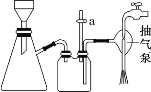
D. 洗涤完成后应将布氏漏斗从吸滤瓶上取下,左手握布氏漏斗,倒转,用右手“拍击”左手, 使固体连同滤纸一起落入洁净的表面皿上,揭去滤纸,再对固体做晾干处理
(6)最后测得纯乙酰苯胺固体 5.40g,该实验的产率为_____(保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】迷迭香酸具有抗氧化、延缓衰老、减肥降脂等功效,它的结构简式为:
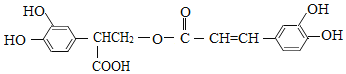
以邻苯二酚为原料合成迷迭香酸的路线为:
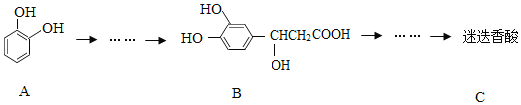
下列说法错误的是( )
A. 有机物B可以发生取代、加成、消去、氧化反应
B. 1 mol B与足量的NaOH溶液反应,最多可消耗4 mol NaOH
C. 迷迭香酸在稀硫酸催化下水解的一种产物可由B转化得到
D. 有机物A分子中所有原子可能在同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
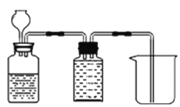
【题目】“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置来制取乙酸乙酯。试回答下列问题:
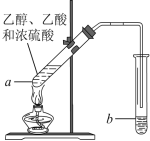
(1)写出a试管中的化学反应方程式_______________。
(2) b中为饱和碳酸钠溶液,其主要作用是_________。
(3)b中导管要插在液面上,不能插入溶液中的目的是_____________。
(4)试管b中观察到的现象____________________ 。
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是_________(填操作名称);主要使用的玻璃仪器是_______。(仪器的名称)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:
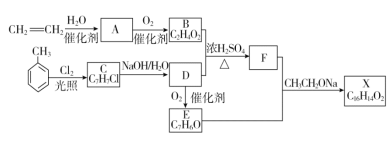
已知:RCHO+CH3COOR′![]() RCH=CHCOOR′。
RCH=CHCOOR′。
请回答:
(1)B中官能团的名称是_______
(2)C生成D的化学方程式:________ ,反应类型为________
(3)E和F生成X的化学方程式________
(4)对于化合物X,下列说法正确的是________
A.能发生水解反应 B.不与浓硝酸发生取代反应
C.能使Br2/CCl4溶液褪色 D.能发生银镜反应
(5)下列化合物中属于F的同分异构体的是________。
A. ![]()
B. ![]()
C.CH2=CHCH=CHCH=CHCH=CHCOOH
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图回答有关问题。
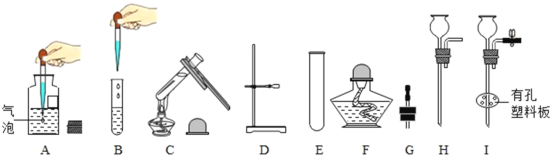
(1)仪器E的名称为___________。
(2)图A~C是常见实验基本操作。其中正确的是___________(填序号);请选择一个有错误的操作写出改正方法:_________________________________________________________________________。
(3)选择仪器D~I完成下列实验操作:
①用KMnO4制备O2,应选仪器________(填序号),其化学反应方程式为_________________________________;
②用大理石与稀盐酸反应制备CO2并使反应随时发生或停止,应选仪器___________,其反应方程式为______________________。
(4)如图是以锌粒和稀硫酸反应制备H2,并用排水法收集。请把图补画完整____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com