
【题目】下列各组物质中,不能按![]() (“→”表示一步完成)的关系相互转化的是 ( )
(“→”表示一步完成)的关系相互转化的是 ( )
选项 | a | b | c |
A | Fe | FeCl3 | FeCl2 |
B | Cl2 | NaClO | NaCl |
C | Si | SiO2 | H2SiO3 |
D | HNO3 | NO | NO2 |
A.AB.BC.CD.D
【答案】C
【解析】
A.2Fe+3Cl2 ![]() 2FeCl3,2FeCl3+Fe=3FeCl2,FeCl2+Mg=MgCl2+Fe,即能够实现题目中的转化,故A正确;
2FeCl3,2FeCl3+Fe=3FeCl2,FeCl2+Mg=MgCl2+Fe,即能够实现题目中的转化,故A正确;
B.Cl2+2NaOH=NaCl+NaClO+H2O,NaClO+HCl=NaCl+HClO,2NaCl+2H2O ![]() 2NaOH+H2↑+Cl2↑,能够实现题目中的转化,故B正确;
2NaOH+H2↑+Cl2↑,能够实现题目中的转化,故B正确;
C.Si+O2![]() SiO2,而SiO2不能直接与H2O反应生成H2SiO3,不能够实现题目中的转化,故C错误;
SiO2,而SiO2不能直接与H2O反应生成H2SiO3,不能够实现题目中的转化,故C错误;
D.3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,2NO+O2=2NO2,二氧化氮与水反应生成一氧化氮和硝酸,反应的化学方程式为3NO2+H2O═2HNO3+NO,即能够实现题目中的转化,故D正确;
故答案为C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在初始温度为500℃、容积恒定为10L的三个密闭容器中,如图充料发生反应:CO2 (g) +3H2 (g) ![]() CH30H(g)十H2 O (g)△H= -25kJ/mol。已知乙达到平衡时气体的压强为开始时的0.55倍;乙、丙中初始反应方向不同,平衡后对应各组分的体积分数相等。下列分析正确的是
CH30H(g)十H2 O (g)△H= -25kJ/mol。已知乙达到平衡时气体的压强为开始时的0.55倍;乙、丙中初始反应方向不同,平衡后对应各组分的体积分数相等。下列分析正确的是

A. 刚开始反应时速率:甲>乙
B. 平衡后反应放热;甲>乙
C. 500℃下该反应平衡常数:K =3×102
D. 若a≠0,则0.9<b<l
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种常见的短周期元素,可形成XY2、Z2Y、XY3、Z2Y2、Z2X等化合物,已知Y的离子和Z的离子具有相同的电子层结构,X离子比Y离子多一个电子层,试回答:
(1)X、Y、Z的单质的晶体分别属于_______晶体,________晶体,_____晶体
(2)Z2Y2的电子式为___________,Z2Y2溶于水的化学方程式为__________。
(3)XY3在标准状态下是针状晶体,它属于___________晶体,XY3的水溶液与Z2Y2反应可生成一种具有漂白性的氧化剂H2Y2,其化学方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D是中学化学中常见的四种不同粒子,它们之间存在如下图所示的转化关系:
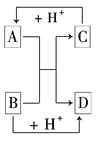
(1)如果A、B、C、D均是10电子的粒子,请写出:
A的结构式_____________;D的电子式____________;
(2)如果A和C是18电子的粒子,B和D是10电子的粒子,请写出:
①A与B在溶液中反应的离子方程式:____________________________________
②根据上述离子方程式,可判断C与B结合质子的能力大小是(用化学式或离子符号表示)________>________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是用0.1 mol·L-1 NaOH溶液分别滴定20 mL浓度均为0.1 mol·L-1的不同一元酸的滴定曲线(图中曲线由上向下依次是氢氰酸、醋酸、氢氟酸、盐酸),下列说法错误的是
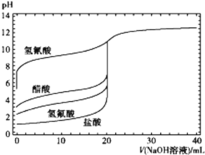
A.酸性:HF>CH3COOH>HCN
B.当加入10 mL NaOH溶液时,c(CN-)>c(CH3COO-)
C.用NaOH溶液滴定醋酸时,应用酚酞作指示剂不能使用甲基橙
D.随NaOH溶液滴入,CH3COOH溶液中水的电离程度先变大后变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将500 mL 0.1mol·L-1CuSO4和1 mol·L-1NaC1混合溶液,用石墨为电极电解。一段时间后在阳极收集到4.48 L(标况下)气体,溶液体积几乎没有变化。
计算: (已知:lg2=0.3,lg3=0.5)
(1)阴极析出铜的质量为多少克?__________
(2)计算电解后溶液的pH__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.苯酚沾在手上,应立即用NaOH溶液清洗
B.给试管中液体加热时,液体不超过试管容积的![]()
C.用升华法分离碘和氯化铵的混合物
D.试管壁上的银镜可用稀硫酸洗涤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】六种短周期元素,aA、bB、cC、dD、eE、fF,已知原子序数大小关系是:a<e<c<b<f<d,且a+b=(c+d)/2;六种元素在周期表中的位置关系是:A、B同主族,C、D也同主族;C、E相邻,B、F也相邻。
(1)B、C、D三种元素形成的六原子核的化合物和水反应的离子方程式是:_______________。
(2)A、C形成的四原子核化合物甲的电子式为_______,该化合物呈弱酸性,试写出这种化合物的电离方程式:_______________。
(3)写出分别由A、B、C、D四种元素所形成的两种化合物的水溶液相互反应的离子方程式:__________________________________________________。
(4)写出A、C、D形成的六原子核化合物乙的水溶液和甲的水溶液反应的化学方程式:_______________________________________________________。
(5)写出E和F形成的化合物和化合物A2C反应的化学方程式:____________。
(6)A、E形成的四原子核化合物丙容易液化,其原因是:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中加入金属铝有氢气放出,则在此溶液中可能大量共存的离子是( )
A.K+、Mg2+、NO3-、SO42-B.K+、Na+、Cl-、HCO3-
C.K+、Na+、AlO2-、SO42-D.K+、NH4+、Cl-、CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com