
【题目】如图是用0.1 mol·L-1 NaOH溶液分别滴定20 mL浓度均为0.1 mol·L-1的不同一元酸的滴定曲线(图中曲线由上向下依次是氢氰酸、醋酸、氢氟酸、盐酸),下列说法错误的是
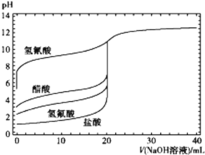
A.酸性:HF>CH3COOH>HCN
B.当加入10 mL NaOH溶液时,c(CN-)>c(CH3COO-)
C.用NaOH溶液滴定醋酸时,应用酚酞作指示剂不能使用甲基橙
D.随NaOH溶液滴入,CH3COOH溶液中水的电离程度先变大后变小
【答案】B
【解析】
A. 相同条件下,相同浓度的三种酸,溶液的pH:HF<CH3COOH<HCN,pH越小,酸性越强,所以酸性:HF>CH3COOH>HCN,故A正确;
B. HCN的酸性小于CH3COOH,相同浓度时,HCN的电离程度小,溶液中CN-的浓度小,所以溶液中c(CN-)<c(CH3COO-),故B错误;
C. NaOH与醋酸反应生成CH3COONa,溶液显碱性,应该选择在碱性条件下变色的指示剂,所以选择酚酞,故C正确;
D. 随NaOH溶液的滴入,CH3COOH溶液中氢离子浓度减小,对水的抑制程度减小,当氢氧化钠过量,NaOH会抑制水的电离,水的电离程度减小,所以CH3COOH溶液中水的电离程度先变大后变小,故D正确。
故答案为B。


科目:高中化学 来源: 题型:
【题目】药物中间体M的合成路线流程图如图:

已知:

 (R、R’、R”为H或烃基)
(R、R’、R”为H或烃基)
请回答下列问题:
(1)A为芳香烃,名称为___。
(2)化合物C含有的官能团名称为__。
(3)下列说法中正确的是__。
A.化合物A只有1种结构可以证明苯环不是单双键交替的结构
B.可利用酸性KMnO4溶液实现A→B的转化
C.化合物C具有弱碱性
D.步骤④、⑤、⑥所属的有机反应类型各不相同
(4)步骤⑥可得到一种与G分子式相同的有机副产物,其结构简式是__。
(5)有机物H与氢气加成的产物J存在多种同分异构体。写出一种同时符合下列条件的同分异构体的结构简式__。
①能与FeCl3溶液发生显色反应;
②核磁共振氢谱检测表明分子中有4种化学环境不同的氢原子。
(6)写出I+G→M的化学方程式(可用字母G和M分别代替物质G和M的结构简式)__。
(7)设计以![]() 和CH3CH2OH为原料制备
和CH3CH2OH为原料制备![]() 的合成路线流程图_____(无机试剂任选)。
的合成路线流程图_____(无机试剂任选)。
合成路线流程图示例如下:CH2=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与金属腐蚀有关的说法,正确的是


A.图1中,插入海水中的铁棒,越靠近底端腐蚀越严重
B.图2中,插入溶液中的铁棒容易溶解,主要是发生电化学腐蚀
C.图3中,燃气灶的中心部位容易生锈,主要是由于高温下铁发生电化学腐蚀
D.图4中,用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在有机物的分子中,当碳原子连有4个不同的原子或原子团时,这种碳原子称为“手性碳原子”,在其旁边标有*号。凡具有一个手性碳原子的化合物一定具有光学活性。如图有机物含有一个手性碳原子,具有光学活性,当发生下列化学反应,生成的新有机物无光学活性的是( )
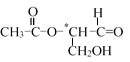
A.与氢氧化钠水溶液共热反应B.与新制银氨溶液共热反应
C.与甲酸在一定条件下发生酯化反应D.与H2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对已达化学平衡的反应 2X(g)+Y(g)![]() 2Z(g) ΔH<0 下列说法正确的是
2Z(g) ΔH<0 下列说法正确的是
A.减小压强,逆反应速率增大,正反应速率减小,平衡向逆方向移动
B.升高温度,正、逆反应速率均增大,平衡向逆方向移动
C.除去部分的Z,正反应速率增大,逆反应速率减小,平衡向正方向移动
D.加入正催化剂,正、逆反应速率均增大,平衡向正方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,不能按![]() (“→”表示一步完成)的关系相互转化的是 ( )
(“→”表示一步完成)的关系相互转化的是 ( )
选项 | a | b | c |
A | Fe | FeCl3 | FeCl2 |
B | Cl2 | NaClO | NaCl |
C | Si | SiO2 | H2SiO3 |
D | HNO3 | NO | NO2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天津是我国研发和生产锂离子电池的重要基地。锂离子电池正极材料是含锂的二氧化钴(LiCoO2),充电时LiCoO2![]() 中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示。电池反应LiCoO2+C6
中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示。电池反应LiCoO2+C6![]() CoO2+LiC6,下列说法正确的是 ( )
CoO2+LiC6,下列说法正确的是 ( )
A.充电时,电池的负极反应为LiC6-e-=Li+C6
B.放电时,电池的正极反应为CoO2+Li2++e-=LiCoO2
C.羧酸、醇等含活泼氢的有机物可用作锂离子电池的电解质
D.锂离子电池的比能量(单位质量释放的能量)低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,H2(g)+CO2(g)![]() H2O(g)+CO2(g)的平衡常数
H2O(g)+CO2(g)的平衡常数![]() 。该温度下在甲、乙、丙三个恒容密闭容器中,
。该温度下在甲、乙、丙三个恒容密闭容器中,
起始浓度 | 甲 | 乙 | 丙 |
c(H2)/mol | 0.010 | 0.020 | 0.020 |
c(CO2)/mol | 0.010 | 0.010 | 0.020 |
投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的是( )
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液中可以发生反应:X+2Y3+=2Y2++X2+,则下列叙述①X被氧化;②X是氧化剂;③X具有还原性;④Y2+是氧化产物;⑤Y2+具有还原性;⑥Y3+的氧化性比X2+的氧化性强。以下叙述中正确的是( )
A.②④⑥B.①③④C.①③⑤⑥D.②⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com