
【题目】(1)中国的高铁技术居于国际领先地位。
①高铁座椅内填充有聚氨酯软质泡沫。聚氨酯属于____(填字母)。
a.金属材料 b.无机非金属材料 c.有机高分子材料
②高铁信息传输系统中使用了光导纤维。光导纤维的主要成分是____(填字母)。
a.铜 b.石墨 c.二氧化硅
③高铁轨道建设需用大量水泥。生产水泥的主要原料为黏土和____(填字母)。
a.石灰石 b.粗盐 c.纯碱
(2)营养均衡有利于身体健康。
①人体内提供能量的主要营养物质为____、糖类和蛋白质。淀粉在人体内水解的最终产物是____。
②维生素是人体需要的营养物质。如图为某品牌维生素C泡腾片说明书的部分内容。该泡腾片中添加的着色剂是____,甜味剂是___。泡腾片溶于水时产生“沸腾”效果,是由于添加的酒石酸和___反应释放出了气体。

(3)煤炭在我国能源结构中占有重要地位,合理使用有利于社会可持续发展。
①控制燃煤产生的SO2排放,能够减少____型酸雨的形成。燃煤排放的烟气中还含有其他污染物,请列举一种:_____。
②燃煤产生的CO2用NH3处理可生产多种化工产品。用氨水吸收CO2可制得碳铵(NH4HCO3),写出该反应的化学方程式_____。用液氨与CO2反应可制备尿素[CO(NH2)2]。尿素和碳铵这两种氮肥中,氮元素的质量分数较高的是_____。
③煤的气化和液化是实现能源清洁化的重要途径。水煤气中CO和H2在加热、加压和催化剂存在条件下可以合成液体燃料(CH3OH),该反应的化学方程式为_____。
【答案】c c a 油脂 葡萄糖 喹啉黄 糖精钠、蔗糖 碳酸氢钠 硫酸 可吸入颗粒物等 NH3·H2O + CO2=NH4HCO3 尿素 CO +2H2 ![]() CH3OH
CH3OH
【解析】
(1)①聚氨酯泡沫,根据名称为聚合物,属于有机高分子材料;答案为c;
②光导纤维的主要成分为二氧化硅;答案为c;
③生成水泥的主要成分为石灰石、黏土;答案为a;
(2)①人体内提供能量的主要营养物质有油脂、糖类、蛋白质;淀粉属于糖类,在人体内最终水解为葡萄糖;答案为油脂 葡萄糖;
②辅料中有柠檬香精,橙味香精、喹啉黄、糖精钠、蔗糖、氯化钠、碳酸氢钠、酒石酸等。从其名称来可以判断其作用,着色剂为喹啉黄,甜味剂有蔗糖、糖精钠;溶于水产生沸腾的效果由于酒石酸和碳酸氢钠反应生成CO2;答案为喹啉黄 糖精钠、蔗糖 碳酸氢钠;
(3)①SO2溶于水后生成亚硫酸,被氧气氧化成硫酸,减少SO2的排放,可以减少硫酸型的酸雨;燃煤排放的烟气中除SO2还有煤炭未完全燃烧生成的CO,高温下氮气和氧气生成的NO,氮氧化物等,还有些烟尘,答案为可吸入颗粒物等;
②氨水吸收CO2制取碳酸铵,为酸性氧化物与碱的反应,答案为NH3·H2O + CO2=NH4HCO3。NH4HCO3中N的质量分数![]() ;CO(NH2)2中N的质量分数
;CO(NH2)2中N的质量分数![]() ,N含量较高的是尿素;
,N含量较高的是尿素;
③水煤气中CO和H2在加热、加压和催化剂存在条件下可以合成液体燃料(CH3OH),根据原子守恒,得到化学方程式为CO +2H2 ![]() CH3OH。
CH3OH。


科目:高中化学 来源: 题型:
【题目】有 X、Y、Z 三种元素,X 是有机化合物中必含的元素, Y 是地壳里含量最多的元素,Z 是质量最轻的元素。X、Y、Z 三种元素组成的有机物 M 能被酸性高锰酸钾氧化生成 N。为了测定有机物 M 的结构,做如下实验:
①将 4.6 g 有机物 M 完全燃烧,测得生成 0.2mol CO2 和 5.4 g 水;
②用质谱仪检测有机物 M,得到如图一所示的质谱图;
③用核磁共振仪处理有机物 M,得到如图二所示图谱,图中三个峰面积之比为1:2:3
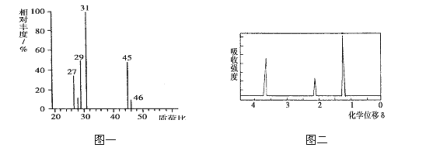
试回答下列问题:
⑴M 的结构简式是______________。
⑵N 中含有的官能团的结构简式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一无色透明的溶液做如下实验:
①取少量溶液滴加盐酸酸化的BaCl2溶液有白色沉淀生成。
②另取部分溶液加入Na2O2,有无色无味气体放出且有白色沉淀生成,加入Na2O2的量与生成沉淀的量的关系如图所示,试问:
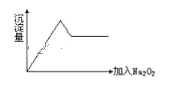
(1)Cu2+、NH4+、Al3+、Mg2+、Na+、Fe3+、K+、SO42-等离子中一定存在的离子是__;可能存在的离子是__;一定不存在的离子是___。
(2)上述溶液至少由___等物质混合成。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用63%的浓HNO3(其密度为1.4g/mL)配制240mL0.50mol/L稀HNO3,若实验仪器有:A.10mL量筒 B.50mL量筒 C.托盘天平 D.玻璃棒 E.100mL容量瓶 F.250mL容量瓶 G.500mL容量瓶 H.胶头滴管 I.200mL烧杯。
(1)此浓硝酸的物质的量浓度为___mol/L。
(2)应量取63%的浓硝酸___mL,应选用的量筒是___(填仪器的字母编号)。
(3)实验时还需选用的仪器有(填序号)D、I、___(填序号)
(4)配制过程中,下列操作会使配制的稀硝酸溶液浓度偏高的是___(填序号)。
①量取浓硝酸的量筒用蒸馏水洗涤2﹣3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③定容时俯视刻度线
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计的微型实验装置验证SO2的性质,通过分析实验,下列结论表达正确的是( )

A.a棉球褪色,验证SO2具有氧化性
B.c棉球蓝色褪去,验证SO2漂白性
C.b棉球褪色,验证SO2具有酸性氧化物的通性
D.可以使用浓硫酸吸收尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组用下图装置研究原电池的工作原理。
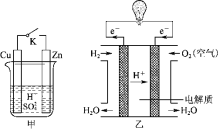
(1)甲中K断开时,装置中发生反应的离子方程式为_______________________;K闭合时,Cu棒上的现象为________,它为原电池的________(填“正”或“负”)极。
(2)乙图为氢氧燃料电池构造示意图,其中通入氢气的一极为电池的________(填“正”或“负”)极,发生________(填“氧化”或“还原”)反应。
(3)某同学欲把反应Fe+2FeCl3=3FeCl2设计成原电池,请写出负极的电极反应式:_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组探究氨基甲酸铵(NH2COONH4)分解的化学平衡和水解反应速率。
(1)将一定量纯净的氨基甲酸铵置于固定容积为 100mL 的密闭真空溶液 A 中,在恒定温度下使其达到分解 平衡。实验测得不同温度下的平衡数据列于下表:
温度(℃) | 20.0 | 25.0 | 30.0 | 35.0 |
平衡气体总物质的量(mol) | 0.34 | 0.48 | 0.68 | 0.94 |
①氨基甲酸铵分解的化学方程式为 NH2COONH4(s) 2NH3(g)+CO2(g),若 25.0℃时达到平衡所用时间为8min,根据数据计算 NH3 的平均生成速率为__________。
②可以判断该分解反应已经达到化学平衡的是_____。
A. 2v(NH3)正=v(CO2)逆
B.密闭容器中总压强不变
C. 密闭容器中混合气体的密度不变
D. 密闭容器中氨气的体积分数不变
(2)已知:NH2COONH4+2H2O NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始浓度的氨基甲酸铵 溶液测定水解反应速率,得到 c(NH2COO-)随时间变化趋势如图所示。根据图中信息,如何说明水解反应速率随温度升高而增大:_____。

(3)合成氨工业对国民经济和社会发展具有重要意义。工业合成氨常用的催化剂是_____,氨分子的电子式是_____。
(4)如图是一定的温度和压强下时 N2 和 H2 反应生成 1molNH3 过程中能量变化示意图,请写出工业合成氨的热化学反应方程式:__________________________。(热量 Q 的数值使用含字母 a、b 的代数式表示)

(5)在催化剂存在下,NH3 可用来消除 NO 的污染,生成两种对环境无害的物质。写出反应的化学方程式:_____________________;该反应中氧化产物与还原产物的物质的量之比是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu2O广泛应用于太阳能电池领域。以CuSO4、NaOH和抗坏血酸为原料,可制备CuO。
(1)Cu2+基态核外电子排布式为________。
(2)SO42-的空间构型为_______(用文字描述)。
(3)抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为______;推测抗坏血酸在水中的溶解性:_______(填“难溶于水”或“易溶于水”)。
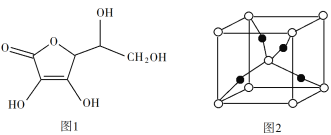
(4)一个Cu2O晶胞(见图2)中,Cu原子的数目为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20.00mL0.1000mol·L-1CH3COOH溶液中慢慢加入NaOH固体。CH3COOH与CH3COO-的浓度变化趋势如图所示(不考虑溶液体积和温度的变化)。n(NaOH)=0.001mol时,溶液呈酸性。下列说法正确的是
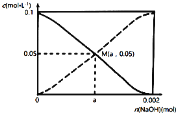
A.当n(NaOH)=0.002mol时,c(CH3COO-)>c(Na+)>c(CH3COOH)
B.在M点时,n(OH-)-n(H+)=a-0.05
C.a<0.001mol
D.当n(NaOH)=0.001mol时,c(H+)+c(CH3COOH)=2c(OH-)+c(CH3COO-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com