
【题目】某同学设计的微型实验装置验证SO2的性质,通过分析实验,下列结论表达正确的是( )

A.a棉球褪色,验证SO2具有氧化性
B.c棉球蓝色褪去,验证SO2漂白性
C.b棉球褪色,验证SO2具有酸性氧化物的通性
D.可以使用浓硫酸吸收尾气
【答案】C
【解析】
亚硫酸钠与浓硫酸反应生成二氧化硫,二氧化硫能使品红溶液褪色,二氧化硫是酸性氧化物,与碱反应生成盐和水,碘单质具有氧化性,能够氧化二氧化硫生成硫酸,据此分析解答。
A.a棉球中品红褪色,可以验证SO2具有漂白性,A错误;
B.碘与SO2和水反应生成氢碘酸和硫酸,碘单质反应完全,c棉球蓝色褪去,根据反应硫元素化合价升高,可以验证SO2具有还原性,B错误;
C.b棉球褪色,SO2与碱液反应,碱性减弱,酚酞溶液褪色,验证SO2具有酸性氧化物的性质,C正确;
D.SO2尽管有还原性,但不能被浓硫酸氧化,因此不能用浓硫酸吸收尾气,SO2具有酸性氧化物的性质,可以用碱液吸收尾气,D错误。
答案选C。


科目:高中化学 来源: 题型:
【题目】将0.8g NaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1 mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是( )
A.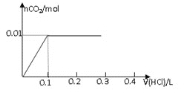
B.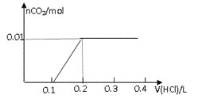
C.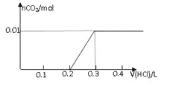
D.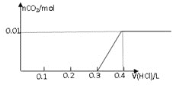
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将O2、CH4、Na2O2置于密闭容器中,在250℃下用电火花引发化学反应。反应停止后使容器内恢复至250℃,容器内的气压为零。由此得出的结论正确的是( )
A. 原O2、CH4、Na2O2物质的量之比为1∶2∶6,反应后容器内生成的固体是Na2CO3和NaOH
B. 原O2、CH4、Na2O2物质的量之比为2∶1∶4,反应后容器内生成的固体是Na2CO3和NaOH
C. 原O2、CH4、Na2O2物质的量之比为1∶2∶6,反应后容器内生成的固体是Na2CO3和NaHCO3
D. 原O2、CH4、Na2O2物质的量之比为2∶1∶4,反应后容器内生成的固体是NaHCO3和NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高岭土主要由高岭石![]() 长期风化而成,其中还含有一定量的白云石
长期风化而成,其中还含有一定量的白云石![]() ,高岭土是制作陶瓷的原料。完成下列填空:
,高岭土是制作陶瓷的原料。完成下列填空:
(1)矿石中除![]() 外的三种非金属元素的原子半径从小到大的顺序是______。硅原子的核外电子排布式是___,镁原子核外有_________种能量不同的电子。
外的三种非金属元素的原子半径从小到大的顺序是______。硅原子的核外电子排布式是___,镁原子核外有_________种能量不同的电子。
(2)判断![]() 的金属性强于
的金属性强于![]() 的事实是____________。
的事实是____________。
a. ![]() 的碱性强于
的碱性强于![]()
b. ![]() 微溶于水,
微溶于水,![]() 难溶于水
难溶于水
c. 与热水反应,钙比镁剧烈
d. 单质钙保存在煤油里,单质镁不需要
(3)![]() 和
和![]() 同是ⅣA族元素的氧化物,
同是ⅣA族元素的氧化物,![]() 的熔点明显比
的熔点明显比![]() 高的原因是________。
高的原因是________。
(4)氮化硅(![]() )是一种新型陶瓷材料,制备反应如下:
)是一种新型陶瓷材料,制备反应如下:![]() ,该反应的平衡常数表达式___________;反应达到平衡后,若增大
,该反应的平衡常数表达式___________;反应达到平衡后,若增大![]() 浓度,则
浓度,则![]() 值____________(填“增大”“减小”或“不变”)。
值____________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸合成治疗禽流感的药物—达菲(Tamiflu)的原料之一。莽草酸是A的一种异构体。A的结构简式如下:
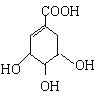 (提示:环丁烷
(提示:环丁烷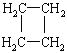 可简写成
可简写成![]() )
)
(1)A与溴的四氯化碳溶液反应的化学方程式_________;
(2)A与乙醇反应的化学方程式________;
(3)17.4g A与足量碳酸氢钠溶液反应,计算生成二氧化碳的体积(标准状况)____L;
(4)A在浓硫酸作用下加热可得到B(B的结构简式为![]() ),其反应类型为___。
),其反应类型为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)中国的高铁技术居于国际领先地位。
①高铁座椅内填充有聚氨酯软质泡沫。聚氨酯属于____(填字母)。
a.金属材料 b.无机非金属材料 c.有机高分子材料
②高铁信息传输系统中使用了光导纤维。光导纤维的主要成分是____(填字母)。
a.铜 b.石墨 c.二氧化硅
③高铁轨道建设需用大量水泥。生产水泥的主要原料为黏土和____(填字母)。
a.石灰石 b.粗盐 c.纯碱
(2)营养均衡有利于身体健康。
①人体内提供能量的主要营养物质为____、糖类和蛋白质。淀粉在人体内水解的最终产物是____。
②维生素是人体需要的营养物质。如图为某品牌维生素C泡腾片说明书的部分内容。该泡腾片中添加的着色剂是____,甜味剂是___。泡腾片溶于水时产生“沸腾”效果,是由于添加的酒石酸和___反应释放出了气体。

(3)煤炭在我国能源结构中占有重要地位,合理使用有利于社会可持续发展。
①控制燃煤产生的SO2排放,能够减少____型酸雨的形成。燃煤排放的烟气中还含有其他污染物,请列举一种:_____。
②燃煤产生的CO2用NH3处理可生产多种化工产品。用氨水吸收CO2可制得碳铵(NH4HCO3),写出该反应的化学方程式_____。用液氨与CO2反应可制备尿素[CO(NH2)2]。尿素和碳铵这两种氮肥中,氮元素的质量分数较高的是_____。
③煤的气化和液化是实现能源清洁化的重要途径。水煤气中CO和H2在加热、加压和催化剂存在条件下可以合成液体燃料(CH3OH),该反应的化学方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)改善空气质量、保护水土资源是实现美丽中国的基础。
①下列气体的排放会导致酸雨形成的是________(填字母,下同)。
a. CH4 b. CO c. SO2
②下列处理废水的方法属于中和法的是________。
a. 用熟石灰处理废水中的酸
b. 用臭氧处理废水中的氰化物
c. 用铁粉回收废水中的铜
③下列做法会造成土壤重金属污染的是________。
a. 作物秸杆露天焚烧
b. 废干电池就地填埋
c. 废旧塑料随意丢弃
(2)新鲜牛肉含蛋白质、脂肪、糖类、维生素A、维生素C、钙、铁等,其中:
①属于人体所需微量元素的是________。
②属于脂溶性维生素的是________。
③可为人体提供能量的是________、________和________。
(3)材料的发展与应用促进了人类社会的进步。
①碳晶地暖环保、节能、安全,其构造如图所示。其中属于金属材料的是________;属于硅酸盐材料的是________;属于高分子材料的是挤塑板和________。
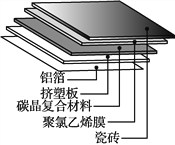
②吸附材料具有多孔、表面积大的特点。活性炭吸附NO2的过程中,会伴有C与NO2的反应,产物为两种常见无毒气体。写出该反应的化学方程式:_________________________________________。
③LiMn2O4是锂离子电池的一种正极材料,可通过MnO2与Li2CO3煅烧制备,同时还生成CO2和一种单质。写出该反应的化学方程式:_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用系统命名法命名: ![]() ____________________________________。
____________________________________。
(2)2,6-二甲基-4-乙基辛烷的结构简式是_______________________,1 mol该烃完全燃烧需消耗氧气____mol。
(3)在烃的分子结构中,若每减少2个氢原子,则相当于碳碳间增加1对共用电子。试完成下列问题:
①分子式为CnH2n+2的烃分子中碳碳间共用电子对数为______。
②碳碳间共用电子对数为n的单烯烃的分子式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式正确的是
A.硫化氢溶于水:H2S![]() 2H++S2-
2H++S2-
B.熔融状态下的NaHSO4:NaHSO4=Na++H++SO42-
C.碳酸氢钠溶于水:NaHCO3=HCO3-+Na+
D.醋酸溶于水:CH3COOH=CH3COO-+H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com