
����Ŀ����ͼ����ʵ���ҽ��а��������Ʊ�������̽��ʵ������װ�ã����̶ֹ�װ��δ������
��1��װ��B��ʢ�ŵ��Լ���________________��װ��D��������____________��
��2����ȼC���ƾ��ƣ����յ��ɼ�2�����ɼ�1���ӷ�Һ©���ų�Ũ��ˮ����û��ƿ�й����رշ�Һ©���������Ե�Ƭ�̣�װ��C�к�ɫ������죬װ��E����Һ����ִ������ݣ�ͬʱ������ɫ��������E���ݳ�Һ����������ֱ�������������д����C�з�����Ӧ�Ļ�ѧ����ʽ��__________________________��E�з�����Ӧ�����ӷ���ʽ��________��
��3����C�й���ȫ�����ɫ�رյ��ɼ�1�������ƿ��ƾ��ƣ�����ȴ����C�й�������������Ӧǰ��������Ϊ16g����Ӧ�������������2.4g��ͨ������ȷ���ù������ijɷ�______________________________(�û�ѧʽ��ʾ)��
��4���ڹرյ��ɼ�1���ɼ�2�������������F�У��ܿ췢��װ��F�в������̣�ͬʱ����G����ҺѸ�ٵ�������F�У�д���������̵Ļ�ѧ����ʽ��________________��Ѹ�ٲ���������ԭ����________��
���𰸡���ʯ��(����ʯ��) ��ֹ������ȫƿ 2NH3+3CuO![]() 3Cu+N2+3H2O 2NH3+Ba2+ +SO2+H2O=BaSO3��+2NH4+ Cu2O��Cu 3Cl2+8NH3=N2+6NH4Cl ʢ�������ļ���ƿ��������HCl��Ӧ���ɹ��壬����ƿ��ѹǿ��С��������Һ����
3Cu+N2+3H2O 2NH3+Ba2+ +SO2+H2O=BaSO3��+2NH4+ Cu2O��Cu 3Cl2+8NH3=N2+6NH4Cl ʢ�������ļ���ƿ��������HCl��Ӧ���ɹ��壬����ƿ��ѹǿ��С��������Һ����
��������
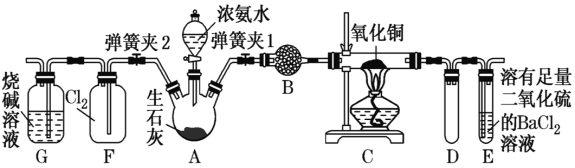
��ʵ���Ŀ�����Ʊ�������̽�������ʡ��۲�ʵ��װ��ͼ��AΪ�����ķ���װ�ã�BΪ����װ�ã������⣨2����3���������Ƴ�C��E��̽��������ԭCuO��ʵ�飬C�з������ǰ�����ԭCuO��D���ӵ�E������Һ����D��Ϊ�˷�ֹ������E��Ϊ��̽��NH3��SO2�ķ�Ӧ�������հ����������⣨4�������Ƴ�F��G��̽��������Cl2�ķ�Ӧ��
��1��BΪ����װ�ã����й���Ϊ��ʯ�ң�����ʯ�ң���DΪ��ȫƿ���������Ƿ�ֹ������
��2����E�з�����Ӧ��SO2+2NH3+H2O+BaCl2=BaSO3��+2NH4Cl�����ӷ���ʽΪ2NH3+Ba2++SO2+H2O=BaSO3��+2NH4+��E���ݳ������壬����ֱ���ŷŵ�������������岻�����ǰ������Ұ�����������ˮ�����������غ㶨�ɣ���C�еķ�Ӧ�ǰ�����ԭCuO�ķ�Ӧ�������Ƴ�������Ϊ������C�еĻ�ѧ����ʽΪ2NH3+3CuO![]() 3Cu+N2+3H2O��
3Cu+N2+3H2O��
��3����Ӧǰ����ΪCuO��n(CuO)=![]() =0.2mol����Ӧ�����ȫ��Ϊ��ɫ�������ù���ȫ��ΪCu����n(Cu)=0.2mol��m(Cu)=0.2mol��64g/mol=12.8g����m=16g-12.8g=3.2g>2.4g����Ӧ��Ĺ��岻����ֻ��Cu������Ӧ��Ĺ���ΪCu��Cu2O��
=0.2mol����Ӧ�����ȫ��Ϊ��ɫ�������ù���ȫ��ΪCu����n(Cu)=0.2mol��m(Cu)=0.2mol��64g/mol=12.8g����m=16g-12.8g=3.2g>2.4g����Ӧ��Ĺ��岻����ֻ��Cu������Ӧ��Ĺ���ΪCu��Cu2O��
��4��F�в����İ���ΪNH4Cl����ѧ����ʽΪ3Cl2+8NH3=N2+6NH4Cl��ʢ�������ļ���ƿ��������HCl��Ӧ���ɹ��壬����ƿ��ѹǿ��С��������Һ������


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ�������ƹ�ʹ������ȼ�ϵ�صĹ���������ij������������Ϊ30%��KOH��ҺΪ����ʵ�����ȼ�ϵ����ʹ��ʱ�ĵ缫��Ӧ���£�2H2 +4OH- - 4e-![]() 4H2O�� O2 + 2H2O + 4e-
4H2O�� O2 + 2H2O + 4e-![]() 4OH- �������йظ�����ȼ�ϵ�ص�˵���У�����ȷ����( )
4OH- �������йظ�����ȼ�ϵ�ص�˵���У�����ȷ����( )
A.�õ�ع���һ��ʱ���KOH��Һ��Ũ������
B.����ʱ���ܷ�ӦΪ��2H2 + O2![]() 2H2O
2H2O
C.ȼ�ϵ�ص���Դ�����ʽϸߣ��������������Ժ�
D.��ȼ�ϵ�ؿ���������������ͬ�ĵ缫
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и���������ָ����Һ���ܴ���������ǣ� ��
A.pH=l����Һ�У�Fe2+��NO3����SO42����Na+
B.��ˮ�����c(H+)=1��10��14mo1��L��1����Һ�У�Ca2+��K+��Cl����HCO3��
C.![]() =1013����Һ�У�NH4+��Al3+��NO3����Cl��
=1013����Һ�У�NH4+��Al3+��NO3����Cl��
D.c(Fe3+)=0.1mol��L��1����Һ�У�K+��ClO����SO42����SCN��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ܱ������зֱ����N2��H2��O2�������壬���¸��������������ȷ����(����)
A.�����ǵ�������¶ȡ�ѹǿ����ͬʱ������������ܶȣ���(H2)>��(N2)>��(O2)
B.�����ǵ��¶Ⱥ��ܶȶ���ͬʱ�����������ѹǿ��P(H2)>P(N2)>P(O2)
C.�����ǵ��������¶ȡ�ѹǿ����ͬʱ����������������V(O2)>V(N2)>V(H2)
D.�����ǵ�ѹǿ��������¶Ⱦ���ͬʱ�����������������m(H2)>m(N2)>m(O2)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֶ�����Ԫ��X��Y��Z��M��N����ԭ�Ӱ뾶��ԭ�������Ĺ�ϵ��ͼ������˵��������ǣ� ��

A. �ǽ����ԣ�X>Z
B. ��̬�⻯����ȶ��ԣ�M<N
C. X��Y�γɵĻ�����ֻ���ܺ����Ӽ�
D. M����������Ӧ��ˮ������һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£������ܱ������з�����Ӧ��4NH3��g��+5O2��g��![]() 4NO��g��+6H2O����g����������������˵���÷�Ӧ��ƽ����ǣ�������
4NO��g��+6H2O����g����������������˵���÷�Ӧ��ƽ����ǣ�������
A.V��������O2����![]() V���棩��NO��B.�ܱ�������������ܶȲ��ٸı�
V���棩��NO��B.�ܱ�������������ܶȲ��ٸı�
C.�ܱ�������ѹǿ����D.������Ũ�Ȳ��ٸı�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȥ�����е����� CaCl2��MgCl2 �� Na2SO4,�������£�
![]()
�����й�˵���У�����ȷ����( )
A. ��ȥ Mg2+����Ҫ��Ӧ�� Mg2++ 2OH-=Mg(OH)2��
B. �Լ���һ������Na2CO3��Һ
C. ���� SO42-�Ƿ������ȡ������Һ����ϡ�����ữ���ټ� BaCl2 ��Һ
D. ��Һ��ϡ����ʱֻ������Ӧ��H+ +OH- =H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ɶ��������Ƹߴ�����������£������ж��д������

A. �٢ڢ۾�����������ԭ��Ӧ B. H2��HCl����ѭ������
C. SiO2��һ�ּ�Ӳ���۵Ĺ��� D. SiHCl3Ħ������Ϊ135.5g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Թ��ȸʯ[��Ҫ�ɷ�ΪCuCO3��Cu(OH)2��CuSiO3��2H2O,��SiO2��FeCO3��Fe2O3������]Ϊԭ���Ʊ�CuCl2�Ĺ�����������:

��֪: SOCl2+H2O![]() SO2��+2HCl��������˵������ȷ����
SO2��+2HCl��������˵������ȷ����
A. ������� ʱӦ���������ܽ���ȸʯ��
B. ��������ʱ������Ӧ�����ӷ���ʽΪ��Cl2+2Fe2+![]() 2Fe3++2Cl-
2Fe3++2Cl-
C. ����pH��ʱ��pH������ڼ�������֤��Ԫ��ȫ����Fe(OH)3��ʽ��ȥ
D. ��������ˮ��ʱ������SOCl2��Ŀ�������ɵ�HCl����CuCl2��ˮ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com