
【题目】下列叙述不正确的是
A. 乙醇、乙烯和植物油都能使酸性高锰酸钾溶液褪色
B. 乙醇、乙烷、乙酸都可以与钠反应生成氢气
C. 乙烯能使酸性高锰酸钾溶液褪色
D. 用灼烧闻气味的方法可以区分纯棉织物和纯毛织物
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案科目:高中化学 来源: 题型:
【题目】下图所示与对应叙述相符的是
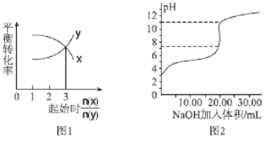
A.—定条件下,X和Y反应生成Z,由图1推出该反应的方程式可表示为:X+3Y![]() Z
Z
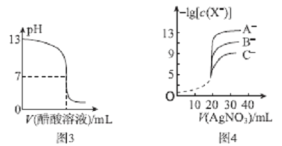
B.图2表示NaOH溶液滴加到0.lmol/L的一元酸溶液得到的滴定曲线(常温下),该实验最好选取酚酞作指示剂
C.常温下,向NaOH溶液中逐滴加入等浓度的醋酸溶液,所得滴定曲线如图3所示。当7<pH<13时,溶液中c(Na+)> c(CH3COO- )>c(OH-)>c(H+)
D.用硝酸银溶液滴定等浓度的A-、B-、C-的混合溶液(均可以与 Ag+反应生成沉淀),由图4可确定首先沉淀的是C-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、X是中学化学中常见的4种物质,它们均由短周期元素组成,转化关系如图所示。请针对以下两种情况回答下列问题。
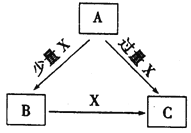
(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,将A、C的水溶液混合可得白色胶状沉淀B。
① A中含有的金属元素为__________(填元素名称)。
②该金属元素的单质与某氧化物在高温下反应,可用于焊接铁轨,此反应的化学方程式为:__________。
(2)若A、B、C的焰色反应均呈黄色,水溶液均呈碱性。
① A中所含有的化学键是________、__________。
②将4.48 L(标准状况下)X通入100 mL3 mol/LA的水溶液后,溶液中离子浓度由大到小的顺序为__________。
③自然界中存在由B或C与H2O按一定比例结晶而成的固体。将一定置的由C与H2O按一定比例形成的晶体溶于水配制成100 mL溶液,测得溶液中金属阳离子的浓度为0.5mol/L。若取相同质量的此晶体加热至恒重,剩余固体的质量为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下向10mL0.1mol·L-1的HR溶液中逐滴滴入0.1 mol·L-1的NH3·H2O溶液,所得溶液pH及导电性变化如图。下列分析不正确的是
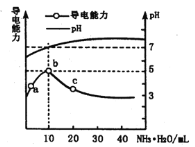
A.ab点导电能力增强,说明HR为弱酸
B.b点溶液pH=7说明NH4R没有发生水解
C.c 点溶液存在 c(NH4+)>c(R-)、c(OH-)>c(H+)
D.b~c任意点溶液均有 c(H+)·c(OH-)=KW=1.0×10-14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数
B. 电离能最小的电子能量最高
C. 同是s能级,在不同的电子层中所能容纳的最多电子数是不相同的
D. 核外电子排布完全相同的两种微粒,其化学性质一定相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小明体检的血液化验单中,葡萄糖为5.9mmol/L。表示该指标的物理量是( )
A.溶解度(s) B.物质的量浓度(c) C.质量分数(w) D.摩尔质量(M)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,对于可逆反应X(g)+3Y(g)![]() 2Z(g),若X、Y、Z的起始浓度分别为 c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1mol/L、0.3mol/L、0.08mol/L,则下列判断正确的是( )
2Z(g),若X、Y、Z的起始浓度分别为 c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1mol/L、0.3mol/L、0.08mol/L,则下列判断正确的是( )
A. c1:c2=3:1
B. 平衡时,Y和Z的生成速率之比为2:3
C. X、Y的转化率相等
D. c1的取值范围为0.04 mol/L<c1<0.14 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)![]() 2SO3(g)△H<0
2SO3(g)△H<0
(1)如果2min内SO2的浓度由6mol/L下降为2mol/L,那么,用O2浓度变化来表示的反应速率为 .
(2)某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如图1所示.根据图示回答下列问题:
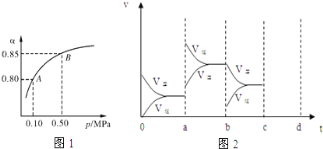
平衡状态由A变到B时平衡常数K(A) K(B)(填“>”、“<”或“=”).
(3)此反应在恒温密闭的装置中进行,能充分说明此反应已达到平衡的标志是 (填字母).
A.接触室中气体的平均相对分子质量不再改变
B.接触室中SO2、O2、SO3的浓度相同
C.接触室中SO2、SO3的物质的量之比为2:1:2
D.接触室中压强不随时间变化而变化
(4)图2表示该反应在密闭容器中达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a~ b过程中改变的条件可能是 ;b~c过程中改变的条件可能是 ; 若增大压强时,请把反应速率变化情况画在c~d处.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【物质结构与性质】钛被称为“国防金属”和“生物金属”,是重要的结构材料。
(1)基态钛原子的核外电子排布式是 。
(2)金红石(TiO2)的熔点1825℃,用熔盐法直接电解金红石可获得金属钛,金红石所属的晶体类型是 晶体。
(3)TiCl4能与NH4Cl反应生成配合物(NH4)2[TiCl6]。
①此配合物中,形成配位键时提供孤对电子的有 。(填元素符号)
②与NH4+互为等电子体的一种阴离子为 。(填化学式)
(4)TiO2+与H2O2在稀酸中反应生成橘红色的[TiO(H2O2)]2+离子,可用于钛的定性检验。下列关于H2O2的说法正确的是 。(填序号)
A.空间构型为直线形 |
B.含非极性键的极性分子 |
C.O原子轨道杂化类型为sp3 |
D.化学性质不稳定是因为氢键的键能较小 |
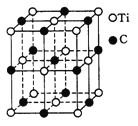
(5)最近发现一种由钛(Ti)原子和碳原子构成的气态团簇分子,结构模型如图所示,它的分子式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com