
【题目】A、B、C、X是中学化学中常见的4种物质,它们均由短周期元素组成,转化关系如图所示。请针对以下两种情况回答下列问题。
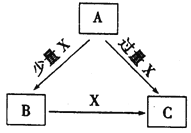
(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,将A、C的水溶液混合可得白色胶状沉淀B。
① A中含有的金属元素为__________(填元素名称)。
②该金属元素的单质与某氧化物在高温下反应,可用于焊接铁轨,此反应的化学方程式为:__________。
(2)若A、B、C的焰色反应均呈黄色,水溶液均呈碱性。
① A中所含有的化学键是________、__________。
②将4.48 L(标准状况下)X通入100 mL3 mol/LA的水溶液后,溶液中离子浓度由大到小的顺序为__________。
③自然界中存在由B或C与H2O按一定比例结晶而成的固体。将一定置的由C与H2O按一定比例形成的晶体溶于水配制成100 mL溶液,测得溶液中金属阳离子的浓度为0.5mol/L。若取相同质量的此晶体加热至恒重,剩余固体的质量为________________。
【答案】(1)①铝(1分)②2Al+Fe2O3![]() Al2O3+2Fe(2分)
Al2O3+2Fe(2分)
(2)①离子键(1分)共价键(1分)
②c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)(2分)③2.65g(2分)
【解析】
试题分析:(1)若A、B、C中均含同一种常见金属元素,将A、C的水溶液混合可得B的沉淀,由转化关系可知,A含有铝离子,B为氢氧化铝,C含有偏铝酸根,x为氢氧化钠。
①A、B、C中含有的同一种常见金属元素为Al;
②该金属元素的单质与某氧化物在高温下反应,可用于焊接铁轨,此反应是铝热反应,反应的化学方程式为2Al+Fe2O3![]() 2Fe+Al2O3;
2Fe+Al2O3;
(2)若A、B、C的焰色反应均呈黄色,水溶液均为碱性,则A为氢氧化钠,B为碳酸钠,C为碳酸氢钠,X为二氧化碳;
①A为氢氧化钠,属于离子化合物,钠离子与氢氧根离子之间形成离子键,氢氧根离子中氧原子与氢原子之间形成1对共用电子对,为共价键,属于A中所含有的化学键是 离子键、共价键;
②将4.48 L(0.2mol)(标准状况下)CO2通入100mL 3 mol/L NaOH的水溶液后,溶液为Na2CO3、NaHCO3等浓度混合溶液,CO32―水解能力强于HCO3―,各离子浓度关系为:c(Na+)>c(HCO3-)>c(CO32- )>c(OH-)>c(H+);
③自然界中存在B、C和H2O按一定比例结晶而成的固体。取一定量该固体溶于水配成100mL溶液,测得溶溶中金属阳离子的浓度为0.5mol·L-1,即钠离子浓度为0.5mol·L-1,取相同质量的固体加热至恒重,剩余固体为碳酸钠,根据钠离子守恒可知,碳酸钠的质量为1/2×0.1L×0.5mol·L-1×106g·mol-1=2.65g。


科目:高中化学 来源: 题型:
【题目】已知:2H2(g)+O2(g)===2H2O(l);ΔH=-571.6 kJ·mol-1
CO(g)+![]() O2(g)===CO2(g);ΔH=-282.8 kJ·mol-1
O2(g)===CO2(g);ΔH=-282.8 kJ·mol-1
现有CO、H2和CO2组成的混合气体112.0 L(标准状况)完全燃烧后放出的总热量为851.4 kJ,并生成18 g液态水。则燃烧前混合气体中CO的体积分数为
A.80% B.40% C.60% D.20%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化工厂用氯气与石灰乳生产漂白粉.该厂出厂产品说明书如下:

(1)漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的2个化学反应方程式:
① ;
② .
(2)某实验室研究员将完全变质后的漂白粉溶于水,往其中加入足量稀硝酸,收集到标准状况下448mL气体,则该漂白粉中所含有效成份的质量为 .(假设漂白粉中的其它成份不与稀硝酸反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中某实验小组同学关于硫酸铜的制取和应用,设计了以下实验:

(1)装置A中发生反应的化学方程式为________________________。
(2)为符合绿色化学的要求,某同学进行如下设计:将铜粉在___________(填仪器名称)中反复的灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应,反应后溶液经过_________、___________、过滤、洗法、干燥,即可得到产品CuSO4·5H2O晶体。
(3)将空气或氧气直接通入到钢粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4作催化剂,即发生反应,生成硫酸铜。其反应过程的第2步是:___________,Fe3++Cu==2Fe2++Cu2+,请写出其第1步反应的离子方程式_________________。
(4)制取的CuSO4溶液和“另一物质”在40~50℃混合时生成了一种难溶物质氢化亚铜(CuH)。将CuH溶解在稀盐酸中时生成了一种气体,这种气体是 _____________,经收集测定生成的该气体为标况下11.2 L,则被还原的离子得电子的物质的量是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )。
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据化学反应的实质是旧键断裂和新键形成这一观点,下列不属于化学变化的是
A. 食醋除垢 B. 胆矾晶体受热由蓝色变白色
C. 在稀盐酸中滴入紫色石蕊试液,溶液变红 D. 液氨变成氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应达到平衡的根本原因是
A. 反应混合物中各组分的浓度相等 B. 正逆反应都还在继续进行
C. 正逆反应的速率均为零 D. 正逆反应的速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A. 乙醇、乙烯和植物油都能使酸性高锰酸钾溶液褪色
B. 乙醇、乙烷、乙酸都可以与钠反应生成氢气
C. 乙烯能使酸性高锰酸钾溶液褪色
D. 用灼烧闻气味的方法可以区分纯棉织物和纯毛织物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A. 苯与浓硝酸、浓硫酸共热并保持55~60℃反应生成硝基苯
B. 苯乙烯在合适条件下催化加氢可生成乙基环己烷
C. 乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷
D. 甲苯与氯气在光照下反应主要生成2,4-二氯甲苯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com