
【题目】下列各组物质中,属于同素异形体的是( )
A.冰与干冰B.H2O与H2O2C.石墨与C60D.木炭与活性炭
科目:高中化学 来源: 题型:
【题目】工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g)+2H2(g)CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化.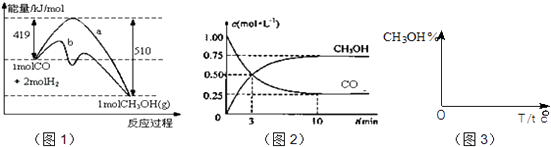
请回答下列问题:
(1)在“图1”中,曲线(填:a或b)表示使用了催化剂;该反应属于反应.
(2)下列说法正确的是 .
A.起始充入的CO为2mol
B.增加CO浓度,CO的转化率增大
C.容器中压强恒定时,反应已达平衡状态
D.保持温度和密闭容器容积不变,再充入1molCO和2molH2 , 再次达到平衡时,n(CH3OH)/n(CO)会减小
(3)从反应开始到建成平衡,v(H2)=;该温度下CO(g)+2H2(g)CH3OH(g)的化学平衡常数值为 . 若保持其它条件不变,将反应体系升温,则该反应化学平衡常数(填“增大”、“减小”或“不变”).
(4)请在“图3”中画出平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出P1、P2 , 且P1<P2).
(5)有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是
A、CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ/mol
B、CH3OH(g)+ ![]() O2(g)=CO2(g)+2H2O(g);△H=﹣192.9kJ/mol
O2(g)=CO2(g)+2H2O(g);△H=﹣192.9kJ/mol
又知H2O(l)=H2O(g)△H=+44kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列装置或操作描述正确的是( )
A.
图中若A为醋酸,B为贝壳,C为苯酚钠溶液,则可验证醋酸的酸性大于碳酸,但不能验证碳酸的酸性大于苯酚
B.
图用于实验室制乙烯
C.
图用于实验室制乙炔并验证乙炔可以发生氧化反应
D.
图用于实验室中分馏石油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯酰胺(CH2═CH﹣CONH2)具有中等毒性,它对人体可造成神经毒性和遗传毒性,可致癌.含淀粉的食物在经油炸之后,都会产生丙烯酰胺.已知有机物H是丙烯酰胺的相邻同系物,A为气态烃,分子中含有支链,其分子式为C4H8;F为三元环状化合物.回答下列问题:
(1)D中含有的官能团名称为 .
(2)A的结构简式为 , K的结构简式为 .
(3)指明下列反应类型:A→B , E→G .
(4)写出下列反应的化学方程式:
C→D .
E→F .
(5)E的同分异构体有多种,其中满足下列条件的E的同分异构体R有种.
①能发生银镜反应;②能与金属钠反应放出H2;③能发生水解反应.
写出核磁共振氢谱中有3个吸收峰的R的结构简式: .
(6)若B中含有两个氯原子,B的同分异构体有多种,试推断B的同分异构体的数目(包括B,不考虑立体异构).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的分类正确的是
A.混合物:空气、矿泉水、水银B.酸性氧化物:CO2 、SO2、 CO
C.盐:醋酸钠、氯化铵、纯碱D.电解质:CH3COOH、H2O、NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将冰醋酸加水稀释的过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示.
请回答下列问题:
(1)“O”点冰醋酸不能导电的原因是 .
(2)a、b、c三点对应的溶液中,C(H+)由小到大的顺序为 . (填字母,后同)
(3)a、b、c三点对应的溶液中,CH3COOH的电离程度最大的是 .
(4)a、b、c三点对应的溶液中,水的电离程度最大的是 .
(5)若使c点对应的溶液中的c(CH3COO﹣)增大,在下列措施中,可行的是 (填字母,后同).
A.加热
B.加KOH固体
C.加水
D.加CH3COONa固体
E.加锌粒
(6)在稀释过程中,随着醋酸浓度的降低,下列各量始终保持增大趋势的是 .
A.C(H+)
B.H+物质的量
C.C(OH﹣)
D.![]() .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种元素位于短周期,原子序数依次增大,C基态原子核外有三个未成对电子,B与D形成的化合物BD与C的单质C2电子总数相等,CA3分子结构为三角锥形,D与E可形成E2D与E2D2两种离子化合物,D与F是同族元素.
根据以上信息,回答下列有关问题:
(1)写出基态时D的电子排布图 .
(2)写出化合物E2F2的电子式 , 化合物ABC的结构式 .
(3)根据题目要求完成以下填空:
BF32﹣中心原子杂化方式;D3中心原子杂化方式;
FD42﹣微粒中的键角;FD3分子的立体构型 .
(4)根据等电子原理,指出与BD2互为等电子体且含有C原子的微粒有、(要求写一种分子和一种离子).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com