
【题目】亚硝酸氯(ClNO)是有机合成中的重要试剂。亚硝酸氯可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+Cl2(g)![]() 2ClNO(g)。
2ClNO(g)。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酸氯,涉及如下反应:
①4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) ΔH1
2NaNO3(s)+2NO(g)+Cl2(g) ΔH1
②2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) ΔH2
NaNO3(s)+ClNO(g) ΔH2
③2NO(g)+Cl2(g)![]() 2ClNO(g) ΔH3
2ClNO(g) ΔH3
则ΔH1、ΔH2、ΔH3之间的关系为ΔH3=____________。
(2)已知几种化学键的键能数据如表(亚硝酸氯的结构为Cl-N=O,一氧化氮的结构为N≡O)
化学键 | N≡O | Cl-Cl | Cl-N | N=O |
键能/kJ mol-1 | 630 | 243 | a | 607 |
则2NO(g)+Cl2(g)![]() 2ClNO(g)反应的ΔH=_________kJ ·mol-1
2ClNO(g)反应的ΔH=_________kJ ·mol-1
(3)T℃时,2NO(g)+Cl2(g) ![]() 2ClNO(g)的正反应速率表达式为υ正=kcn(ClNO),测得速率和浓度的关系如下表:
2ClNO(g)的正反应速率表达式为υ正=kcn(ClNO),测得速率和浓度的关系如下表:
序号 | c(ClNO)/mol·L-1 | υ/mol·L-1· s-1 |
① | 0.30 | 3.6×10-8 |
② | 0.60 | 1.44×10-7 |
③ | 0.90 | 3.24×10-7 |
n=__________;k=___________(注明单位)。
(4)在2 L的恒容密闭容器中充入4mol NO(g)和2molCl2(g),在不同温度下测得c(ClNO)与时间的关系如图。
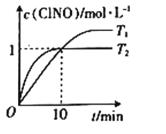
①由图可知T1、T2温度的速率υ1______υ2温度T1______T2。(填>、<或=)
②温度为T1时,能作为该反应达到平衡的标志的有__________。
a.气体体积保持不变 b.容器压强保持不变 c.气体颜色保持不变 d.υ(ClNO)=υ(NO) e.NO与ClNO的物质的量比值保持不变
③反应开始到10min时,Cl2的平均反应速率υ(Cl2)=_______________。
【答案】2ΔH2-ΔH1 289-2a 2 4×10-7L·mol-1·s-1 < < bce 0.05mol·L-1·min-1
【解析】
(1)根据盖斯定律,将方程式2×②-①得方程式③,则ΔH3=2ΔH2-ΔH1,本题答案为:2ΔH2-ΔH1;
(2)反应的焓变ΔH等于反应物总键能减去生成物总键能,即有ΔH=(630×2+243-607×2-2a)kJ ·mol-1=(289-2a)kJ ·mol-1,本题答案为:289-2a;
(3)根据表格信息计算可得,反应速率与ClNO浓度的平方成正比,所以n=2,将n=2代入υ正=kcn(ClNO),并将表中数据代入该式,计算可得k=4×10-7L·mol-1·s-1,本题答案为:2;4×10-7L·mol-1·s-1;
(4)①由图可知T1<T2,温度越高,速率越快,所以的速率υ<υ2,故本题答案为:<;<;
②a.恒容条件下,容器体积始终保持不变,不能据此判断平衡状态,故错误;
b.反应前后气体的物质的量减小,压强越小,当容器压强保持不变时,正逆反应速率相等,反应达到平衡状态,故正确;
c.只有氯气有颜色,当气体颜色保持不变,正逆反应速率相等,反应达到平衡状态,故正确;
d.υ(ClNO)=υ(NO) 时反应方向未知,无法确定是否达到平衡状态,故错误;
e.NO与ClNO的物质的量比值保持不变时,正逆反应速率相等,反应达到平衡状态,故正确;
故选bce;
③反应开始到10min时,同一时间段内各物质的反应速率之比等于其计量数之比,据此得
![]() ,故本题答案为:
,故本题答案为:![]() 。
。


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式书写均正确的是( )
A.用Cl2与NaOH溶液反应制漂白液:2OH-+Cl2=2ClO-+H2↑
B.SO2通入FeCl3溶液:2Fe3++SO2+2H2O=2Fe2++![]() +4H+
+4H+
C.向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+=H2SiO3+2Na+
D.H2SO4溶液与Ba(OH)2溶液反应:![]() +Ba2+=BaSO4↓
+Ba2+=BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.已知石墨比金刚石稳定,则反应C(石墨,s)=C(金刚石,s)为放热反应
B.物质发生化学反应时都伴随能量变化,则伴随能量变化的物质变化也一定是化学变化
C.相同条件下,如果1mol氧原子所具有的能量为E1,1mol氧分子所具有的能量为E2,则2E1=E2
D.已知![]()
![]() ,
,![]()
![]() ,则
,则![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是()
A. NaCl的摩尔质量是58.5gB. 64g氧气中含有2mol氧
C. 4g氦气中含有2mol氦原子D. 0.1molCO2中含有6.02×1022个CO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利尿酸在奥运会上被禁用,其结构简式如下图所示。下列叙述正确的是( )

A. 利尿酸衍生物利尿酸甲酯的分子式是C14H14Cl2O4
B. 利尿酸分子内处于同一平面的原子不超过10个
C. 1 mol利尿酸能与7 mol H2发生加成反应
D. 利尿酸能与FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2009年《化学教育》期刊封面刊载如图所示的有机物M(只含C、H、O)的球棍模型图。不同大小、颜色的小球代表不同的原子,小球之间的“棍”表示共价键,既可以表示三键,也可以表示双键,还可以表示单键。下列有关M的推断正确的是( )
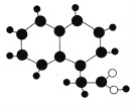
A. M的分子式为C12H12O2
B. M与足量氢气在一定条件下反应的产物的环上一氯代物有7种
C. M能发生中和反应、取代反应
D. 一个M分子最多有11个原子共面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述正确的是( )
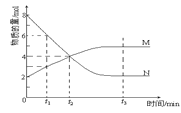
A.反应的化学方程式:2M![]() N
N
B.t2时,正、逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,表中所列的字母分别代表一种化学元素。

(1)a、b、c三种元素的原子半径由大到小的顺序是___(填元素符号);b、f、h三种元素对应简单氢化物的热稳定性由强到弱的顺序是___(填化学式)。
(2)c、d、e三种元素最高价氧化物对应水化物中碱性最强的是___(填水化物的化学式)。
(3)利用如图装置可比较a、e、h的非金属性强弱,则装置中试剂X、Z分别为___(填化学式)。
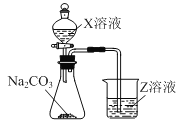
(4)元素i的原子结构示意图为___;写出元素i的最高价氧化物对应水化物溶液与元素d的单质反应的离子方程式___。
(5)推测原子序数为34的元素在周期表中的位置___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是中学化学中常见的物质,且A、B、C均含有同一种元素,在一定条件下相互转化关系如下图所示(部分产物已略去)。请回答:
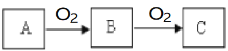
(1)若B是无色气体,C是红棕色气体。
① A、B、C所含相同元素在元素周期表中的位置是______。
② 下列说法正确的是______(填字母)。
a.常温下,A为无色气体
b.A、B、C中所含相同元素的化合价依次升高
c.C与水反应只做还原剂。
③若A是化合物,写出由A氧化生产B的化学方程式__________________。
(2)若B是一种有刺激性气味的有毒气体,C与水反应生成硫酸
① A、B、C所含相同元素的原子结构示意图是______。
② 下列说法不正确的是______(填字母)。
a.A一定是黄色晶体
b.可以用上述转化关系制备硫酸
c.B与水反应做还原剂。
③C的水溶液与氢氧化钠的反应为______________(填吸热或放热)反应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com