
【题目】下表为元素周期表的一部分,请参照元素①~⑦在表中的位置,用化学用语回答下列问题:
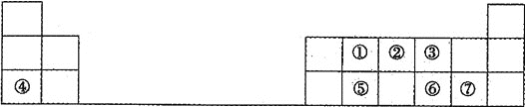
(1)①在周期表中的位置是__,②、⑤原子半径的大小关系为__(填元素符号)。
(2)①、⑤、⑦的最高价含氧酸的酸性由强到弱的顺序是__(填化学式)。
(3)③和⑥的气态氢化物稳定性强弱关系__(填化学式)。
(4)④和⑦两种单质形成的化合物含有的化学键__(填“共价键”或“离子键”),③和⑥两种单质反应的化学方程式__。
(5)②的最简单氢化物与其最高价氧化物对应水化物反应的离子方程式为__。
【答案】第二周期ⅣA族 r(Si)>r(N) HClO4>H2CO3>H2SiO3 H2O>H2S 离子键 S+O2![]() SO2 NH3+H+=NH
SO2 NH3+H+=NH![]()
【解析】
按元素在周期表中的位置可知,①为C、②为N、③为O、④为Na、⑤为Si、⑥为S、⑦为Cl,结合元素周期律回答;
(1)①是C,在周期表中的位置是第二周期ⅣA族,根据同主族原子电子层数越多其原子半径越大、同周期从左到右原子半径递减,则原子半径的大小关系r(Si)> r(C)>r(N),则r(Si)>r(N);
故答案为:第二周期ⅣA族;r(Si)>r(N);
(2)元素非金属性越强,其最高价氧化物的水化物酸性越强,①、⑤、⑦非金属性强弱顺序是Cl>C>Si,则其最高价含氧酸的酸性由强到弱的顺序是HClO4>H2CO3>H2SiO3;
答案为:HClO4>H2CO3>H2SiO3;
(3) 非金属性越强,气态氢化物稳定性就越强;根据同主族元素从上到下非金属性逐渐减弱可知,③和⑥的非金属性为O>S,则气态氢化物稳定性强弱关系为H2O>H2S;
答案为:H2O>H2S;
(4)④和⑦两种单质形成的化合物为氯化钠,是典型的离子化合物,含有的化学键为离子键,③的单质是氧气,⑥的单质是硫,反应的化学方程式为:S+O2![]() SO2;
SO2;
答案为:离子键;S+O2![]() SO2;
SO2;
(5)②的最简单氢化物为氨气,其最高价氧化物对应水化物为硝酸,两者反应生成硝酸铵,则反应的离子方程式为NH3+H+=NH![]() ;
;
答案为:NH3+H+=NH![]() 。
。


科目:高中化学 来源: 题型:
【题目】(1)CH≡CCH(CH3)2系统命名法命名为 。
(2) 2,3-二甲基-1-丁烯的结构简式为 。
(3)支链只有一个乙基且式量最小的烷烃的结构简式为 。
(4)某烃分子式为C6H14,若该烃不可能由炔烃与氢气加成得到则该烃的结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为元素周期表中原子序数依次增大的前36号元素,基态A原子的价电子排布式为nsnnpn,C原子基态时2p能级上有2个未成对的电子,D元素的原子结构中3d能级上成对电子数是未成对电子数的3倍,B与E同主族。
请回答下列问题:
(1)基态A原子的价电子轨道表示式为_______,其电子占据的最高能级的电子云形状为________。
(2)B、C、E三种元素的电负性由大到小的顺序为________(用元素符号表示)
(3)E的含氧酸有两种形式,化学式分别为H3EO3和H3EO4,则二者酸性强弱H3EO3_____H3EO4(填“>”“<”或“=”)
(4)D单质在AC气流中轻微加热,生成无色挥发性液态D(AC)4配合物,该配合物的晶体类型是_________。
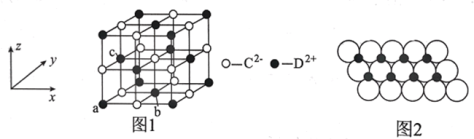
(5)DC晶胞结构如图1所示,离子坐标参数a为(0,0,0),b为(![]() ,
,![]() ,0),则c离子的坐标参数为________;一定温度下,DC晶体可自发地分散并形成“单层分子”,可以认为C2–作密置单层排列,D2+填充其中,如图2所示,C2–离子的半径为xm,阿伏加德罗常数的值为NA,则每平方米面积上分散的该晶体的质量为_____g(用含x、NA的代数式表示)。
,0),则c离子的坐标参数为________;一定温度下,DC晶体可自发地分散并形成“单层分子”,可以认为C2–作密置单层排列,D2+填充其中,如图2所示,C2–离子的半径为xm,阿伏加德罗常数的值为NA,则每平方米面积上分散的该晶体的质量为_____g(用含x、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化合物(a)![]() 、(b)
、(b)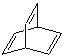 、(c)
、(c)![]() ,(d)
,(d)![]() ,下列说法不正确的是 ( )
,下列说法不正确的是 ( )
A. a、b、c、d互为同分异构体B. 除a外均可发生加成反应
C. c中所有原子不可能处于同一平面D. 一氯代物同分异构体最多的是c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置检验对应气体时,不能达到目的是( )
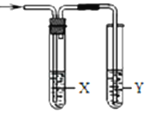
除杂装置 检验装置
生成的气体 | 试剂 | 试剂 | |
| 电石与水反应制取的乙炔 |
|
|
| 木炭与浓 | 饱和 | 澄清石灰水 |
|
| 水 |
|
|
|
|
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】扎来普隆是一种短期治疗失眠症的药物,其合成路线如下:

回答下列问题:
(1)A中的官能团名称是________________。
(2)![]() 所需的试剂和条件分别为________________。
所需的试剂和条件分别为________________。
(3)![]() 、
、![]() 的反应类型依次为________、________。
的反应类型依次为________、________。
(4)扎来普隆的分子式为________________。
(5)![]() 的化学方程式为________________________。
的化学方程式为________________________。
(6)属于芳香化合物,且含有硝基,并能发生银镜反应的B的同分异构体有________种(不考虑立体异构),其中核磁共振氢谱有4组峰的结构简式有________________。
(7)已知:![]() 有碱性且易被氧化。设计由
有碱性且易被氧化。设计由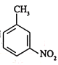 和乙醇制备
和乙醇制备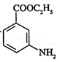 的合成路线(无机试剂任选)。________
的合成路线(无机试剂任选)。________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.用稀硫酸除去硫酸钠溶液中少量的硫代硫酸钠:S2O32-+2H+=SO2↑+S↓+H2O
B.KClO碱性溶液与Fe(OH)3反应:3ClO+2Fe(OH)3=2FeO42-+3Cl+4H++H2O
C.硬脂酸与乙醇的酯化反应:C17H35COOH+C2H518OH![]() C17H35COOC2H5+H218O
C17H35COOC2H5+H218O
D.向NH4HCO3溶液中加入足量石灰水:Ca2++HCO3-+OH=CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种以海水晒盐后所得苦卤(溶质主要含MgCl2,还有NaCl等)为原料制取金属镁的流程如图:
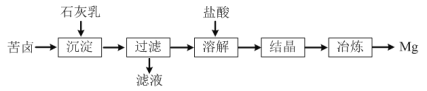
(1)“沉淀”反应的化学方程式为___。
(2)“溶解”反应的离子方程式为___。
(3)工业上冶炼镁时采用的方法是___(填字母)。
a.电解熔融MgCl2
b.用氢气还原MgCl2
c.加热分解MgCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,所使用的装置(夹持装置略)、试剂和操作方法都正确的是( )
A.观察Fe(OH)2的生成
B.配制一定物质的量浓度的NaCO3溶液
C.除去CO中的CO2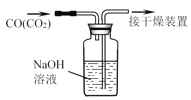
D.实验室模拟制备NaHCO3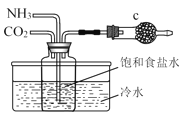
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com