
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 10g46%甲酸(HCOOH)水溶液所含的氧原子数为0.5NA
B. 1molCnH2n+2所含的共用电子对数为(2n+1)NA
C. 含有C﹣Si数目为2NA的SiC晶体中硅原子的物质的量为1mol
D. 常温下,5.6gFe与含0.2molHNO3的溶液充分作用,最少会失去电子数为0.15NA
【答案】A
【解析】
A.10g46%甲酸(HCOOH)水溶液含有溶质的物质的量n(HCOOH)=![]() ,其中含有O原子的物质的量为n(O)=2n(HCOOH)=0.2mol,该溶液中含有溶剂水的物质的量为n(H2O)=
,其中含有O原子的物质的量为n(O)=2n(HCOOH)=0.2mol,该溶液中含有溶剂水的物质的量为n(H2O)=![]() ,掌握水中所含的氧原子数为0.3mol,故该溶液中含有O原子的总物质的量为0.5mol,含有的O原子数目为0.5NA,A正确;
,掌握水中所含的氧原子数为0.3mol,故该溶液中含有O原子的总物质的量为0.5mol,含有的O原子数目为0.5NA,A正确;
B.在一个CnH2n+2中含有C-H键为2n+2,含有C-C键为n-1,故含有的共价键数目为3n+1个,则1molCnH2n+2所含的共用电子对数为(3n+1)NA,B错误;
C.每个Si原子与相邻的4个C原子形成共价键,所以SiC晶体中含4个Si-C键,若含有C-Si数目为2NA,则SiC晶体的物质的量是0.5mol,因此含有Si原子的物质的量为0.5mol,,C错误;
D.5.6gFe的物质的量是0.1mol,与0.2molHNO3反应,当硝酸为稀硝酸时。此时n(Fe):n(HNO3)=1:2>3:8,可知Fe过量,按照HNO3的量计算,还原产物为NO,1molHNO3有![]() 被还原,根据电子守恒可得转移的电子数目为0.2mol×
被还原,根据电子守恒可得转移的电子数目为0.2mol×![]() =0.15mol;若硝酸为浓硝酸,反应条件加热,若无情反应产生Fe(NO3)2,则Fe过量,反应按照HNO3计算,转移的电子数为0.2mol
=0.15mol;若硝酸为浓硝酸,反应条件加热,若无情反应产生Fe(NO3)2,则Fe过量,反应按照HNO3计算,转移的电子数为0.2mol![]() =0.1mol,至少转移0.1mol电子;电子数目为0.1NA,D错误;
=0.1mol,至少转移0.1mol电子;电子数目为0.1NA,D错误;
故合理选项是A。


科目:高中化学 来源: 题型:
【题目】I.无水MgBr2可用作催化剂,实验室采用镁屑与液溴为原料制备无水MgBr2,装置如图所示(夹持装置省略)。
已知:①Mg和Br2反应剧烈放热;MgBr2具有强吸水性
②MgBr2+3C2H5OC2H5![]() MgBr2·3C2H5OC2H5。
MgBr2·3C2H5OC2H5。

主要步骤如下:
步骤1:三颈烧瓶中装入10g镁屑和150mL无水乙醚;装置C中加入15mL液溴;
步骤2:缓慢通入干燥的氩气,直至溴完全导入三颈烧瓶中;
步骤3:反应完毕后恢复至室温,过滤除去镁,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品;
步骤4:常温下用CCl4溶解粗品,冷却至0℃,析岀晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解得无水MgBr2产品。
请回答下列问题
(1)仪器A的名称是___________。B的作用为___________。
(2)下列有关步骤4的说法正确的是___________(填选项字母)
A.可用75%的乙醇代替CCl4溶解粗品
B.加热至160℃的主要目的是除去CCl4
C.洗涤晶体可选用0℃的CCl4
D.该步骤只除去了可能残留的溴
(3)若将装置C改为装置D,可能会导致的后果是___________。
(4)为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,以铬黑T(简写为In)为指示剂。已知Mg2+与铬黑T和EDTA均能形成配合物,且EDTA与Mg2+配合更稳定:
物质 | 颜色 | 物质 | 颜色 |
Y4- | 无色 | MgY2- | 无色 |
In | 纯蓝色 | MgIn- | 酒红色 |
反应的离子方程式为Mg2++Y4-=MgY2-
①滴定终点的现象为______________________。
②测定前,先称取0.2500g无水MgBr2产品,溶解后,加入2滴铬黑T试液作指示剂,用0.0500mol·L-1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液25.00mL,则测得无水MgBr2产品的纯度是______________________(用质量分数表示)。
Ⅱ.化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时按如下化学方程式分解:2Mg5Al3(OH)19(H2O)4===27H2O+10MgO+3Al2O3。
(5)写出该化合物作阻燃剂的两条依据:______________________。
(6)MgO可溶于NH4Cl的水溶液,用离子方程式表示其原理:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 18.0 g葡萄糖和果糖的混合物中含有氢原子的数目为1.2 NA
B. 0.1 mol MgCl2中含有最外层电子的数目为1.6NA
C. 1 L 0.1 mol/L乙醇溶液中含有氧原子的数目为0.1 NA
D. 0.1 mol Fe与足量Cl2完全反应转移电子的数目为0.2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《茉莉花》是一首脍炙人口的江苏民歌。茉莉花香气的成分有多种,乙酸苯甲酯是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:

(1)A的结构式为 ________________;C的结构简式为_________________;
(2)写出反应①的化学方程式_________________;
(3)反应③的反应类型为__________________;
(4)C通常有三种不同类别的芳香族同分异构体,试写出另两种不同类别的同分异构体的结构简式(各写一种)______________;_______________。
(5)反应 ________(填序号)原子的理论利用率为100%,符合绿色化学的要求。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酚酯的合成方法之一是由酚与酰卤(![]() )反应制得。
)反应制得。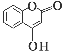 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
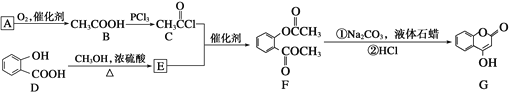
(1)A与银氨溶液反应有银镜生成,则A的结构简式是_________。
(2)B→C的反应类型是_________。
(3)E的结构简式是__________________。
(4)写出F和过量NaOH溶液共热时反应的化学方程式:__________。
(5)下列关于G的说法不正确的是________(填序号)。
a.能与溴单质反应 b.能与金属钠反应
c.1 mol G最多能和3 mol氢气反应 d.分子式是C9H6O3
(6)写出符合下列要求的D的所有同分异构体的结构简式_____。
①遇FeCl3溶液发生显色反应;
②能发生银镜反应
③最多能消耗3molNaOH。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮肥是最重要的化肥,它能使农作物枝叶茂盛,叶片增大,促进叶绿素的形成,从而有利于光合作用,提高农作物产量和质量。
(1)氮气分子的电子式是_________,氨气分子的空间形状为:__________。
(2)农谚有“雷雨发庄稼”一说。用化学方程式表示在闪电作用下游离态氮转化为化合态氮的过程_____.
(3)合成氨工业是氮肥的最主要来源。写出工业合成氨的化学方程式 _________________.
(4)合成氨工业也是硝酸工业的基础,写出氨催化氧化的化学方程式_____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三盐基硫酸铅(3PbO·PbSO4·H2O,其相对分子质量为990)简称“三盐”,不溶于水及有机溶剂。主要适用于不透明的聚氯乙烯硬质管、注射成型制品,也可用于人造革等软质制品。以铅泥 (主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如下图所示。


已知:KSP(PbSO4)=1.82×10-8,KSP(PbCO3)=1.46×10-13请回答下列问题:
(1)写出步骤①“转化”的离子方程式__________________。
(2)根据右图溶解度曲线(g/100g水),由滤液I得到Na2SO4固体的操作为:将“滤液1”、_________、_________、用乙醇洗涤后干燥。
(3)步骤③“酸溶”,为提高酸溶速率,可采取的措施是________________(任意写出一条)
(4)“滤液2”中可循环利用的溶质为_______(填化学式)。若步骤④“沉铅”后的滤液中c(Pb2+)=1.82×10-5 mol·L-1,则此时c(SO42-)=________mol·L-1。
(5)步骤⑥“合成”三盐的化学方程式为____________________。
(6)若消耗100.0t铅泥,最终得到纯净干燥的三盐49.5t,假设铅泥中的铅元素有75%转化为三盐,则铅泥中铅元素的质量分数为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)溶质的质量分数为14%的KOH溶液,经加热蒸发去100g水后,质量分数变成28%,体积为80mL,则此时溶液的物质的量浓度为
A. 5mol/L B. 6mol/L C. 6.25mol/L D. 6.75mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com