
����Ŀ������������Ҫ�Ļ��ʣ�����ʹũ����֦Ҷïʢ��ҶƬ���ٽ�Ҷ���ص��γɣ��Ӷ������ڹ�����ã����ũ���������������
��1���������ӵĵ���ʽ��_________���������ӵĿռ���״Ϊ��__________��
��2��ũ���С����귢ׯ�ڡ�һ˵���û�ѧ����ʽ��ʾ����������������̬��ת��Ϊ����̬���Ĺ���_____.
��3���ϳɰ���ҵ�ǵ��ʵ�����Ҫ��Դ��д����ҵ�ϳɰ��Ļ�ѧ����ʽ _________________.
��4���ϳɰ���ҵҲ�����Ṥҵ�Ļ�����д�����������Ļ�ѧ����ʽ_____________.
���𰸡�![]() ������ N2��O2
������ N2��O2 ![]() 2NO N2��3H2
2NO N2��3H2 ![]() 2NH3 4NH3��5O2
2NH3 4NH3��5O2 4NO��6H2O
4NO��6H2O
��������
��1�������������Ե���������ϣ����ݼ۲���ӶԻ��������ж���ռ乹�ͣ�
��2�������������£������еĵ�����������Ӧ����NO��
��3����ҵ�����������뵪���ɺϳɰ�����
��4�������Ĵ�������ָ�����������ڴ�������������һ��������ˮ�Ĺ��̡�
��1����ԭ������������Ϊ5��������ԭ��֮��������Թ��õ��ӣ����8�����ȶ��ṹ��N2�ĵ���ʽΪ![]() ��NH3���ӵŵ��Ӷ���Ϊ
��NH3���ӵŵ��Ӷ���Ϊ![]() =1���۲���Ӷ���=3+
=1���۲���Ӷ���=3+![]() =4����������ṹ�������Σ��ʴ�Ϊ��
=4����������ṹ�������Σ��ʴ�Ϊ��![]() �������Σ�
��������
��2���ڷŵ�������£������еĵ�����������������һ����������ѧ����ʽΪ��N2��O2 ![]() 2NO��
2NO��
��3�������������ڸ��¡���ѹ�ʹ��ӵ������»������ɰ����÷�Ӧ�����ϳɰ���Ӧ����ѧ����ʽΪ��N2��3H2 ![]() 2NH3��
2NH3��
��4��NH3�е�Ԫ��Ϊ-3�ۣ����л�ԭ�ԣ��ڴ����ͼ��������¿ɱ���������Ϊһ���������÷�Ӧ�������Ĵ�������Ӧ����ѧ����ʽΪ��4NH3��5O2 4NO��6H2O��
4NO��6H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ô�����CaCO3��100 mLϡ���ᷴӦ��ȡCO2��ʵ����̼�¼��ͼ��ʾ(CO2�����������Ϊ��״���µ����)�����з�����ȷ���ǣ� ��

A��OE�α�ʾ��ƽ���������
B��EF�Σ��������ʾ�÷�Ӧ��ƽ����Ӧ����Ϊ0.4 mol��L��1��min��1
C��OE��EF��FG�����У��÷�Ӧ�ö�����̼��ʾ��ƽ����Ӧ����֮��Ϊ2��6��7
D��F���ռ�����CO2�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ���õ��л�����ֻ��һ�ֵ���
A. ������ļ����������ڹ��������µ�ȡ����Ӧ
B. ��ϩ���Ȼ���ļӳɷ�Ӧ
C.  ��NaOH����Һ�����µ���ȥ��Ӧ
��NaOH����Һ�����µ���ȥ��Ӧ
D. �ױ���Һ�����廯�������������µ�ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ���ǣ�������
A. 10g46%����(HCOOH)ˮ��Һ��������ԭ����Ϊ0.5NA
B. 1molCnH2n+2�����Ĺ��õ��Ӷ���Ϊ(2n+1)NA
C. ����C��Si��ĿΪ2NA��SiC�����й�ԭ�ӵ����ʵ���Ϊ1mol
D. �����£�5.6gFe�뺬0.2molHNO3����Һ������ã����ٻ�ʧȥ������Ϊ0.15NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ����ѡ����Լ���װ�û�����(�г�װ������ ȥ)�ܴﵽ��Ӧʵ��Ŀ�ĵ���
A. ��ȡ��ˮ�е���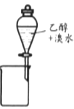
B. ��֤ʯ���ͷֽ�����к���ϩ��
C. ��֤H2O2 �ֽ�ʱ�������̵Ĵ�Ч�������Ȼ���
D. ��ȡ20.00mL 0.1000mol/L HCl��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�����ˮ����������ȷ����
A. ������ˮ��ֻ��Cl2��H2O����
B. ������ˮ��ʹ��ɫʯ����ֽ�ȱ�����ɫ
C. ������ˮ�������ݳ�����������Cl2
D. ��ˮ������������Լ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ֲ���纣�������к��зḻ�ĵ�Ԫ�أ�ʵ������Ӻ�������ȡ���������ͼ��
 ��ش�
��ش�
��1��д����ȡ�������й�ʵ����������ƣ���____����___��
��2���������õ�����Ҫ��������____��
��3����ȡ��Ĺ����У��ɼ�����л��ܼ���___�����������ú��ϲ��___ɫ���²��____ɫ��
��4��д���ڵ����ӷ���ʽ_____��
��5����ҵ��ȡ�õ��ĵ��������ҩƷ��������Ƭ�����ص�Ƭ��������Գɷ�Ϊ���ӵ⡣�������һ�ַ�������֤����Ƭ�еķ��ӵ⣬�䷽���ǣ���������������__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��POC13����Ҫ�Ļ���ԭ�ϣ�ij��ȤС���������Ȼ��ס����������������Ʊ�POC13�������л���һ����ˮǿ��ˮ�������SOC12��

��֪��PC13�۵㣭93.6�桢�е�76.1�棬��ˮǿ��ˮ�⣬����������Ӧ��POC13��ˮǿ��ˮ�⣬������PC13.
(1)������������________________��
(2)��֪װ��B�Ʊ�POC13�����������ӿ����ӵ�˳��Ϊa____d��װ��B�з�����Ӧ�Ļ�ѧ����ʽΪ_________________________��
(3)B�з�Ӧ�¶ȿ�����60��65�棬��ԭ����__________________________��
(4)�÷�����·��ⶨPOC13������ȷ��ȡ20.20g POC13��Ʒ������ʢ��60.00mL����ˮ��ˮ��ƿ��ҡ������ȫˮ�⣻��ˮ��Һ���100.00mL��Һ��ȡ10.00mL��Һ����ƿ�У�����10.00mL 3.200mol��L-1AgNO3����Һ����������������������ҡ����ʹ�������汻�л��︲�ǣ�����ָʾ������0.2000mol��L-1KSCN��Һ�ζ�������AgNO3��Һ���ﵽ�ζ��յ�ʱ����ȥ10.00mL KSCN��Һ��
����֪��KSP(AgC1)=3.2��10-10��KSP(AgSCN)=2��10-12��
��POC13ˮ��Ļ�ѧ��Ӧ����ʽΪ______________________________��
�ڵζ�ѡ�õ�ָʾ����__________(ѡ����ĸ)���ζ��յ������Ϊ__________��
a��FeC12 b��NH4Fe(SO4)2 c������ d������
�������������dz�����Ŀ����___________________________________��
�ܲ�Ʒ��POC13�İٷֺ���Ϊ____________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com