
【题目】下列叙述正确的是( )
A.1molH2O的质量为18g/mol
B.摩尔是国际单位制中的一个基本物理量
C.3.01×1023个SO2分子的质量为32g
D.C2H5OH的摩尔质量为46g
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:
【题目】在配制一定物质的量浓度的NaOH溶液时,下列哪个原因会造成所配溶液浓度偏高( )
A.所用NaOH已经潮解B.有少量NaOH溶液残留在烧杯里
C.向容量瓶中加水未到刻度线D.称量时误用“左码右物”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁、铜等金属离子是人体内多种酶的辅因子。工业上从海水中提取镁时,先制备无水氯化镁,然后将其熔融电解,得到金属镁。
(1)以MgCl2为原料用熔融盐电解法制备镁时,常加入NaCl、KCl或CaCl2等金属氯化物,其主要作用除了降低熔点之外还有________。
(2)已知MgO的晶体结构属于NaCl型。某同学画出的MgO晶胞结构示意图如图所示,请改正图中错误:__________________。
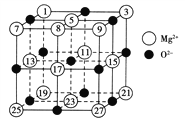
(3)Mg是第三周期元素,该周期部分元素氟化物的熔点见下表:
氟化物 | NaF | MgF2 | SiF4 |
熔点/K | 1 266 | 1 534 | 183 |
解释表中氟化物熔点差异的原因:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用如图所示装置来制取氯气,该装置由A、B、C三个基本装置组合而成,请回答下列问题:
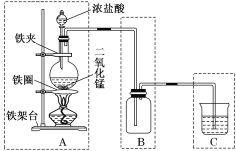
(1)说出A、B、C三个基本装置的名称:A是________装置,B是________装置,C是________装置。
(2)C装置中烧杯内所装液体是________溶液。
(3)写出A装置中反应的化学方程式_____________________________。
(4)氯气工业制法的原理为:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。
此反应的氧化剂是________,________元素的化合价升高;还原剂是_________,而________元素的化合价降低。该反应中4mol氧化剂能得到(失去)________mol电子。标准状况下,反应中产生了5.6L的氢气时,被氧化的物质的质量为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色溶液中,下列离子能大量共存的是
A.Na+、NH4+ 、NO3-、MnO4-B.K +、 SO42-、Cl-、Mg2+
C.K +、 H+ 、 HCO3-、Br-D.Ba2+ 、Na+ 、OH-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室制取氯气时,下列操作不正确的是________(填字母)。


A.装置Ⅰ可用于制取少量氯气
B.用装置Ⅱ除去氯气中的少量氯化氢
C.用装置Ⅲ制取氯气
D.用装置Ⅳ干燥氯气
(2)实验室制取干燥、纯净的氯气,除了二氧化锰、浓盐酸外还需要的试剂是____________、____________、____________。
(3)已知高锰酸钾与浓盐酸在常温下反应能产生氯气。
若用如下图所示的实验装置来制备纯净、干燥的氯气及验证它与金属的反应。每个虚线框表示一个单元装置,其中有错误的是________(填字母)。
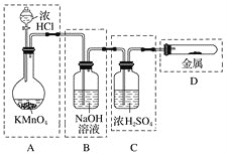
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若ABn分子的中心原子上没有孤对电子,应用价层电子对互斥模型理论,判断下列说法正确的是
A. n=3时,则分子的立体构型为V形
B. n=2时,则分子的立体构型平面三角形
C. n=4时,则分子的立体构型为正四面体形
D. n=4时,则分子的立体构型为三角锥形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F都是元素周期表前四周期的元素,它们的核电荷数:B<A<C<D<E<F。B、C两种元素都能引起水体富营养化。E原子得到一个电子后3p轨道全充满。A+比E原子形成的离子少1个电子层。D可以形成两种氧化物,其中一种氧化物是形成酸雨的主要气体之一。F的原子序数为26。请回答下列问题:
(1)C、D、E的第一电离能由小到大的顺序为________(用元素符号表示)。
(2)写出B的氢化物与水反应的离子方程式:________________,B的氢化物极易溶于水的原因是____________________________________________________________。
(3)化合物BE3的分子空间构型为________________。
(4)F元素原子的核外电子排布式为________。F的一种常见化合物F(CO)5在常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,则F(CO)5的晶体类型为__________________。
(5)将FE3的饱和溶液滴入沸水中,请写出有关反应的离子方程式:___________________________。
(6)比较B、C两种元素的氢化物稳定性并说明理由:____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com