
【题目】下列反应中,既属于氧化还原反应又属于吸热反应的是
A. Ba(OH)2· 8H2O 晶体与 NH4Cl 固体反应 B. 锌与硫酸反应制取氢气
C. 高温条件下碳粉与二氧化碳的反应 D. 高温煅烧石灰石
科目:高中化学 来源: 题型:
【题目】下列说法正确的( )
A. 含有共价键的化合物一定是共价化合物 B. 分子中只有共价键的化合物一定是共价化合物 C. 离子化合物中只能含离子键 D. 只有非金属原子间才能形成共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.4gNaOH 和 1.06g Na2CO3混合并配成溶液, 向溶液中滴加 0.1mol·L-1稀盐酸。 下列图像能正确表示加入盐酸的体积和生成 CO2的物质的量的关系的是( )
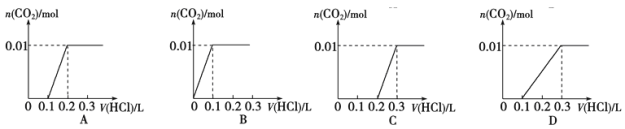
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白(填写序号不得分)

(1)在最高价氧化物的水化物中,酸性最强的化合物的化学式是________;
(2)比较①与⑤的最高价氧化物对应的水化物,酸性强的是________(填化学式):能通过________(写反应的化学方程式)说明。
(3)实验室制取②的氢化物的化学方程式________
(4)②可以形成多种氧化物,其中一种是红棕色气体,试用方程式说明该气体不宜采用排水法收集的原因________(用化学方程式表示)
(5)比较③与⑥的氢化物,更稳定________(填化学式)
(6)③④两元素组成的化合物A2B2型电子式为:________;存在的化学键是________;写出A2B2与水反应的化学方程式______________。
(7)⑨的单质与水反应所得离子化合物中阳离子半径_______S2-(填“>”或“<”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,A与B反应可生成C和D,其能量变化如图:

(1)下列有关反应A+BC+D的说法正确的是_______(填字母)。
A.反应前后原子的种类和数目一定不变
B.该反应若有热量变化,则一定是氧化还原反应
C.若该反应为放热反应,则不需要加热反应就一定能自发进行
D.反应物的总质量及总能量与生成物的总质量、总能量均相等
(2)若E1<E2,则反应热ΔH_______0(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列化学用语:
(1)书写电离方程式:KClO3:_____;H2SO4:_____
(2)某金属氯化物 MCl2 40.5g 中含有 0.6mol Cl,则 MCl 2 的摩尔质量为_____
(3)工业上用电解饱和食盐水制 Cl2,写出该反应的化学方程式:_____
(4)工厂里常用浓氨水来检验氯气管道是否泄漏,其原理为:8NH3+3Cl2=6NH4Cl+N2,请用双线桥表示其电子转移的方向和数目_____
(5)相同温度和体积的 A 和 B 两容器,A 容器中充满 O2,B 容器中充满 O3,若密度相同,则氧气和臭氧的物质的量之比为:_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g)![]() C(g)+D(g) 过程中的能量变化如图所示,回答下列问题
C(g)+D(g) 过程中的能量变化如图所示,回答下列问题

(1)该反应是________反应(填“吸热”“放热”);
(2)反应体系中加入催化剂对反应热是否有影响?__________
(3)在反应体系中加入催化剂,反应速率增大,E1的变化是:E1_________(填“增大”“减小”“不变”)
(4)由氢气和氧气反应生成1mol水蒸气放热241.8kJ·mol-1,写出其热化学方程式:____________。
(5)氢氧燃料电池是常见的燃料电池,在电解质溶液是KOH溶液的负极反应为__________。
(6)反应3Fe(s)+4H2O(g)![]() Fe3O4+4H2(g),在一可变的容积的密闭容器中进行,
Fe3O4+4H2(g),在一可变的容积的密闭容器中进行,
①增加Fe的量, 其正反应速率的变化是_______(填增大、不变、减小,以下相同)
②保持体积不变,充入N2使体系压强增大,其正反应速率_______
③保持压强不变,充入N2使容器的体积增大,逆反应速率_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com