
【题目】抗酸药的药理作用是
A.促进腹泻B.中和过多胃酸
C.抑制胃酸分泌D.促进血液循环
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:
【题目】节日期间因燃放鞭炮会引起空气中SO2含量增高.造成大气污染。某实验小组同学欲探究SO2的性质,并测定空气中SO2的含量
(1)他们设计如下实验装置,请你参与探究并回答问题
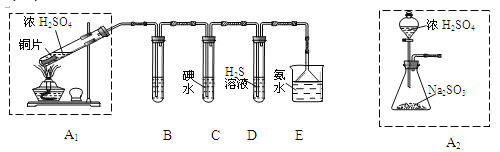
①装置A1中发生反应的化学方程式为________________________。
②装置B用于检验SO2的漂白性,其中所盛试剂为_________,装置D中实验现象为_______________。
③装置C中反应的离子方程式为___________________________________。
④为了实现绿色环保的目标。 甲同学欲用装置A2代替装置A1,你认为装置A2的优点是(写两点)________________________________________________________________。
(2)他们拟用以下方法测定空气中SO2含量(假设空气中无其他还原性气体)
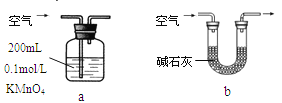
你认为哪个装置可行(填序号)__________,使用你所选用的装置测定SO2含量时,还需要测定的物理量是______________________________;不可行的请说明理由___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、为三种常见的单质,其中A、C为气体,B为常见金属.A溶于水可使石蕊试液先变红后褪色.F的水溶液为浅绿色溶液,它们的关系如图1:
(1)写出A、B、D的化学式:A.____________B.____________D.____________
(2)写出反应①②的离子方程式:①____________;②____________.
(3)A溶于水使石蕊试液先变红后褪色的原因是:____________.
(4)检验D的水溶液中的阳离子的方法是(指出药品、试剂、步骤和现象):_____.将D溶液逐滴加入的沸水中会产生一种红褐色的液体.你认为该液体中的分散质粒子直径在____________之间,验证的简单方法是:____________。
(5)某同学将A的饱和溶液装满大试管倒置在烧杯中如图2,光照一段时间后,发现试管底部有无色的气体产生,溶液的颜色也变成无色,请你帮他对产生的气体进行探究:
①你预测气体可能是____________ 。
②针对你的预测写出验证实验方案(步骤和现象):___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用废铜合金(含少量铁和铝)来制取硫酸铜晶体(CuSO4·5H2O),方案如下:

金属离子生成氢氧化物沉淀的pH可参考下列数据:
Fe3+ | Fe2+ | Cu2+ | Al3+ | |
开始沉淀时的pH | 2.2 | 7.5 | 5.2 | 3.7 |
完全沉淀时的pH | 3.2 | 9.0 | 6.7 | 4.7 |
请回答:
(1)若溶解合金时加入的混酸由2 L 3 mol·L-1硫酸和1 L 2 mol·L-1硝酸混合而成,则反应后生成标准状况下的NO的体积最多为____________L。
(2)加入H2O2的目的是____________。
(3)为保证产品的纯度,M物质最好选用________(填字母),调节pH的范围为____________。
a.Cu(OH)2 b.H2SO4 c.NH3·H2O d.Na2CO3
(4)滤液D中加入硫酸的目的为_______________________________________。
(5)从溶液E制得CuSO4·5H2O晶体所需要的步骤为________、结晶、过滤和干燥。
(6)0.80g CuSO4·5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示。试确定200℃时固体物质的化学式______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H4)是火箭燃料,常温下为液体,其分子的球棍模型如下图所示。肼能与双氧水发生反应:N2H4+ 2H2O2=== N2+ 4H2O。下列说法正确的是()

A. 标准状况下,3.2 g N2H4的体积是2.24L
B. 标准状况下,11.2 L N2中含电子总数约为7×6.02×1023
C. 标准状况下,22.4 L H2O2中所含原子总数约为4×6.02×1023
D. 若生成3.6 g H2O,则上述反应转移电子的数目约为2×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,既属于氧化还原反应又属于吸热反应的是
A. Ba(OH)2· 8H2O 晶体与 NH4Cl 固体反应 B. 锌与硫酸反应制取氢气
C. 高温条件下碳粉与二氧化碳的反应 D. 高温煅烧石灰石
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于乙烯的化学性质的叙述中,不正确的是 ( )
A. 能使溴水褪色
B. 能使酸性高锰酸钾褪色
C. 能与HCl发生加成反应
D. 不能发生加成聚合反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用海水晒盐后的母液进行提溴,其流程如下

己知:①3Br2+3H2O![]() 5HBr+HBrO3
5HBr+HBrO3
②已知液溴沸点为59℃,CCl4和苯的沸点分别为77℃和80℃。
(1)写出反应Ⅰ的化学方程式_________________________________________。
(2)试剂Ⅰ为__________,并书写反应Ⅱ的离子方程式_____________________________。
(3)操作Ⅰ为__________。
(4)工业上得到的单质Br2中往往还含有少量Cl2,加__________(填试剂)除去氯气,并用__________(填方法)进行分离提纯。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com