
����Ŀ��ʵ�������÷�ͭ�Ͻ�(������������)����ȡ����ͭ����(CuSO4��5H2O)���������£�

�������������������������pH�ɲο��������ݣ�
Fe3�� | Fe2�� | Cu2�� | Al3�� | |
��ʼ����ʱ��pH | 2.2 | 7.5 | 5.2 | 3.7 |
��ȫ����ʱ��pH | 3.2 | 9.0 | 6.7 | 4.7 |
��ش�
��1�����ܽ�Ͻ�ʱ����Ļ�����2 L 3 mol��L��1�����1 L 2 mol��L��1�����϶��ɣ���Ӧ�����ɱ�״���µ�NO��������Ϊ____________L��
��2������H2O2��Ŀ����____________��
��3��Ϊ��֤��Ʒ�Ĵ��ȣ�M�������ѡ��________(����ĸ)������pH�ķ�ΧΪ____________��
a��Cu(OH)2��b��H2SO4��c��NH3��H2O��d��Na2CO3
��4����ҺD�м��������Ŀ��Ϊ_______________________________________��
��5������ҺE�Ƶ�CuSO4��5H2O��������Ҫ�IJ���Ϊ________���ᾧ�����˺��
��6��0.80g CuSO4��5H2O��Ʒ������ˮ���̵��������ߣ���Ʒ�������¶ȱ仯�����ߣ���ͼ��ʾ����ȷ��200��ʱ�������ʵĻ�ѧʽ______________��

���𰸡� 44.8L ��Fe2+������Fe3+ a 4.7��PH��5.2 ����Cu2+��ˮ�� �������� CuSO4��H2O
���������������̣���ʼ����������������ҺA�к���Cu2+��Fe2+��Al3+����ҺA�м�H2O2����Fe2+����ΪFe3+����ֹ����ʱӰ��Cu2+�����������Һ������M����pH��ȥFe3+��Al3+����ҺD����һϵ�в����õ�����ͭ������
��1�������⣬n(H+)=2L��3mol��L-1��2+1L��2mol��L-1=14 mol��n��NO3-��=1L��2mol��L-1=2 mol�����ݷ���ʽ3Cu+2NO3-+8H+=3Cu2++2NO��+4H2O�ɵã������ӹ�����NO3-��ȫ��Ӧ����������ɱ�״����NO�����Ϊ2 mol��22.4Lmol-1=44.8L��
��2��������������������H2O2��Ŀ���ǽ�Fe2+����ΪFe3+��
��3�����������Һ������M����pH��ȥFe3+��Al3+��Ϊ�˲����������ʣ�M���ѡ��a.Cu(OH)2�����ݽ������������������������pH���ݿɵ���ҪʹFe3+��Al3+��ȫ��������Cu2+������������pH�ķ�ΧΪ��4.7��pH<5.2��
��4����ΪCu2+���������ӣ�����ֱ�Ӽ�����ҺD��ٽ���ˮ�⣬�ʼ�����������Cu2+ˮ�⡣
��5��������ͭ��Һ�Ƶ�CuSO45H2O���壬��Ϊ���庬�нᾧˮ��������Ҫ����������������Ũ��������ȴ�ᾧ�����ˡ�ϴ�ӡ�����Ȳ��衣
��6��CuSO45H2O���ȵ�102��ʱ��ʼ��ʧˮ��113��ʱ�ɵõ����ȶ����м�����258��ʱ�����ֽ⣬����200��ʱʧȥ��ˮ������Ϊ0.80g-0.57g=0.23g�����ݷ�Ӧ�Ļ�ѧ����ʽ��CuSO45H2O![]() CuSO4��5-x��H2O+xH2O���ɵã�
CuSO4��5-x��H2O+xH2O���ɵã�
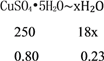
�б���ʽ�ɽ��x��4����200��ʱ�������ʵĻ�ѧʽΪCuSO4H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڲ�ͬ�����£��ֱ��÷�Ӧ2SO2��g����O2��g��2SO3��g�����������£����л�ѧ��Ӧ����������(����)
A. v(SO2)��4 mol��L��1��min��1 B. v(O2)��2 mol��L��1��min��1
C. v(SO3)��6 mol��L��1��min��1 D. v(O2)��1 mol��L��1��min��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
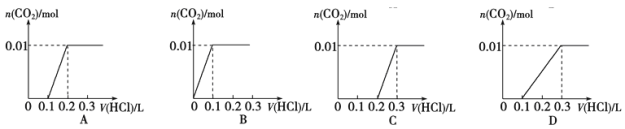
����Ŀ����0.4gNaOH �� 1.06g Na2CO3��ϲ������Һ�� ����Һ�еμ� 0.1mol��L-1ϡ���ᡣ ����ͼ������ȷ��ʾ������������������ CO2�����ʵ����Ĺ�ϵ���ǣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�У���100mL 0.6mol/L NaCl��Һ������Cl�����ʵ���Ũ����ͬ���ǣ����»����Һ����������ƿ�������Һ���֮�ͣ� �� ��
A. 50mL 0.6mol/L MgCl2��Һ
B. 200mL 0.3mol/L AlCl3��Һ��100mL 0.2mol/L AgNO3��Һ�ĵĻ����Һ
C. 70ml 1mol/L NaCl��Һ��100ml 1mol/L KCl��Һ�Ļ����Һ
D. 25ml 0.6mol/L HCl��Һ ��50mL 0.3mol/L MgCl2��Һ�Ļ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣���Ա��еĢ١�����Ԫ�أ���д���пհ�(��д��Ų��÷�)

��1��������������ˮ�����У�������ǿ�Ļ�����Ļ�ѧʽ��________��
��2���ȽϢ���ݵ�����������Ӧ��ˮ�������ǿ����________���ѧʽ������ͨ��________��д��Ӧ�Ļ�ѧ����ʽ��˵����
��3��ʵ������ȡ�ڵ��⻯��Ļ�ѧ����ʽ________
��4���ڿ����γɶ������������һ���Ǻ���ɫ���壬���÷���ʽ˵�������岻�˲�����ˮ���ռ���ԭ��________���û�ѧ����ʽ��ʾ��
��5���ȽϢ�����⻯����ȶ�________���ѧʽ��
��6���ۢ���Ԫ����ɵĻ�����A2B2�͵���ʽΪ��________�����ڵĻ�ѧ����________��д��A2B2��ˮ��Ӧ�Ļ�ѧ����ʽ______________��
��7����ĵ�����ˮ��Ӧ�������ӻ������������Ӱ뾶_______S2-���>������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʵ��������и������У�����ԭ�Ӹ��������� �� ��
A. HF B. H2O C. N2 D. CH4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Se�����仯�����ڹ�ũҵ��������������;����ͭ�����ࣨ��Ҫ�ɷ�ΪAg2Se��Cu2Se�������𡢲��ȣ�Ϊԭ���Ʊ������Ĺ���������ͼ��ʾ��

�ش��������⣺
��1����������ʱ������Ũ�����Ϊ_____�����ţ���
A��Ũ���� B�� 20������ C��50������ D�� 80%����
��2����������������Cu2Se���뷴Ӧʱ���÷�Ӧ������������_______��
��3����ˮ��������������Ӧ�Ļ�ѧ����ʽΪ____________��
��4�������������ô����ɲ����������ķ��������ᴿ����ô������������Ļӷ��������������¶ȵĹ�ϵ��ͼ��ʾ��

��������п��Ƶ�����¶���_____�����ţ���
A��455�� B��462�� C��475�� D��515��
��5����ˮ�������е�¯������飬�Ҽ�����ˮ���н��ݣ�Ŀ����____________________�����������к��еĽ���������___________��
��6����������Һ���У�c(Ag+)=3.0��10-2 mol/L������Һ��c(SO42-)���Ϊ___________________����֪��Ksp(Ag2SO4)=1.4��10-5������������2λ��Ч���֣���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com