
 氮及其化合物在工业生产和国防建设中有广泛应用.回答下列问题:
氮及其化合物在工业生产和国防建设中有广泛应用.回答下列问题: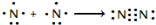 .
.| 化学键 | N-H | N-N | N=N | N≡N | O=O | O-H |
| 键能(kJ/mol) | 390.8 | 193 | 418 | 946 | 497.3 | 462.8 |
分析 (1)两个氮原子形成一个氮气分子;
(2)根据肼燃烧的方程式N2H4 (g)+O2(g)=N2(g)+2H2O(g),结合化学反应的实质是旧键的断裂、新键的形成来分析反应吸收和放出的热量,而△H=吸收的热量-放出的热量,然后根据H2O(l)=H2O(g)△H=+44kJ/mol来分析;
(3)KCN可用于溶解难溶金属卤化物.将AgI溶于KCN溶液中,形成稳定的Ag(CN)2-和I-,据此写出离子方程式;而此反应的平衡常数表达式为K=$\frac{c(Ag(CN{)_{2}}^{-})•c({I}^{-})}{c(C{N}^{-})^{2}}$,然后根据Ksp(AgI)=1.5×10-16,K稳[Ag(CN)2-]=1.0×1021来分析.
(4)氨的催化氧化用于工业生产硝酸.在此反应中,氨气被氧化为NO在负极放电,结合环境为碱性分析;
(5)①反应是放热反应,在绝热恒容容器中,反应进行热量升高,反应速率增大;
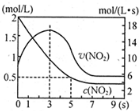
②分析图象5s二氧化氮变化浓度=2mol/L-0.5mol/L=1.5mol/L,结合转化率概念计算=$\frac{消耗量}{起始量}$×100%.
解答 解:(1)两个氮原子形成一个氮气分子,故用电子式表示氮气的形成过程为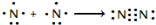 ,故答案为:
,故答案为: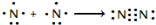 ;
;
(2)肼的燃烧反应为:N2H4 (g)+O2(g)=N2(g)+2H2O(g)
吸收能量:(4×390.8+193)KJ 497.3KJ 吸收热量:946KJ 462.8×4KJ
故△H=(4×390.8+193)KJ/mol+497.3KJ/mol-946KJ/mol-462.8×4KJ/mol=-543.7KJ/mol,故可知热化学方程式为:
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-543.7KJ/mol ①
而H2O(l)=H2O(g)△H=+44kJ/mol ②
将①-②×2可知:N2H4 (g)+O2(g)=N2(g)+2H2O(l)△H=-631.7kJ/mol 故答案为:N2H4 (g)+O2(g)=N2(g)+2H2O(l)△H=-631.7kJ/mol;
(3)KCN可用于溶解难溶金属卤化物.将AgI溶于KCN溶液中,形成稳定的Ag(CN)2-和I-,据此写出离子方程式为:AgI(s)+2CN-(aq)?Ag(CN)2-(aq)+I-(aq);
而此反应的平衡常数表达式为K=$\frac{c(Ag(CN{)_{2}}^{-})•c({I}^{-})}{c(C{N}^{-})^{2}}$,
而Ksp(AgI)=1.5×10-16=c(Ag+)•c(I-) ①
K稳[Ag(CN)2-]=1.0×1021=$\frac{c(A{g}^{+})•{c}^{2}(C{N}^{-})}{c(Ag(CN{)_{2}}^{-})}$ ②
将$\frac{①}{②}$可得此反应的平衡常数,故K=$\frac{c(Ag(CN{)_{2}}^{-})•c({I}^{-})}{c(C{N}^{-})^{2}}$=$\frac{Ksp(AgI)}{{K}_{稳}[Ag(CN{)_{2}}^{-}]}$=$\frac{1.5×1{0}^{-16}}{1.0×1{0}^{21}}$=1.5×10-37,故答案为:AgI(s)+2CN-(aq)?Ag(CN)2-(aq)+I-(aq);1.5×10-37;
(4)氨的催化氧化用于工业生产硝酸.在此反应中,氨气被氧化为NO在负极放电,结合环境为碱性可知电极反应为:NH3-5e-+5OH-=NO+4H2O,故答案为:NH3-5e-+5OH-=NO+4H2O;
(5)①反应是放热反应,在绝热恒容容器中,反应进行热量升高,反应速率增大,随反应进行二氧化氮浓度减小,反应为达到平衡,0-3s时v(NO2)增大是由于体系温度升高,故答案为:容器为绝热体系,该反应正向进行放热,体系温度升高,v(NO2)增大;
②分析图象5s二氧化氮变化浓度=2mol/L-0.5mol/L=1.5mol/L,结合转化率概念计算=$\frac{消耗量}{起始量}$×100%=$\frac{1.5mol/L}{2mol/L}$×100%=75%,故答案为:75%.
点评 本题考查了图象分析判断,反应速率、转化率概念计算分析,平衡常数的计算,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 20 g D2O所含的电子数为10 NA | |
| B. | 6.0gSiO2晶体中含有0.2NA个Si-O键 | |
| C. | 氢气与氯气反应生成标准状况下22.4 L氯化氢,断裂化学键总数为2 NA | |
| D. | 苯与液溴反应生成1mol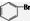 时消耗0.5NA个Br2 时消耗0.5NA个Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
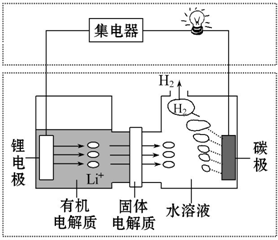
| A. | 碳极发生的反应:2H2O+2e-═H2↑+2OH- | |
| B. | 有机电解质和水溶液不可以互换区域 | |
| C. | 理论上外电路中每转移1 mol电子,负极消耗的质量为7 g | |
| D. | 若该电池可以充电,充电时碳极接外加电源的负极,锂极接外加电源的正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作 | 实验现象 | 结论 |
| A | 向NaBr溶液中加入氯水,再加入淀粉KI溶液 | 溶液变蓝 | 氧化性:Cl2>Br2>I2 |
| B | 将铝片放入盐酸中 | 产生气泡的速率开始较慢,随后加快,后来又逐渐减慢 | H+的浓度是影响反应速率的唯一因素 |
| C | 向蔗糖溶液中加入稀硫酸,水浴加热后,加入新制氢氧化铜悬浊液,加热 | 得到蓝色溶液 | 蔗糖水解产物没有还原性 或蔗糖未水解 |
| D | 向漂白粉中滴入稀硫酸,将生成的气体通入品红溶液 | 品红溶液褪色 | 气体中含有Cl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.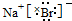 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol•L-1的氯化铁溶液中,若Fe3+的数目为 NA,则Cl-的数目为3NA | |
| B. | 常温下,1 mol Fe与足量稀HNO3反应,转移电子的数目为2 NA | |
| C. | 8.0gCu2S和CuO的混合物中含有的铜原子数为0.1NA | |
| D. | 标准状况下,2.24 LCl2溶于水,转移电子的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
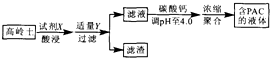 采用高岭土(主要成分为A12 O3、SiO2和Fe2O3)为原料制备水质净化剂PAC{[A12(OH)nC16-n]m(n<6,m为聚合度)}的过程如图.下列说法正确的是( )
采用高岭土(主要成分为A12 O3、SiO2和Fe2O3)为原料制备水质净化剂PAC{[A12(OH)nC16-n]m(n<6,m为聚合度)}的过程如图.下列说法正确的是( )| A. | 试剂X为H2SO4 | B. | 滤渣主要成分为Fe(OH)3、H2 SiO3 | ||
| C. | 调pH过高或过低均会减少PAC生成 | D. | 滤液浓缩聚合过程发生了加聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
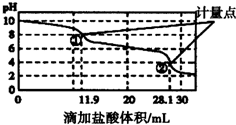
| A. | 此样品n(NaHCO3)=(28.1-11.9)×10-4mol | |
| B. | 计量点②溶液中大量存在的阴离子是Cl- | |
| C. | 计量点①-②之间发生反应的离子方程式为HCO3-+H+═H2O+CO2↑ | |
| D. | 使用该方法测定Na2CO3和NaOH混合溶液中的NaOH含量,将会得到1个计量点 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com