
 ,分子较小的单体含氧官能团名称是羟基.
,分子较小的单体含氧官能团名称是羟基.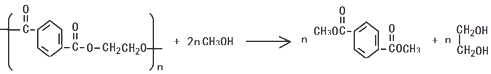 .
. )的原料.
)的原料.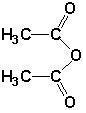 )反应生成阿司匹林的化学方程式:
)反应生成阿司匹林的化学方程式: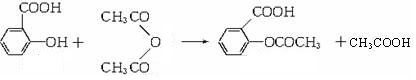 .
. ,该同分异构体符合以下条件:
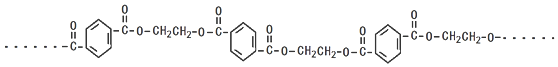
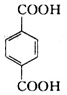
,该同分异构体符合以下条件:分析 (1)①根据高分子化合物结构特点知,形成该高分子化合物需要的单体是 和HOCH2CH2OH,分子量较小的是乙二醇;
和HOCH2CH2OH,分子量较小的是乙二醇;
②PET塑料有多种降解途径,其中常用的甲醇法是在一定条件下将其与过量的甲醇作用,降解为两种小分子,两种小分子分别是对二苯甲酸二甲酯、乙二醇;
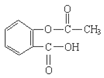
(2)①水杨酸和乙酸酐发生取代反应生成阿司匹林和乙酸;
②阿司匹林同分异构体符合下列条件:
a.芳香族化合物,说明含有苯环;
b.与氢氧化钠溶液共热,完全反应将消耗四倍物质的量的氢氧化钠,说明水解生成物中含有两个酚羟基、两个羧基;
c.苯环上氢原子被一个溴原子取代,可能的产物有两种,说明苯环上有两种氢原子.
解答 解:(1)①根据高分子化合物结构特点知,形成该高分子化合物需要的单体是 和HOCH2CH2OH,相对分子质量较大的是
和HOCH2CH2OH,相对分子质量较大的是 ,分子量较小的是乙二醇,乙二醇中官能团是羟基,
,分子量较小的是乙二醇,乙二醇中官能团是羟基,
故答案为: ;羟基;
;羟基;
②PET塑料有多种降解途径,其中常用的甲醇法是在一定条件下将其与过量的甲醇作用,降解为两种小分子,两种小分子分别是对二苯甲酸二甲酯、乙二醇,该反应方程式为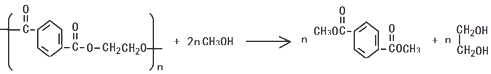 ,
,
故答案为: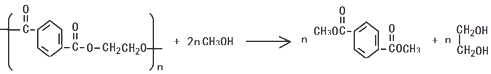 ;
;
(2)①水杨酸和乙酸酐发生取代反应生成阿司匹林和乙酸,反应方程式为 ,
,
故答案为: ;
;
②阿司匹林同分异构体符合下列条件:
a.芳香族化合物,说明含有苯环;
b.与氢氧化钠溶液共热,完全反应将消耗四倍物质的量的氢氧化钠,说明水解生成物中含有两个酚羟基、两个羧基;
c.苯环上氢原子被一个溴原子取代,可能的产物有两种,说明苯环上有两种氢原子,
则符合条件的结构简式为 ,
,
故答案为: .
.
点评 本题考查有机物合成,为高频考点,侧重考查学生分析判断能力,明确物质转化中断键和成键方式是解本题关键,难点是判断同分异构体结构简式确定,题目难度中等.


 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案科目:高中化学 来源: 题型:解答题
| 时间/min | CO | H2O(g) | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
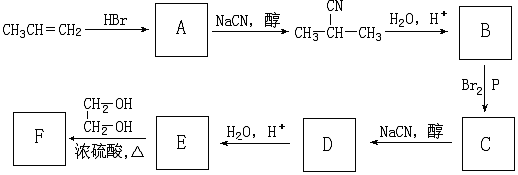
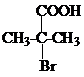 +NaCN$\stackrel{醇}{→}$NaBr+
+NaCN$\stackrel{醇}{→}$NaBr+ ,E→F(F为高分子时)nHOOC-C(CH3)2-COOH+nHOCH2CH2OH$→_{△}^{浓硫酸}$
,E→F(F为高分子时)nHOOC-C(CH3)2-COOH+nHOCH2CH2OH$→_{△}^{浓硫酸}$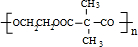 +2nH2O.
+2nH2O.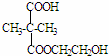 ,②分子内含有一个七元环
,②分子内含有一个七元环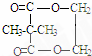 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作和现象 | 结论或目的 | |
| A | 向纯碱中滴加足量浓盐酸,将所得气体通入硅酸钠溶液中,溶液变浑浊 | 酸性:盐酸>碳酸>苯酚 |
| B | 取某溶液少量,加入盐酸酸化的氯化钡溶液,出现白色沉淀 | 该溶液中一定含有大量的SO42- |
| C | 取少量Fe(NO3)2试样加水溶液后加稀硫酸酸化,滴加KSCN溶液,溶液变为红色 | 该Fe(NO3)2试样已经变质 |
| D | 处理锅炉水垢中的CaSO4时,依次加入饱和Na2CO3溶液和盐酸,水垢溶解 | 目的:将不溶于酸的沉淀转化为易溶于酸的沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 化学用语 | 推论 |
| A | ${\;}_{92}^{238}$U3+ | 该铀离子核外有89个电子 |
| B | 2H2(g)+O2(g)═2H2O(g);△H=-483.6kJ•mol | 1mol氢气完全燃烧放出热量483.6kJ. |
| C | 2NaCl+2H2O $\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑ | NaCl氧化性比Cl2强 |
| D | FeO+4H++NO3-═Fe3++NO2↑+2H2O | 氧化亚铁溶于稀硝酸的离子方程式 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12g由${\;}_{6}^{12}$C60和${\;}_{6}^{14}$C60组成的固体中的原子数为NA | |
| B. | 4.4g由CO2和N2O组成的混合气体中的电子数为2.2NA | |
| C. | 常温常压下22.4LNH3中所含的共价键数为3NA | |
| D. | 1L1mol•L-1次氯酸溶液中的ClO-数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | 25℃~550℃~600℃~700℃ |
| 主要成分 | WO3 W2O5 WO2 W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 性质 | 实际应用 |
| A | MgO熔点高 | 可用作耐火材料 |
| B | KMnO4具有强氧化性 | 可用于漂白织物 |
| C | 常温下,铁能被浓硫酸钝化 | 常温下,可用铁质器皿盛放浓硫酸 |
| D | TiCl4在水中能发生水解 | 可用TiCl4溶液制备TiO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com