
【题目】下列热化学方程式中,正确的是
A.甲烷的燃烧热△H = -890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g) + 2O2(g)═ CO2(g) + 2H2O(g) △H = -890.3kJ/mol
B.一定条件下,将0.5mol N2和1.5m01H2置于密闭容器中充分反应生成NH3放热19.3kJ其热化学方程式为:N2(g) + 3H2(g)![]() 2NH3(g) △H =-38.6kJ/mol
2NH3(g) △H =-38.6kJ/mol
C.在l01kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g) + O2(g)═2H2O(l) △H =-571.6kJ/mol
D.HCl和NaOH反应的中和热△H = -57.3kJ/mol,则H2SO4和Ca(OH)2反应的反应热△H = 2×(-57.3)kJ/mol
【答案】C
【解析】
A、燃烧热是生成液态水放出的能量,选项A错误;
B、N2(g)+3H2(g)2NH3(g)反应可逆,0.5 mol N2和1.5 molH2置于密闭容器中充分反应,生成NH3的物质的量小于1mol,N2(g)+3H2(g)2NH3(g)△H<﹣38.6 kJ/mol,选项B错误;
C、1mol H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=﹣571.6 kJ/mol,选项C正确;
D、H2SO4和Ca(OH)2反应生成硫酸钙沉淀,不仅仅生成水,放出更多的热量,则H2SO4和Ca(OH)2反应的中和热△H<2×(-57.3)kJ/mol,故D错误;
答案选C。


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】某柔性屏手机的柔性电池以碳纳米管做电极材料,以吸收![]() 溶液的有机高聚物做固态电解质,其电池结构如图所示。电池总反应为:
溶液的有机高聚物做固态电解质,其电池结构如图所示。电池总反应为:
![]()
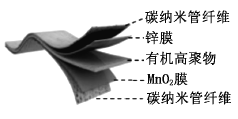
下列说法中,正确的是( )
A.充电时,![]() 移向Zn膜
移向Zn膜
B.充电时,含有![]() 膜的碳纳米管纤维一端连接有机高聚物电源负极
膜的碳纳米管纤维一端连接有机高聚物电源负极
C.放电时,电子由锌膜表面经有机高聚物至![]() 膜表面
膜表面
D.放电时,电池的负极反应为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用一定浓度的盐酸滴定某浓度的氨水。滴定终点附近溶液的pH和导电能力的变化如图所示(利用溶液导电能力的变化可判断滴定终点,溶液总体积变化忽略不计)。下列说法错误的是( )

A.a点对应的溶液中:![]()
B.a→b过程中,![]() 不断增大
不断增大
C.c→d溶液导电性增强的主要原因是![]() 和
和![]() 增大
增大
D.根据溶液pH和导电能力的变化可判断:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气相条件下,立方烷能自发地发生热重排反应生成一系列化合物。下列说法正确的是
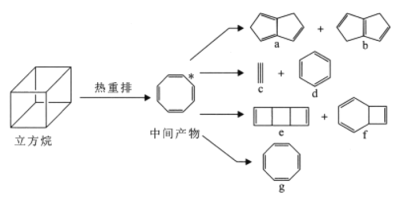
A.a、f中所有原子均可处于同一平面
B.1mol化合物e完全燃烧消耗12molO2
C.六硝基立方烷最多有3种结构(不考虑立体异构)
D.立方烷热重排产物均能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】他米巴罗汀是一种对白血病、阿尔茨海默症等疾病具有较好治疗效果的药物,其一种合成路线:
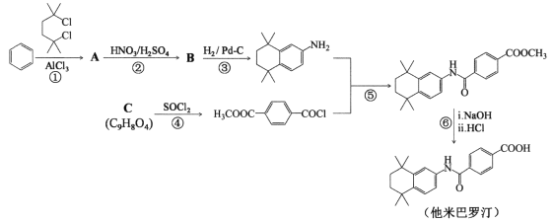
回答下列问题:
(1)A的结构简式是_________,C中含氧官能团的名称是_________
(2)①和③的反应类型分别是_________
(3)下列说法正确的是_________(填标号)。
a.A为苯的同系物b.B的一氯代物有5种
c.1molC最多可与2molNaOH反应d.弱碱性条件有利于反应⑤进行
(4)草酰氯![]() 与乙二胺(
与乙二胺(![]() )反应可得到一种六元环状化合物,该反应的化学方程式为_________
)反应可得到一种六元环状化合物,该反应的化学方程式为_________
(5)化合物W与C互为同分异构体,且满足下列条件:①属于芳香族化合物且能与NaHCO3反应:②能发生银镜反应;③酸性条件下可发生水解反应,其产物能之一与FeCl3发生显色反应,则W共有_________种,其中一种核磁共振氢谱为1:2:2:2:1,其结构简式为__________。
(6)参照上述合成路线,设计由苯和1,3-丁二烯合成![]() 的路线(其它无机试剂任选)。__________
的路线(其它无机试剂任选)。__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钠(Na2FeO4)是具有紫色光泽的粉末,是一种高效绿色强氧化剂,碱性条件下稳定,可用于废水和生活用水的处理。实验室以石墨和铁钉为电极,以不同浓度的NaOH溶液为电解质溶液,控制一定电压电解制备高铁酸钠,电解装置和现象如下:
c(NaOH) | 阴极现象 | 阳极现象 |
1 mol·L-1 | 产生无色气体 | 产生无色气体,10min内溶液颜色无明显变化 |
10 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,3min后溶液变为浅紫红色,随后逐渐加深 |
15 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,1min后溶液变为浅紫红色,随后逐渐加深 |
下列说法不正确的是

A. a为铁钉,b为石墨
B. 阴极主要发生反应:2H2O + 2e-=== H2↑+ 2OH-
C. 高浓度的NaOH溶液,有利于发生Fe-6e-+ 8OH-=== FeO42-+ 4H2O
D. 制备Na2FeO4时,若用饱和NaCl溶液,可有效避免阳极产生气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,可逆反应N2 +3H2![]() 2NH3 △H<0,达到平衡后,当单独改变下述条件时,有关叙述错误的是
2NH3 △H<0,达到平衡后,当单独改变下述条件时,有关叙述错误的是
A.加催化剂,υ正、υ逆都发生变化,且变化的倍数相等
B.加压,υ正、υ逆都增大,且υ正增大的倍数大于υ逆增大的倍数
C.降温,υ正、υ逆都减小,且υ正减小的倍数小于υ逆减小的倍数
D.增大氮气的浓度,υ正、υ逆都增大,且υ正增大倍数大于υ逆增大倍数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院科研团队研究发现,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理示意图如下。下列说法不正确的是( )
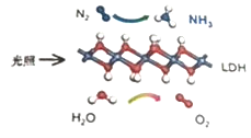
A.该过程将太阳能转化成为化学能
B.该过程中,只涉及到极性键的断裂与生成
C.氧化剂与还原剂的物质的量之比为1:3
D.原料气N2可通过分离液态空气获得
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴化钙可用作阻燃剂、制冷剂,具有易溶于水、易吸潮等性质。实验室用工业大理石(含少量Al3+、Fe3+等杂质)制备溴化钙的主要流程如下(已知步骤Ⅲ的滤液中不含![]() )。
)。
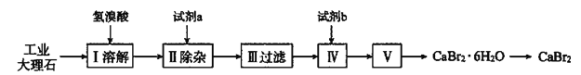
下列说法错误的是( )
A.试剂a可以是生石灰,试剂b是氢溴酸
B.步骤V所含的操作依次是蒸发浓缩、冷却结晶、过滤、洗涤、干燥
C.为将杂质离子除尽,步骤Ⅱ需加过量试剂a,保证溶液呈强碱性
D.工业上常用氨气与溴、石灰乳反应制取溴化钙,若反应中氧化剂与还原剂的物质的量比为3∶2,则产物中会生成一种无色气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com