
����Ŀ�������£���һԪ��HA����Һ��KOH��Һ�������ϣ���������仯����ʵ���������±���
ʵ���� | ��ʼŨ��/��mol��L��1�� | ��Ӧ����Һ��pH | |
c��HA�� | c(KOH) | ||
�� | 0.1 | 0.1 | 9 |
�� | x | 0.2 | 7 |
�����жϲ���ȷ����
A��ʵ������Ӧ�����Һ�У�c(K��)>c(A��)>c(OH��)>c(H��)
B��ʵ������Ӧ�����Һ�У�c(OH��)=c(K��)��c(A��)=![]() mol/L
mol/L
C��ʵ������Ӧ�����Һ�У�c(A��)��c(HA)>0.1mol��L��1
D��ʵ������Ӧ�����Һ�У�c(K��)=c(A��)>c(OH��) =c(H��)
���𰸡�B
��������
A�������ǵ������Ũ�Ȼ�ϣ�Ӧ��ǡ����ȫ��Ӧ��������KA����Ӧ����Һ�Լ��ԣ�˵��HA�����ᣬA������ˮ�⣬A����H2O![]() HA��OH��������Ũ�ȴ�С˳����c(K��)>c(A��)>c(OH��)>c(H��)����A˵����ȷ��B�����ݵ���غ㣬��c(K��)��c(H��)=c(OH��)��c(A��)������c(OH��)=c(K��)��c(H��)��c(A��)=Kw/10��9mol��L��1����B˵������C����ΪHA�����ᣬ��Ӧ����Һ�����ԣ�����ΪHA��KA�����HA��Ũ��Ӧ����0.2mol�����������غ㣬c(A��)��c(HA)>0.2/2mol��L��1=0.1mol��L��1����C˵����ȷ��D�����ݵ����ԣ�c(K��)��c(H��)=c(OH��)��c(A��)����Һ�����ԣ���c(H��)=c(OH��)��c(K��)=c(A��)������Ũ�ȴ�С˳����c(K��)=c(A��)> c(H��)=c(OH��)����D˵����ȷ��
HA��OH��������Ũ�ȴ�С˳����c(K��)>c(A��)>c(OH��)>c(H��)����A˵����ȷ��B�����ݵ���غ㣬��c(K��)��c(H��)=c(OH��)��c(A��)������c(OH��)=c(K��)��c(H��)��c(A��)=Kw/10��9mol��L��1����B˵������C����ΪHA�����ᣬ��Ӧ����Һ�����ԣ�����ΪHA��KA�����HA��Ũ��Ӧ����0.2mol�����������غ㣬c(A��)��c(HA)>0.2/2mol��L��1=0.1mol��L��1����C˵����ȷ��D�����ݵ����ԣ�c(K��)��c(H��)=c(OH��)��c(A��)����Һ�����ԣ���c(H��)=c(OH��)��c(K��)=c(A��)������Ũ�ȴ�С˳����c(K��)=c(A��)> c(H��)=c(OH��)����D˵����ȷ��


 �ִʾ��ƪϵ�д�
�ִʾ��ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ���������ͬ��������Һ����pH=3��CH3COOH��Һ ��pH=3������ ��pH=11�İ�ˮ ��pH=11��NaOH��Һ������˵������ȷ������ ��
A. ����������Һϡ��100����ϡ�ͺ���ҺpH��С˳��>��>��>��
B. ������Ģں͢ۻ������ǿ�������Σ���Ϻ���Һ������
C. ������Ģۺֱܷ͢��õ�Ũ�ȵ�������Һ�кͣ�����������Һ���������>��
D. ������Ģٺ͢ڷֱ���������п����Ӧ���ɵ�������ͬ��ͬѹ���������>��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��WΪԭ������������������ֶ���������Ԫ�أ�A��B��C��D��EΪ��������Ԫ���е����ֻ���������ɵĻ������֪A����Է�������Ϊ28��B�����к���18�����ӣ����ֻ�������ת����ϵ��ͼ��ʾ������˵��������ǣ� ��
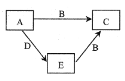
A. X��Y��ɻ�����ķе�һ����X��Z��ɻ�����ķе��
B. Y������������ˮ����Ϊ����
C. Y��Z��ɵķ��ӿ���Ϊ�Ǽ��Է���
D. W������������ԭ�Ӱ뾶��С��Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ҫ��������и�С�⣺
��.��1��������ϡ��ǿ�ᡢǿ�Ӧ����1mol H2O��l��ʱ�ų�57.3kJ��������д����ʾϡ�����ϡ����������Һ��Ӧ���к��ȵ��Ȼ�ѧ����ʽ________ ��
��2����֪���ұ��������Ʊ���ϩ��Ӧ�����ڼ������ʱ���˴��ɿ���Ϊ![]() ��
�� ![]()
![]()
![]() +H2��g��
+H2��g��
��ѧ�� | C��H | C��C | C=C | H��H |
����/kJ��mol��1 | 412 | 348 | 612 | 436 |
����������Ӧ����H��________ kJ��mol��1��
��.25 ��ʱ���������ʵĵ���ƽ�ⳣ�������ʾ����ش��������⣺
��ѧʽ | CH3COOH | H2CO3 | HClO |
����ƽ�ⳣ�� | 1.7��10��5 | K1��4.3��10��7 K2��5.6��10��11 | 3.0��10��8 |
��1��CH3COOH��H2CO3��HClO��������ǿ������˳��Ϊ_______��
��2��������CO2����ͨ��NaClO��Һ�У�д����Ӧ�����ӷ���ʽ��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��ʹCH3COONa��Һ��Na����Ũ����CH3COO����Ũ�ȱ�Ϊ1��1������CH3COONa��Һ�м���( )
������������ ��������NaCl �������Ĵ��� ��������CH3COONa
A���٢� B����
C���ۢ� D����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�г���ͼ��ֱ�۵�������ѧ��Ӧ�Ľ��̻���������ͼ��������ȷ����

A.����ͼ�����жϿ��淴ӦA2(g)+3B2(g)![]() 2AB3(g)����Ӧ�����ȷ�Ӧ
2AB3(g)����Ӧ�����ȷ�Ӧ
B.ͼ����ʾѹǿ�Կ��淴Ӧ2A(g)+2B(g)![]() 3C(g)+D(s)��Ӱ�죬�ҵ�ѹǿ��
3C(g)+D(s)��Ӱ�죬�ҵ�ѹǿ��
C.ͼ���ɱ�ʾ������Һ��ͨ�백����������������Һ�����Եı仯
D.����ͼ���ܽ������ҺpH��ϵ������ȥCuSO4��Һ�е�Fe3+������Һ�м�������CuO��������pH��4���ҡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.��![]() ��101KPa�����£�1molҺ̬ˮ����Ϊˮ�������յ�����Ϊ
��101KPa�����£�1molҺ̬ˮ����Ϊˮ�������յ�����Ϊ![]() ����
����![]() ��
��![]()
B.��֪![]() ��
��![]() �����������
�������к�����![]() ����Һ�У�����
����Һ�У�����![]() ����
����![]()
C.��֪��![]() �ļ���
�ļ���![]() ��
��![]() �ļ���
�ļ���![]() ��
��![]() �ļ���
�ļ���![]() ��
�� ![]() �ļ���
�ļ���![]() ����Ӧ
����Ӧ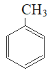 (g)+3H2(g)��
(g)+3H2(g)��![]() (g)���ʱ�Ϊ��
(g)���ʱ�Ϊ��![]()
![]()
D.̼��������Һ�д��ڣ�![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȼ�ϵ����ͼ��ʾ��a��b��Ϊ���Ե缫��������������ȷ����
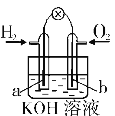
A.a���Ǹ������õ缫�Ϸ���������Ӧ
B.b����Ӧ��O![]() ��4OH
��4OH![]() ��4e
��4e![]() ��2H
��2H![]() O
O
C.�ܷ�Ӧ����ʽΪ2H![]() ��O
��O![]() ��2H
��2H![]() O
O
D.����ȼ�ϵ����һ�־���Ӧ��ǰ������ɫ��Դ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����Ȼ�ѧ����ʽ�У���H1>��H2���� ( )
��C(s)��O2(g)=CO2(g) ��H1 ��C(s)��![]() O2(g)=CO(g) ��H2
O2(g)=CO(g) ��H2
��S(s)��O2(g)=SO2(g) ��H1 ��S(g)��O2(g)=SO2(g) ��H2
��H2(g)��![]() O2(g)=H2O(l) ��H1 ��2H2(g)��O2(g)=2H2O(l) ��H2
O2(g)=H2O(l) ��H1 ��2H2(g)��O2(g)=2H2O(l) ��H2
��CaCO3(s)=CaO(s)��CO2(g) ��H1 ��CaO(s)��H2O(l)=Ca(OH)2(s) ��H2
A. ��B. ��C. �ڢۢ�D. �٢ڢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com