
����Ŀ����CH4����ԭNOX�������������������Ⱦ�����磺
��CH4��g��+4NO2��g��=4NO��g��+CO2��g��+2H2O��g����H1
��CH4��g��+4NO��g��=2N2��g��+CO2��g��+2H2O��g����H2=��1 160 kJmol��1��
��֪NO��NO2���������ܶ�����ͬ�����������ܶȵ�17����16 g����û������ȫ��Ӧ����N2��CO2��H2O��g���ų�1 042.8 kJ������������H1�ǣ�������
A. ��867 kJmol��1 B. ��574 kJmol��1 C. ��691.2 kJmol��1 D. ��925.6 kJmol��1
���𰸡�B
��������
NO��NO2���������ܶ�����ͬ�����������ܶȵ�17�������������ƽ����Է�������=17��2=34����NO�����ʵ�������Ϊx����NO2�����ʵ�������Ϊ1-x��30x+46(1-x)=34�����x=0.75������������NO��NO2�����ʵ���֮��Ϊ��0.75��0.25=3��1��16g��������ʵ���Ϊn=![]() =1mol����CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ��H1����CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ��H2=��1 160 kJmol��1�����ݸ�˹����֪����+�ڵã�CH4(g)+2NO2(g)�TN2(g)+CO2(g)+2H2O(g) ��H=
=1mol����CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ��H1����CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ��H2=��1 160 kJmol��1�����ݸ�˹����֪����+�ڵã�CH4(g)+2NO2(g)�TN2(g)+CO2(g)+2H2O(g) ��H=![]() �� (��H1-1 160 kJmol��1)��NO��NO2�����ʵ���֮��Ϊ3��1�����ݷ���ʽ֪����NO��NO2��ȫת��Ϊ����ʱ���ֱ��NO��NO2��Ӧ�ļ�������ʵ���֮��=
�� (��H1-1 160 kJmol��1)��NO��NO2�����ʵ���֮��Ϊ3��1�����ݷ���ʽ֪����NO��NO2��ȫת��Ϊ����ʱ���ֱ��NO��NO2��Ӧ�ļ�������ʵ���֮��=![]() ��
��![]() =3��2������0.6mol�����NO��Ӧ��0.4mol�ļ����NO2��Ӧ��16g����û������ȫ��Ӧ����N2��CO2��H2O(g)�ų�1042.8kJ����������0.6mol��1160kJ/mol+0.5(-��H1+1 160 kJmol��1)��0.4mol=1042.8kJ�������H1=-574kJ/mol����ѡB��
=3��2������0.6mol�����NO��Ӧ��0.4mol�ļ����NO2��Ӧ��16g����û������ȫ��Ӧ����N2��CO2��H2O(g)�ų�1042.8kJ����������0.6mol��1160kJ/mol+0.5(-��H1+1 160 kJmol��1)��0.4mol=1042.8kJ�������H1=-574kJ/mol����ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���NaOH��Һ�μӵ�ijһԪ��(HA)��Һ�У���û����Һ��pH������Ũ�ȱ仯��ϵ����ͼ��ʾ[��֪��![]() ]��������������ȷ����
]��������������ȷ����

A. Ka(HA) = 10-4.76
B. �μ�NaOH��Һ�����У�![]() ���ֲ���
���ֲ���
C. m����ʾ��Һ�У�c(H+) = c(HA)+c(OH-)-c(Na+)
D. n����ʾ��Һ�п��ܣ�c((Na+) = c(A-)+c(HA)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Һ����Ҫ�����������ӣ����жϸ���Һ�����ʲ�д������뷽��ʽ��
(1)H����CH3COO-_____________��_____________________��
(2)Fe3����SO42-_____________��_______________________��
(3)Na����HCO3-_____________��_______________________��
(4)H+��HS-��S2-_____________��______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�����Ũ�ȶ�Ϊ0.1mol��L��1HA��HB����Һ��20mL���ֱ���0.1mol��L��1NaOH��Һ�ζ�����Һ��pH�����NaOH��Һ���V�Ĺ�ϵ��ͼ��ʾ�������жϴ������
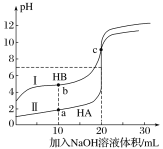
A. �ζ������У�ˮ�����c(H+)��c(OH��)������
B. ��ͬ�����£�HB�ĵ���̶�С��HA�ĵ���̶�
C. V=10mLʱ��c(HB)+c(B��)=2c(Na+)
D. V=20mLʱ��c(A��)>c(B��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��þ����Ͻ���һ����;�ܹ�Ľ������ϣ�Ŀǰ������60%��þ�ǴӺ�ˮ����ȡ�ġ���Ҫ�������£�

(1)Ϊ��ʹMgSO4ת��ΪMg(OH)2���Լ�������ѡ��________��ҪʹMgSO4��ȫת��Ϊ�����������Լ�����ӦΪ________________��
(2)�����Լ������ܹ�����õ�Mg(OH)2�����ķ�����_____________��
(3)�Լ���ѡ��________��д���䷴Ӧ�����ӷ���ʽ_______��
(4)��ˮMgCl2������״̬�£�ͨ������þ���������÷�Ӧ�Ļ�ѧ����ʽΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ�Ӧ��NO+CO2![]() NO2+CO���ܱ������н��У�������Щ�����ӿ�÷�Ӧ����
NO2+CO���ܱ������н��У�������Щ�����ӿ�÷�Ӧ����
A. �������ʹѹǿ��С B. ����������CO2ʹѹǿ����
C. ����������He��ʹѹǿ���� D. ѹǿ�������N2ʹ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ﶬ���������߷����ڣ���������β����ȼúβ���������������Ҫԭ��֮һ��
(1)��ҵ�����ü������ԭNOX�ɼ��ٵ���������ŷš���֪��
CH4(g)+4NO2(g)![]() 4NO(g)+CO2(g)+2H2O(g)��H=-574kJ/mol
4NO(g)+CO2(g)+2H2O(g)��H=-574kJ/mol
CH4(g)+4NO(g)![]() 2N2(g)+CO2(g)+2H2O(g)��H=-1160kJ/mol
2N2(g)+CO2(g)+2H2O(g)��H=-1160kJ/mol
����ֱ�ӽ�NO2��ԭΪN2���Ȼ�ѧ����ʽΪ_______________________________��
(2)����β���������ǿ�������β���ŷš���������β����Ⱦ������Ч���ֶΣ���Ҫԭ��Ϊ2NO(g)+2CO(g)![]() N2(g)+2CO2(g)��H<O����һ�������µĺ����ܱ������г���NO��CO���ô�������ø÷�Ӧ�ڲ�ͬʱ��NO��CO��Ũ�����±���ʾ��
N2(g)+2CO2(g)��H<O����һ�������µĺ����ܱ������г���NO��CO���ô�������ø÷�Ӧ�ڲ�ͬʱ��NO��CO��Ũ�����±���ʾ��
ʱ��/s | 0 | 1 | 2 | 3 | 4 |
c(NO)/mol��L-1 | 9.00��10-3 | 4.00��10-3 | 2.00��10-3 | 1.00��10-3 | 1.00��10-3 |
c(CO)/mol��L-1 | 9.00��10-3 | 4.00��10-3 | 2.00��10-3 | 1.00��10-3 | 1.00��10-3 |
�����п��жϷ�Ӧ�ﵽƽ��״̬����___________(����ĸ����)��
A.c(NO)���ٸı� B.c(NO)/c(CO)���ٸı�
C.c(NO)/c(CO2)���ٸı� D.V(CO)=V(CO2)
�ڴ������´ﵽƽ��ʱ������÷�Ӧ��ƽ�ⳣ��K=________��
��Ϊ�����β��������Ч��,�ɲ�ȡ�Ĵ�ʩ��_____________________(д�����ּ���)��
(3)��ҵ�ϳ����á�����Һ���ա��ķ�����ͬʱ����SO2�͵�������������(NOx),��д������������Һ����NO��NO2�����������1��1�������ӷ���ʽ ___________________��
(4)��Ԫ��(Ce)����ϵ��������Ȼ�����ߵ�һ��,������+3��+4���ּ�̬�������к��д�������Ⱦ��NO�����Ա���Ce4+����Һ����,����NO2����NO3�����������ʵ���֮��Ϊ1:1)���ɲ��õ�ⷨ����������Һ�е�NO2-ת��Ϊ������,ͬʱ����Ce4+,��ԭ������ͼ��ʾ��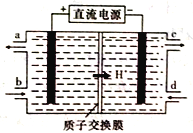
��Ce4+�ӵ��۵�_____(����ĸ����)��������
��д�������ĵ缫��Ӧʽ��______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳ��÷�¯��(��Ҫ��FeO��V2O5����������SiO2��P2O5������)��ȡV2O5���������£�

��1�����յ�Ŀ���ǽ�FeO��V2O3ת��Ϊ������NaVO3���ù����б�������Ԫ����_______________������������Ҫ�ɷ�Ϊ____________________(�ѧʽ)��
��2����MgSO4��Һ���衢��ʱ����������Ҫ�ɷ�Ϊ__________��
��3���ڱ���NH4VO3�Ĺ����У����������ļ���ֵ(������)���¶ȱ仯��������ͼ��ʾ��210��ʱ��ʣ��������ʵĻ�ѧʽΪ_____________________��

��4����V2O5ұ���������������ȷ����������ȷ�Ӧ��ʵ�������__________________.
��5����V2O5��������ϡ����õ�250mL(VO2)2SO4��Һ��ȡ25.00mL����Һ����ƿ�У���0.1000 mol��L-1H2C2O4����Һ���еζ����ﵽ�ζ��յ�ʱ���ı���Һ�����Ϊ20.00mL����֪�ζ�������H2C2O4������ΪCO2��VO2+(��ɫ)����ԭΪVO2+(��ɫ)��
�ٸõζ�ʵ�鲻��Ҫ�������ָʾ�����ﵽ�ζ��յ��������___________________��
��(VO2)2SO4��Һ�����ʵ����ʵ���Ũ��Ϊ___________________��
�۴ﵽ�ζ��յ�ʱ�����ӵζ��ܶ�����ʹ���_________(�ƫ�ߡ�����ƫ�͡�����Ӱ�족)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�뻷���������������ϡ����彡��ϢϢ��ء�
��1��2015�궬���ҹ����ִ�Χ����������������з���PM2.5�ض���Ⱦ������
��������Ϊ�������ӳ��д�����PM2.5Ũ�ȵ���______(�����)��
a��ȼ���̻�����
b��¶�������Ҷ
c��Ϊ�������ɵ���ˮ����
��ȼú���������ڼ���PM2.5��д����̿��ˮ������Ӧ�Ļ�ѧ����ʽ______________________________��
��2��������������������ͷ�չ����Ҫ���ʻ�����
�����в����������ϵ���______(�����)��
a���ֻ������������� b���л������������� c��ʯӢ����
�����ʯ�׳���ʯ��������Ҫ�ɷ���________(�����)��
a��C b��SiO2 c��Al2O3
������������ˮ�����ͨ���������õ��Ĺ�ͬԭ����____(�����)��
a��ʯ��ʯ���� b������������ c�����������d��ʯӢ
��3��ҩ���г���ҩƷ�ܶ�����a.�����b.��ù����c.��˾ƥ����d.θ��ƽ(����������)��
�������__________(�����������������������)��
����ʹ��ǰһ��Ҫ����Ƥ����������(Ƥ��)����______(�����)��
�������ӷ���ʽ����θ��ƽ����Ϊ����ҩ��ԭ��____________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com