
【题目】已知溶液中主要存在下列离子,试判断该溶液的溶质并写出其电离方程式:
(1)H+、CH3COO-_____________、_____________________。
(2)Fe3+、SO42-_____________、_______________________。
(3)Na+、HCO3-_____________、_______________________。
(4)H+、HS-、S2-_____________、______________________。
【答案】CH3COOH CH3COOH![]() H++CH3COO- Fe2(SO4)3 Fe2(SO4)3=2Fe3++3SO42- NaHCO3 NaHCO3=Na++HCO3- H2S H2S
H++CH3COO- Fe2(SO4)3 Fe2(SO4)3=2Fe3++3SO42- NaHCO3 NaHCO3=Na++HCO3- H2S H2S![]() H++HS-,HS-
H++HS-,HS-![]() H++S2-
H++S2-
【解析】
将溶液中含有的离子结合在一起就是相应的溶质电解质,然后判断电解质的强弱,然后根据强电解质完全电离,弱电解质部分电离,多元弱酸分步电离,写出相应的电离方程式。
(1)溶液中含有的主要离子为H+、CH3COO-的电解质是CH3COOH,醋酸是弱电解质,在溶液中只有一部分电解质分子发生电离,存在电离平衡,电离方程式为:CH3COOH![]() H++CH3COO-;
H++CH3COO-;
(2)溶液中含有的主要离子为Fe3+、SO42-的电解质是Fe2(SO4)3,该电解质是盐,属于强电解质,完全电离产生自由移动的离子Fe3+、SO42-,电离方程式为:Fe2(SO4)3=2Fe3++3SO42-;
(3)溶液中含有的主要离子为Na+、HCO3-的电解质是NaHCO3,该电解质是盐,属于强电解质,完全电离产生自由移动的离子Na+、HCO3-,电离方程式为:NaHCO3=Na++HCO3-;
(4)溶液中含有的主要离子为H+、HS-、S2-的电解质是H2S,H2S是二元弱酸,在溶液中存在电离平衡,电离方程式为H2S![]() H++HS-,HS-
H++HS-,HS-![]() H++S2-。
H++S2-。


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:
【题目】在体积为2L的恒容密闭容器内,充入一定量的NO和O2,800°C时发生反应2NO(g)+O2(g)![]() 2NO2(g),容器中n(NO)随时间的变化如表所示:
2NO2(g),容器中n(NO)随时间的变化如表所示:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)反应在1~2s内,O2的物质的量减少__mol。该反应在第3s___(填“达到”或“未达到”)平衡状态。
(2)如图所示,表示NO2浓度变化曲线的是___(填字母)。用O2表示0~2s内该反应的平均速率v=___mol·L-1·s-1。

(3)能说明该反应已达到平衡状态的是___(填字母)。
a.容器内气体颜色不再变化
b.O2的物质的量保持不变
c.容器内混合气体的密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室进行物质制备时,下列从原料及有关试剂分解制取相应的最终产物的设计中,理论上有错误或操作上不可行或经济上不合理的是( )
A. FeFe2O3 ![]() Fe2(SO4)3溶液
Fe2(SO4)3溶液
B. C![]() CO
CO![]() CO2
CO2![]() Na2CO3溶液
Na2CO3溶液
C. CuO![]() CuSO4溶液
CuSO4溶液![]() Cu
Cu
D. CaO![]() Ca(OH)2溶液
Ca(OH)2溶液![]() NaOH溶液
NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有一瓶未知浓度的Na2S2O3,通过下列实验测定其浓度
①取10.0 mL Na2S2O3于锥形瓶中,滴入指示剂2—3滴。
②取一滴定管,依次查漏,洗涤,用0.01 mol·L-1的I2溶液润洗,然后注入该标准溶液,调整液面,记下读数。
③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2+2Na2S2O3 =2NaI+Na2S4O6。
试回答下列问题:
(1)步骤①加入的指示剂是__________。
(2)步聚③达到滴定终点的判断__________________________________。
(3)己知消耗标准液实验数据如下表:
实验次数 | 始读数(ml) | 末读数(ml) |
1 | 0.10 | 19.20 |
2 | 1.85 | 20.75 |
3 | 0.00 | 24.06 |
则废水中的Na2S2O3物质的量浓度为_______________。
(4) 下列操作会导致测定结果偏高的是_________。
A.滴定管在装液前未用标准溶液润洗
B.滴定过程中,锥形瓶振荡得太剧烈,锥形瓶内有液滴溅出
C.装标准溶液的滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
D.达到滴定终点时,仰视读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中△H的含义表示正确的是
A. H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) △H(中和热)
B. NaOH(aq)+![]() H2SO4(浓)=
H2SO4(浓)=![]() Na2SO4(aq)+H2O(l) △H(中和热)
Na2SO4(aq)+H2O(l) △H(中和热)
C. CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H(燃烧热)
D. 2H2(g)+O2(g)=2H2O(g) △H(燃烧热)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蛋白质是构成生物体内的基本物质,蛋白质的组成元素主要有氢、碳、氮、氧、硫,同时还有微量元素铁、锌等。回答下列问题:
(1)碳、氮、氧三元素的第一电离能由小到大的顺序为________________(用元素符号表示);
(2)N3-的立体构型是___________形:与N3-互为等电子体的一种分子是___________(填分子式)。
(3)将足量的氨水逐滴地加入到ZnSO4溶液中,先生成沉淀,然后沉淀溶解生成配合物[Cu(NH3)4SO4,配位化合物中的阳离子结构式为___________;SO42-中的硫原子杂化方式为___________;用价层电子对互斥理论解释SO42-的键角大于SO32-的原因是_________________________________。
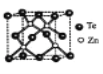
(4)碲化锌晶体有两种结构,其中一种晶胞结构如下图,晶胞中与Zn原子距离最近的Te原子围成____体图形;与Te原子距离最近的Te原子有___个;若Zn与距离最近的Te原子间距为apm,则晶体密度为____g/cm3。
(已知相对原子质量:Zn-65、Te-128)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用CH4催化还原NOX可以消除氮氧化物的污染,例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH2=﹣1 160 kJmol﹣1。
已知NO、NO2混合气体的密度是相同条件下氢气密度的17倍,16 g甲烷和该混合气完全反应生成N2、CO2、H2O(g)放出1 042.8 kJ的热量,则ΔH1是( )
A. ﹣867 kJmol﹣1 B. ﹣574 kJmol﹣1 C. ﹣691.2 kJmol﹣1 D. ﹣925.6 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于油脂和乙酸乙酯的比较正确的是( )
A.油脂和乙酸乙酯都是纯净物,在室温下都是液体
B.油脂和乙酸乙酯在碱性条件下的水解反应都是皂化反应
C.乙酸乙酯和油脂都有果香味,乙酸乙酯是一种特殊的油脂
D.油脂和乙酸乙酯都难溶于水,而易溶于有机溶剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com