
【题目】常温下,将NaOH溶液滴加到某一元酸(HA)溶液中,测得混合溶液的pH与离子浓度变化关系如下图所示[已知:![]() ]。下列叙述不正确的是
]。下列叙述不正确的是

A. Ka(HA) = 10-4.76
B. 滴加NaOH溶液过程中,![]() 保持不变
保持不变
C. m点所示溶液中:c(H+) = c(HA)+c(OH-)-c(Na+)
D. n点所示溶液中可能:c((Na+) = c(A-)+c(HA)
【答案】D
【解析】
A. 根据公式Ka(HA) = ![]() 分析作答;
分析作答;
B. NaA的水解平衡常数Kh (NaA) =![]() ;
;
C. 根据电荷守恒规律及m点离子浓度特点分析;
D. n点溶液显酸性,溶液中溶质为HA和NaA。
A. m点溶液中![]() = 0,即c(HA) = c(A-),结合HA的电离平衡常数公式Ka(HA) =
= 0,即c(HA) = c(A-),结合HA的电离平衡常数公式Ka(HA) = ![]() 得,Ka(HA) = c(H+) = 10-4.76,故A项正确;
得,Ka(HA) = c(H+) = 10-4.76,故A项正确;
B. ![]() = Kh (NaA),其NaA的水解平衡常数Kh (NaA)只与温度有关,则滴加NaOH的过程中,
= Kh (NaA),其NaA的水解平衡常数Kh (NaA)只与温度有关,则滴加NaOH的过程中,![]() 保持不变,故B项正确;
保持不变,故B项正确;
C. m点所示溶液中满足电荷守恒,c(H+) + c(Na+)= c(OH-)+ c(A-),又 c(HA) = c(A-),则有c(H+) = c(HA)+c(OH-)-c(Na+),故C项正确;
D. n点溶液呈酸性,![]() 在2-3之间,则说明混合溶液中的溶质为HA和NaA,则c((Na+) < c(A-)+c(HA),故D项错误;
在2-3之间,则说明混合溶液中的溶质为HA和NaA,则c((Na+) < c(A-)+c(HA),故D项错误;
答案选D。


科目:高中化学 来源: 题型:
【题目】下列溶液中有关物质的量浓度关系不正确的是
A. pH相等的 NaOH、CH3COONa和NaHCO3三种溶液,则有c(NaOH)<c(NaHCO3)<c(CH3COONa)
B. 0.1mol·L-1的NaOH溶液与0.2mol·L-1的HA溶液等体积混合,所得溶液呈碱性:c(Na+)>c(HA)>c(A-)>c(OH-)>c(H+)
C. 25℃时,0.1 mol·L-1 Na2CO3溶液中水电离出来的c(OH-)大于0.1 mol·L-1 NaOH溶液中水电离出来的c(OH-)
D. 已知25℃时Ksp(AgCl)=1.8×10-10,则在该温度下0.3 mol·L -1NaCl溶液中,Ag+的物质的量浓度最大可达到6.0×10-10mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为2L的恒容密闭容器内,充入一定量的NO和O2,800°C时发生反应2NO(g)+O2(g)![]() 2NO2(g),容器中n(NO)随时间的变化如表所示:
2NO2(g),容器中n(NO)随时间的变化如表所示:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)反应在1~2s内,O2的物质的量减少__mol。该反应在第3s___(填“达到”或“未达到”)平衡状态。
(2)如图所示,表示NO2浓度变化曲线的是___(填字母)。用O2表示0~2s内该反应的平均速率v=___mol·L-1·s-1。

(3)能说明该反应已达到平衡状态的是___(填字母)。
a.容器内气体颜色不再变化
b.O2的物质的量保持不变
c.容器内混合气体的密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年4月,中国科学院长春应用化学研究所研究员张新波课题组提出并论证了基于反应6Li+N2![]() 2Li3N,通过Li-N2可充电电池直接利用空气中的氮气实现人工固氮的可能性。电Li-N2池的结构如图所示,电解液为LiCF3SO3。下列说法正确的是
2Li3N,通过Li-N2可充电电池直接利用空气中的氮气实现人工固氮的可能性。电Li-N2池的结构如图所示,电解液为LiCF3SO3。下列说法正确的是
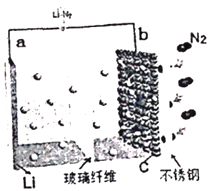
A. b极为电池的负极
B. 电池放电时Li+移向a极
C. b极的电极方程式为N2+6Li++6e- = 2Li3N
D. 金属锂在放电过程中发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用下列装置进行有关Cl2的实验。下列说法不正确的是( )
A.  图中:实验现象证明氯气无漂白作用,氯水有漂白作用
图中:实验现象证明氯气无漂白作用,氯水有漂白作用
B.  图中:收集氯气
图中:收集氯气
C.  图中:生成棕黄色的烟,加少量水溶解得到蓝绿色溶液
图中:生成棕黄色的烟,加少量水溶解得到蓝绿色溶液
D.  图中:若气球干瘪,证明可与NaOH溶液反应
图中:若气球干瘪,证明可与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。可通过以下反应制得:2KClO3+H2C2O4+H2SO4![]() 2ClO2↑+K2SO4+2CO2↑+2H2O。有关该反应的说法正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O。有关该反应的说法正确的是( )
A. H2C2O4是还原剂B. KClO3在反应中失电子
C. KClO3被还原D. H2SO4发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室进行物质制备时,下列从原料及有关试剂分解制取相应的最终产物的设计中,理论上有错误或操作上不可行或经济上不合理的是( )
A. FeFe2O3 ![]() Fe2(SO4)3溶液
Fe2(SO4)3溶液
B. C![]() CO
CO![]() CO2
CO2![]() Na2CO3溶液
Na2CO3溶液
C. CuO![]() CuSO4溶液
CuSO4溶液![]() Cu
Cu
D. CaO![]() Ca(OH)2溶液
Ca(OH)2溶液![]() NaOH溶液
NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用CH4催化还原NOX可以消除氮氧化物的污染,例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH2=﹣1 160 kJmol﹣1。
已知NO、NO2混合气体的密度是相同条件下氢气密度的17倍,16 g甲烷和该混合气完全反应生成N2、CO2、H2O(g)放出1 042.8 kJ的热量,则ΔH1是( )
A. ﹣867 kJmol﹣1 B. ﹣574 kJmol﹣1 C. ﹣691.2 kJmol﹣1 D. ﹣925.6 kJmol﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com