
【题目】某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A(g)+xB(g)2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如图所示.下列说法中正确的是( ) 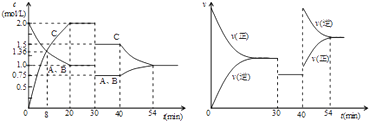
A.30min时降低温度,40min时充入生成物C
B.0~8min内A的平均反应速率为0.08mol/(Lmin)
C.反应方程式中的x=1,正反应为吸热反应
D.20min~40min间该反应的平衡常数均为8
【答案】B
【解析】解:A.由图象可知,30min时只有反应速率降低了,反应物与生成物的浓度瞬时降低,反应仍处于平衡状态,故不能是温度变化,而是降低了压强,40min时,正逆反应速率都增大,且逆反应速率大于正反应速率,平衡向逆向进行,应是升高温度,则正反应为放热反应,故A错误;
B.反应从开始到8min内浓度减少了0.64mol/L,故A的反应速率为0.08 mol/(Lmin),故B正确;
C.由开始到达到平衡,A、B的浓度减少的量相同,由此可知X=1,则增大压强平衡不移动,40min时,正逆反应速率都增大,且逆反应速率大于正反应速率,平衡向逆向进行,应是升高温度,则正反应为放热反应,故C错误;
D.20~30 min间,各物质的浓度为:c(A)=c(B)=1mol/L,c(C)=2mol/L,所以K= ![]() =4,30~40min时改变条件为压强,所以K不变,所以20min~40min间该反应的平衡常数均为4,故D错误.
=4,30~40min时改变条件为压强,所以K不变,所以20min~40min间该反应的平衡常数均为4,故D错误.
故选B.
由图象可知,30min时只有反应速率降低了,反应物与生成物的浓度瞬时降低,反应仍处于平衡状态,故不能是温度变化,而是降低了压强;
反应从开始到8min内浓度减少了0.64mol/L,故A的反应速率为0.08 mol/(Lmin);
由开始到达到平衡,A、B的浓度减少的量相同,由此可知X=1,则增大压强平衡不移动,40min时,正逆反应速率都增大,且逆反应速率大于正反应速率,平衡向逆向进行,应是升高温度,则正反应为放热反应.


科目:高中化学 来源: 题型:
【题目】下列实验操作或记录正确的是( )
A.用托盘天平称取2.50 g胆矾,受热充分失水后,固体质量减轻0.90 g
B.用量筒测得排水法收集制得的氢气体积为50.28 mL
C.用两只250 mL的容量瓶配制0.1 molL﹣1500 mLNaOH溶液
D.常温常压下测得1 mol N2的质量为28 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、Y、Z的原子序数依次增大,W与Y最外层电子数之和为X的最外层电子数的2倍。Z最外层电子数等于最内层电子数,X、Y、Z的简单离子的电子层结构相同,W的单质是空气中体积分数最大的气体,下列说法正确的是
A. 离子半径的大小顺序:r(W)>r(X)>r(Y)>r(Z)
B. W的气态氢化物比X的稳定
C. XY2与ZY2中的化学键类型相同
D. Y的最高价氧化物对应水化物的酸性比W的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在含CH3COOH和CH3COOˉ的溶液中,CH3COOH和CH3COOˉ二者中各自所占的物质的量分数(α)随溶液pH变化的关系如图所示.下列说法不正确的是( ) 
A.在pH<4.76的溶液中,c(CH3COO﹣)<c(CH3COOH)
B.在pH=7的溶液中,α(CH3COOH)=0,α(CH3COO﹣)=1.0
C.在pH>4.76的溶液中,c(CH3COO﹣)与c(OH﹣)之和可大于c(H+)
D.在pH=4.76的溶液中加盐酸,α(CH3COOH)与α(CH3COO﹣)之和保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、D、E、W是中学常见的四种元素,原子序数依次增大。A的原子最外层电子数是次外层的2倍,D的氧化物属于两性氧化物,D、E位于同周期,A、D、E的原子最外层电子数之和为14,W是人体必需的微量元素,缺乏W会导致贫血症状。
(1)A在元素周期表中的位置是__________________。
(2)下列事实能用元素周期律解释的是_____(填字母序号)。
a . D的最高价氧化物对应水化物的碱性弱于Mg(OH)2
b. E的气态氢化物的稳定性小于HF
c. WE3的溶液可用于刻蚀铜制的印刷电路板
(3)E的单质可以从NaBr溶液中置换出Br2单质,从原子结构的角度解释其原因是__________。
(4)①工业上用电解法制备D的单质,反应的化学方程式为____________________。
②家用“管道通”的有效成分是烧碱和D的单质,使用时需加入一定量的水,此时发生反应的化学方程式为____________________。
(5)W的单质可用于处理酸性废水中的NO3-,使其转换为NH4+,同时生成有磁性的W的氧化物X,再进行后续处理。
① 上述反应的离子方程式为__________。
② D的单质与X在高温下反应的化学方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以氧化铝为原料,通过碳热还原法可合成氮化铝(AlN);通过电解法可制取铝.电解铝时阳极产生的CO2可通过二氧化碳甲烷化再利用. 请回答:
(1)已知:2Al2O3(s)═4Al(g)+3O2(g)△H1=3351KJmol﹣12C(s)+O2(g)═2CO(g)△H2=﹣221KJmol﹣1
2Al(g)+N2(g)═2AlN(s)△H3=﹣318KJmol﹣1
碳热还原Al2O3合成AlN的总热化学方程式是 , 该反应自发进行的条件 .
(2)在常压、Ru/TiO2催化下,CO2和H2混和气体(体积比1:4,总物质的量a mol)进行反应,测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化的CO2中生成CH4或CO的百分比). 反应ⅠCO2(g)+4H2(g)CH4(g)+2H2O(g)△H4
反应ⅡCO2(g)+H2(g)CO(g)+H2O(g)△H5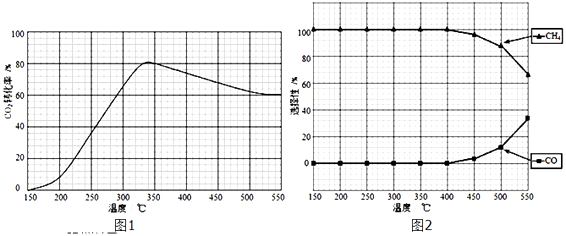
①下列说法不正确的是
A.△H4小于零
B.温度可影响产物的选择性
C.CO2平衡转化率随温度升高先增大后减少
D.其他条件不变,将CO2和H2的初始体积比改变为1:3,可提高CO2平衡转化率
②350℃时,反应Ⅰ在t1时刻达到平衡,平衡时容器体积为VL该温度下反应Ⅰ的平衡常数为(用a、V表示)
③350℃下CH4物质的量随时间的变化曲线如图3所示.画出400℃下0~t1时刻CH4物质的量随时间的变化曲线. 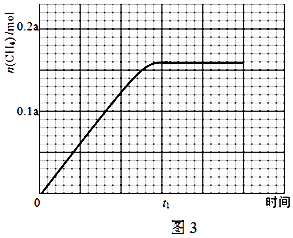
(3)据文献报道,CO2可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、N、O、Al、Si、Cu是常见的六种元素.
(1)Si位于元索周期表第周期第族.
(2)N原子的原子结构示意图为;Cu的低价氧化物的颜色为 .
(3)用“>”或“<”填空:
原子半径 | 电负性 | 熔点 | 沸点 |
AlSi | NO | 金刚石晶体硅 | CH4SiH4 |
(4)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生. 
0﹣t1时,原电池的负极是Al片,此时,正极的电极反应式是 , 溶液中的H+向极移动,t1时,原电池中电子流动方向发生改变,其原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置进行下列实验,能达到实验目的的是( )
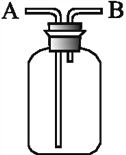
A. 瓶中盛适量浓硫酸,从A口进气来干燥NH3
B. 从B口进气,用排空气法收集SO2
C. 瓶中盛满水,从B口进气,用排水法收集NO2
D. 瓶中盛满水,A口连接导管并伸入量筒中,从B口进气用排水法测量生成NO的体积,
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com