
【题目】下列烷烃命名正确的是( )
A. 1,4-二甲基丁烷 B. 3-甲基-4-乙基己烷
C. 2-乙基戊烷 D. 2,3,3-三甲基丁烷
 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法错误的是
A. 1 LpH=1 Ba(OH)2溶液中所含OH-的数目为0.2NA
B. 28g聚乙烯![]() 中含有的碳原子数为2NA
中含有的碳原子数为2NA
C. 1 mol CH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-的数目为NA
D. 1 mol Na与O2完全反应生成Na2O和Na2O2的混合物,转移的电子总数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D四种第一、二周期元素,A分别与B、C、D结合生成甲、乙、丙三种化合物,且甲、乙、丙3分子中含相同数目的质子数,C、D结合生成化合物丁。有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如下图:

(1)写出B+乙→甲+C的化学反应方程式__________________。
(2)根据以上条件可以确定A、B、C、D四种元素中的三种,分别是_______、_______、_______(元素符号)
(3)依据下列条件可以进一步确定上述第四种元素:
①甲与丙以及乙与丙均能够发生反应,②甲、丙、丁都是无色有刺激性气味的物质。据此,请回答下列问题:
A.写出上述第四种元素在周期表中的位置______________。
B.写出C+丙→乙+丁的化学反应方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
①将金属Na投入水中:2Na+2H2O=2Na++2OH-+H2↑
②在硫酸溶液中加入氢氧化钡溶液至中性:Ba2++OH-+H++SO2-4=BaSO4↓+H2O
③碳酸氢钠溶液中滴加盐酸:HCO3-+H+=CO2↑+H2O
④氢氧化钠中滴加醋酸:OH-+H+=H2O
A. ①③④ B. ①③ C. ②④ D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物排放是形成臭氧层空洞、酸雨、雾霾的重要成因之一。SCR法是工业上消除氮氧化物的常用方法,反应原理为:4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g) △H<0
4N2(g)+6H2O(g) △H<0
(1)氮氧化物破坏臭氧层原理为:①NO+O3![]() NO2+O2 ②NO2+O
NO2+O2 ②NO2+O![]() NO+O2
NO+O2
常温下反应①的平衡常数为K1,反应②的平衡常数为K2,则反应O3+O![]() 2O2的平衡常数K =________(用K1、K2表示)。
2O2的平衡常数K =________(用K1、K2表示)。

(2)SCR法除NO时,投料比一定时有利于提高NO平衡转化率的反应条件是________、________。该法可能发生副反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),减少副反应的主要措施是________、________。
4NO(g)+6H2O(g),减少副反应的主要措施是________、________。
(3)其他条件相同,在甲、乙两种催化剂作用下,NO转化率与温度的关系如图。
①工业上选择催化剂乙的原因是________;
②在催化剂甲作用下,图中M点处(对应温度为210℃)NO的转化率_________(填“可能是”、“一定是”或“一定不是”)该温度下的平衡转化率。高于210℃时,NO转化率降低的原因可能是________。
(4)消除汽车尾气中的NO时,可用尿素[(NH2)2CO]还原NO,既安全又高效,且产物都是空气中含有的成分。与SCR法相比,等物质的量的尿素与氨气可消除的NO物质的量之比为________。(不考虑副反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸钴用途广泛,可用于指示剂和催化剂制备。一种利用水钴矿[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等]制取CoC2O4·2H2O工艺流程如下:

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中加入Na2SO3的目的是将_____________还原(填离子符号)以便固体溶解。该步反应的离子方程式为 (写一个)。
(2)NaClO3的作用是将浸出液中的Fe2+氧化成Fe3+,氯元素被还原为最低价。该反应的离子方程式为 。
(3)利用平衡移动原理分析:加Na2CO3能使浸出液中Fe3+、Al3+转化成氢氧化物沉淀的原因是 。
(4)萃取剂对金属离子的萃取率与pH的关系如图所示。滤液Ⅱ中加入萃取剂的作用是 ;使用萃取剂适宜的pH=____(填序号)左右:

A.2.0 B.3.0 C. 4.0
(5)滤液Ⅰ“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液c(Mg2+)/c(Ca2+)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以淀粉为主要原料合成一种具有果香味有机物C和高分子化合物E的合成路线如下图所示。
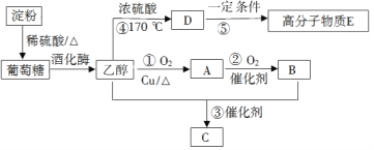
请回答下列问题:
(1)写出C的结构简式:__________________,A分子内含有的官能团是_______(填名称)。
(2)写出下列反应的反应类型:①________________,③________________。
(3)写出下列反应的化学方程式:①________________________;⑤________________________。
(4)某同学欲用下图装置制备物质C,将试管B中的物质C分离出来,用到的主要玻璃仪器有:烧杯、________,插入试管B的导管接有一个球状物,其作用为________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能说明非金属性C1>I的是
A. C12+2I-=2C1-+I2 B. 稳定性:HC1>HI
C. 酸性:HC1O4>HIO4 D. 酸性:HC1O3>HIO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com