
ϴ����ȫ�����ǵ¹���ȫ����Ҫ���ϡ�������������ײ��˲�䣬��ȫװ��ͨ����ʹ���еķ�ĩ�ֽ��ͷų������ĵ����γ����ң��Ӷ�����˾�����˿������˺���Ϊ�о���ȫ���ҹ����Ļ�ѧԭ����ȡ��ȫװ���еķ�ĩ����ʵ�顣����ɷ�����ȷ���÷�ĩ��Na��Fe��N��O����Ԫ�ء�ˮ������������������ĩ�����ܽ⡣����⣬������Ϊ������ף�������Ϊ����ɫ���壬���������ᡣ
ȡ13.0g������ף�����ʹ����ȫ�ֽ⣬���ɵ����͵����ң����ɵĵ����ۺϳɱ�״���µ����Ϊ6.72L���������ڸ��¸����������������벻�������ɫ��ĩ��Ӧ���ɻ������������һ�ֵ��ʡ��������������Ӵ���ת��Ϊ�������Ρ�
��ش��������⣺
��1���Ļ�ѧʽΪ �����ĵ���ʽΪ ��
��2�������ڿ�����ת��Ϊ̼�����Σ���Ӧ�Ļ�ѧ����ʽΪ ��
��3�������������ɫ��ĩ������Ӧ�Ļ�ѧ����ʽΪ ����ȫ�����к���ɫ��ĩ�������� ��
��4�����������У��п�����Ϊ��ȫ�����к���ɫ��ĩ���Ʒ���� ��
A. KCl B. KNO3 C. Na2S D. CuO
��5�����һ��ʵ�鷽����̽���������������Ӵ������ɿ������εijɷ֣������ǽᾧˮ��� ��
 ���������1����ĩ���������ʻ�϶��ɡ�2������ɫ���ʿ���ΪFe2O3\Fe(OH)3��,��������ֻ����Fe2O3��3����ֻ������Ԫ�أ��Һ�N���غ�Na��3�����㣺N(6.72/22.4)*2*14=8.4g����Na�����ʵ���Ϊ����13-8.4��/23=0.2mol��N��Na�����ʵ���֮��Ϊ��0.6:0.2=3:1�������ΪNa3N��4���ڸ�����Na��Fe2O3��Ӧ�IJ���ΪNa2O2��Fe��
���������1����ĩ���������ʻ�϶��ɡ�2������ɫ���ʿ���ΪFe2O3\Fe(OH)3��,��������ֻ����Fe2O3��3����ֻ������Ԫ�أ��Һ�N���غ�Na��3�����㣺N(6.72/22.4)*2*14=8.4g����Na�����ʵ���Ϊ����13-8.4��/23=0.2mol��N��Na�����ʵ���֮��Ϊ��0.6:0.2=3:1�������ΪNa3N��4���ڸ�����Na��Fe2O3��Ӧ�IJ���ΪNa2O2��Fe��
���͵��ѵ�1��ͨ�����ԺͶ������ַ�ʽȷ�����ʵĻ�ѧ�ɷ֣�����Na3N����ѧ���ܲ���Ϥ�ġ��ѵ�2��������ԭ����ʽ����д����ƽ����������ԭԭ����Ӧ�á��ѵ�3��ʵ����ƣ�ͨ�����������ԡ�������Ŀ�����������ƶ���ƽʱ����ϰ�������б�Ȼ���漰������ʵ����Ʋ��֣���ʡ�ж��ͳ���о����й�̼�������ᷴӦ����������ֹ�������ϰ���������ڼ��Ļ�����Ҳ�������Ѷȵġ�������Ҫ���õ�ƽʱ֪ʶ�Ļ��ۣ������ɰܻ�����ƽʱ��
���𰸡�
��1��Na3N��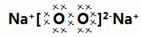
(2)2N2O2+4CO2+2H2O=4NaHCO3+O2
(3)6Na+2Fe2O3=3Na2O2+4Fe ,��ɫ��ĩ�������dz䵱����������ȥ�����Ʒֽ�����Ľ����ƣ����� ������ˮ�����������Ⱥͼ����к����ʣ����ṩ�������������ڵ����Ƶ�Ѹ�ٷֽ⡣
������ˮ�����������Ⱥͼ����к����ʣ����ṩ�������������ڵ����Ƶ�Ѹ�ٷֽ⡣
��4���������ԽǶȷ���KNO3��CuO���ɣ���KNO3�������ȷֽ⣬���������뵪����Ӧ����ѡ��D. CuO����5��ʵ��Ŀ�ģ�����Na2O2�ڿ�������ˮ�������̼��Ӧ�IJ��������NaOH��Na2CO3��NaHCO3��ʵ�����һ��ʵ��ԭ����������������
���裺1��������Ϲ����������2�����������ȣ���������ͨ�����ʯ��ˮ������������NaHCO3��ʯ��ˮ���������NaHCO3��NaOH������ʯ��ˮ�����仯��mg��3������������ᣬ������������ͨ�����ʯ��ˮ������ʯ��ˮ����������ng��4��ͨ��m��n�ļ��������ս����
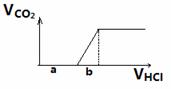 ʵ����ƶ���ʵ��ԭ�����ⶨ�������������������̼�����Ĺ�ϵȷ�������ɷ֡�1��������������̼������ֻ��NaOH��2����ʼ����������̼ǰ���뿪ʼ����������ֱ̼����������ĵ�����������Ϊ1:1��ֻ��Na2CO3������1:1��ΪNaOH��Na2CO3�Ļ���С��1:1��ΪNa2CO3��NaHCO3�Ļ������Ƚ�ͼ��a,b�Ĵ�С��
ʵ����ƶ���ʵ��ԭ�����ⶨ�������������������̼�����Ĺ�ϵȷ�������ɷ֡�1��������������̼������ֻ��NaOH��2����ʼ����������̼ǰ���뿪ʼ����������ֱ̼����������ĵ�����������Ϊ1:1��ֻ��Na2CO3������1:1��ΪNaOH��Na2CO3�Ļ���С��1:1��ΪNa2CO3��NaHCO3�Ļ������Ƚ�ͼ��a,b�Ĵ�С��


 ��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д� �����������Ż�ѧϰϵ�д�
�����������Ż�ѧϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NA��ʾ�����ӵ�����������˵���У���ȷ���ǣ� ��
A�����³�ѹ�£�3.0 g�����к��е�̼�����Ϊ0.7 NA
B����״���£�22.4 L C2H5OH�к��е���ԭ����Ϊ6 NA
C�����³�ѹ�£�92 g�� NO2��N2O4 ������庬�е�ԭ����Ϊ 6 NA
D����״���£���Na2O2�Ƶ�11.2 L O2����Ӧת�Ƶĵ�����Ϊ0.5 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ��ѧ�кܶࡰ���ɡ����������÷�Χ�����и����йء����ɡ��Ƴ��Ľ�����ȷ����(����)
| ѡ�� | ���� | ���� |
| A | ��ǿ�������ȡ������ | ��������Һ����ȡ���� |
| B | ��Ӧ��Ũ��Խ��Ӧ����Խ�� | �����£���ͬ����Ƭ�зֱ����������Ũ��ϡ���ᣬŨ��������Ƭ���ܽ��� |
| C | �ṹ��������Ƶ����ʣ��е�����Է���������������� | NH3�ķе����PH3 |
| D | �ܽ��С�ij��������ܽ�ȸ�С�ij���ת�� | ZnS�����еμ�CuSO4��Һ���Եõ�CuS���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ƣ���������Ӻ���(xNa2SO4��yH2O2��zH2O)����ɿ�ͨ������ʵ��ⶨ����ȷ��ȡ1.7700 g��Ʒ�����Ƴ�100.00 mL��ҺA����ȷ��ȡ25.00 mL��ҺA�����������ữ��BaCl2��Һ��������ȫ�����ˡ�ϴ�ӡ����������أ��õ���ɫ����0.5825 g����ȷ��ȡ25.00 mL��ҺA��������ϡ�����ữ����0.020 00  mol��L��1 KMnO4��Һ�ζ����յ㣬����KMnO4��Һ25.00 mL��H2O2��KMnO4��Ӧ�����ӷ���ʽ���£�
mol��L��1 KMnO4��Һ�ζ����յ㣬����KMnO4��Һ25.00 mL��H2O2��KMnO4��Ӧ�����ӷ���ʽ���£�
2MnO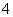 ��5H2O2��6H��===2Mn2����8H2O��5O2��
��5H2O2��6H��===2Mn2����8H2O��5O2��
(1)��֪������BaSO4��Ksp��1.1��10��10����ʹ��Һ��c(SO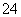 )��1.0��10��6mol��L��1��Ӧ������Һ��c(Ba2��)��_______mol��L��1��
)��1.0��10��6mol��L��1��Ӧ������Һ��c(Ba2��)��_______mol��L��1��
(2)�����ζ�������ϡ�����ữ��MnO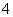 ����ԭΪMnO2�������ӷ���ʽΪ__________________��
����ԭΪMnO2�������ӷ���ʽΪ__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ǰ����ǣ�Li2NH����һ�ִ�������������ȫ�ԺõĹ��崢����ϣ��䴢��ԭ���ɱ�ʾΪLi2NH��H2��LiNH2��LiH�������й�˵����ȷ����
A.Li2NH��N�Ļ��ϼ��ǣ�1 B.�÷�Ӧ��H2�������������ǻ�ԭ��
C.Li����H�������Ӱ뾶��� D.�˷������ƿ�����ԭ����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij����ˮ�к�5.00��10-3 mol��L-1��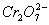 ,�䶾�Խϴ�ij�о���ѧϰС��Ϊ�˱��Ϊ��,����ˮ�����õ���
,�䶾�Խϴ�ij�о���ѧϰС��Ϊ�˱��Ϊ��,����ˮ�����õ��� �Բ���Cr0.5Fe1.5FeO4(Fe�Ļ��ϼ�����Ϊ+3��+2),���������ʵ������:
�Բ���Cr0.5Fe1.5FeO4(Fe�Ļ��ϼ�����Ϊ+3��+2),���������ʵ������:
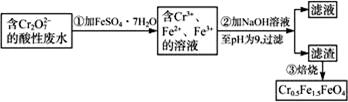
(1)�ڢٲ���Ӧ�����ӷ���ʽ��____________________________________��
(2)�ڢڲ�����pH��ֽ�ⶨ��ҺpH�IJ�����:__________________��
(3)�ڢڲ����˵õ�����������Ҫ�ɷֳ�Cr(OH)3��,����__________________��
(4)��ʹ1 L�÷�ˮ�е�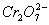 ��ȫת��ΪCr0.5Fe1.5FeO4,��������Ҫ����_________g FeSO4��7H2O��
��ȫת��ΪCr0.5Fe1.5FeO4,��������Ҫ����_________g FeSO4��7H2O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£���H2O2��Һ�еμ�����FeSO4��Һ���ɷ�������������Ӧ��
2Fe2++H2O2+2H+====2Fe3++2H2O
2Fe3++H2O2====2Fe2++O2��+2H+
����˵����ȷ���ǣ� ��
A.H2O2�������Ա�Fe3+ǿ���仹ԭ�Ա�Fe2+��
B.��H2O2�ֽ�����У���Һ��pH���½�
C.��H2O2�ֽ�����У�Fe2+��Fe3+���������ֲ���
D.H2O2��������Ҫ�ϸ�������Fe2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪������ԭ��Ӧ��
2Cu(IO3)2+24KI+12H2SO4=2CuI��+13I2+12K2SO4+12H2O
����1mol�������ڷ�Ӧ�еõ��ĵ���Ϊ
A.10 mol B.11 mol
C.12 mol D.13 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�л�������A~H��ת����ϵ������ʾ��
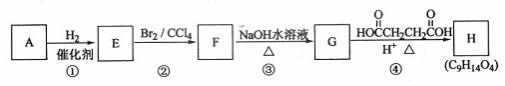
��ش��������⣺
��1������A��������ֻ��һ�������ţ�����Է���������65~75֮�䣬1 mol A��ȫȼ������7 mol��������A�Ľṹ��ʽ�� �������� ��
��2�����ض����������£�A������ʵ�����H2��Ӧ����E����Eת��ΪF�Ļ�ѧ����ʽ�� ��
��3��G������Ʒ�Ӧ�ܷų����壬��Gת��ΪH�Ļ�ѧ����ʽ�� ��
��4���ٵķ�Ӧ������ ���۵ķ�Ӧ������ ��
��5������B��A��ͬ���칹�壬�����е�����̼ԭ�ӹ�ƽ�棬����⻯����Ϊ����Ϊ�飬д��B���п��ܵĽṹ��ʽ
��6��CҲ��A��һ��ͬ���칹�壬����һ�ȴ���ֻ��һ�֣������������칹����C�Ľṹ��ʽΪ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com