
【题目】金属M在酸性或碱性溶液中均可与HNO3发生氧化还原反应,转化关系如图(部分生成物未列出): 
已知:C、D、E、G均为气体,且G为单质;将D通入A溶液产生白色沉淀;将F逐滴加入B溶液至过量,先产生白色沉淀,随后沉淀消失.
请回答下列问题:
(1)写出下列物质的化学式:M、F、G .
(2)A溶液与B溶液混合也能产生白色沉淀,写出该反应的离子方程式 .
(3)除去气体C中的气体E的化学方法是 .
(4)将10mL充满气体E和O2混合气的试管倒扣在水槽中,反应后试管中残留1mL无色气体,则试管中气体E的体积是mL
(5)D→C反应的化学方程式是 .
(6)M与NO3﹣在碱性条件下反应的离子方程式为 .
【答案】
(1)Al;HNO3;N2
(2)Al3++3AlO2﹣+6H2O=4Al(OH)3↓
(3)将气体通入水中,再用排水法收集
(4)8.6或7.2
(5)4NH3+5O2 ![]() 4NO+6H2O
4NO+6H2O
(6)8Al+3NO3﹣+5OH﹣+2H2O=8Al+3NH3↑
【解析】解:C、D、E、G均为气体,且G为单质,根据各物质转化关系,D能催化氧化得C,C氧化得E,D与E催化作用下生成G,则可推知D为NH3 , C为NO,E为NO2 , G为N2 , E与水反应生成F为HNO3 , 将F逐滴加入B溶液至过量,先产生白色沉淀,随后沉淀消失,则说明B中含有偏铝酸根,将D通入A溶液产生白色沉淀,说明A中含有铝离子,结合图中转化关系可知,M为Al,A为Al(NO3)3 , B为含AlO2﹣的溶液,(1)根据上面的分析可知,M为Al,F为HNO3 , G为N2 , 所以答案是:Al;HNO3;N2;(2)A溶液与B溶液混合也能产生白色沉淀为氢氧化铝,反应的离子方程式为Al3++3AlO2﹣+6H2O=4Al(OH)3↓,
所以答案是:Al3++3AlO2﹣+6H2O=4Al(OH)3↓; (3)由于二氧化氮与水反应能生成一氧化氮,所以除去气体NO中的气体NO2的化学方法是将气体通入水中,再用排水法收集,
所以答案是:将气体通入水中,再用排水法收集; (4)将10mL充满气体NO2和O2混合气的试管倒扣在水槽中,反应后试管中残留1mL无色气体可能为氧气,也可能为NO,当残留的为氧气时,则根据反应4NO2+O2+H2O=4HNO3 , 可知,参加反应的体积为 ![]() mL=7.2mL,当残留的为NO时,原反应剩余二氧化氮为3mL,则根据反应4NO2+O2+H2O=4HNO3 , 可知参加反应的二氧化氮为
mL=7.2mL,当残留的为NO时,原反应剩余二氧化氮为3mL,则根据反应4NO2+O2+H2O=4HNO3 , 可知参加反应的二氧化氮为 ![]() mL=5.6mL,则试管中NO2的总体积是5.6mL+3mL=8.6mL,
mL=5.6mL,则试管中NO2的总体积是5.6mL+3mL=8.6mL,
所以答案是:8.6或7.2; (5)D→C反应的化学方程式是4NH3+5O2 ![]() 4NO+6H2O,
4NO+6H2O,
所以答案是:4NH3+5O2 ![]() 4NO+6H2O; (6)Al与NO3﹣在碱性条件下反应的离子方程式为8Al+3NO3﹣+5OH﹣+2H2O=8Al+3NH3↑,
4NO+6H2O; (6)Al与NO3﹣在碱性条件下反应的离子方程式为8Al+3NO3﹣+5OH﹣+2H2O=8Al+3NH3↑,
所以答案是:8Al+3NO3﹣+5OH﹣+2H2O=8Al+3NH3↑.


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3 , 含Fe2O3杂质)为原料冶炼铝的工艺流程如下,下列叙述正确的是( ) 
A.试剂X可以是氢氧化钠溶液,也可以是盐酸
B.反应①、过滤后所得沉淀为氢氧化铁
C.图中所示转化反应都不是氧化还原反应
D.反应②的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氯的物质与人们的生活密切相关.已知氯元素常见的化合价有﹣1、0、+1、+3、+5、+7六种,其不同价态的物质间可以相互转化.回答下列问题.
(1)氯原子的原子结构示意图;氯离子的电子式 .
(2)氯气能使湿润的有色布条褪色,起到漂白作用的物质是(写名称).漂粉精的主要有效成分是(写化学式).
(3)实验室制取氯化氢的化学方程式;
(4)工业上将含有氯气的尾气通过进行处理,在处理时发生的反应中氯气作为 . a.氧化剂 b.还原剂 c.既是氧化剂又是还原剂 d.既不是氧化剂又不是还原剂
(5)写出氯气的两种用途 , .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有①甲醇、②乙醛、③苯、④聚乙烯、⑤苯酚、⑥环己烷、⑦邻二甲苯、⑧环己烯( ![]() ).其中既能使KMnO 4酸性溶液褪色又能与溴水反应使溴水褪色的是( )
).其中既能使KMnO 4酸性溶液褪色又能与溴水反应使溴水褪色的是( )
A.②④⑤⑧
B.②⑤⑧
C.②④⑤⑦
D.②④⑤⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1L某混合溶液中,溶质X,Y的浓度都为0.1molL﹣1 , 向混合溶液中滴加某溶液Z(0.1molL﹣1氢氧化钠或硫酸溶液)至溶液呈中性,所得沉淀的物质的量如图所示,则X,Y,Z分别是( ) 
A.氯化铝、氯化铁、氢氧化钠
B.氯化铝、氯化镁、氢氧化钠
C.偏铝酸钠、氢氧化钡、硫酸
D.偏铝酸钠、氯化钡、硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一种钠硫高能电池的结构示意图,M由Na2O和Al2O3制得,其作用是导电和隔膜,该电池反应为2Na+xS=Na2Sx . 该电池正极的电极反应式为 .
用该电池作电源进行铁件镀铜时,若电镀池中两电极的质量开始相同,电镀完成后取出洗净、烘干、称量,二者质量差为25.6g,则理论上该电池负极消耗的质量为g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计实验图以确认上述混合气体中有C2H4和SO2 . 回答下列问题: 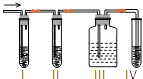
(1)实验室制备乙烯的反应方程式是:
(2)I、Ⅱ、Ⅲ、IV装置可盛放的试剂是I;Ⅱ;Ⅲ;Ⅳ . (将下列有关试剂的序号填入空格内). A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(3)能说明SO2气体存在的现象是 .
(4)使用装置II的目的是 .
(5)使用装置III的目的是 .
(6)确定含有乙烯的现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学研究铝及其化合物的性质时设计了如下两个实验方案.
方案①:2.7g Al ![]() X溶液
X溶液 ![]() Al(OH)3沉淀
Al(OH)3沉淀
方案②:2.7g Al ![]() Y溶液
Y溶液 ![]() Al(OH)3沉淀
Al(OH)3沉淀
NaOH和HCl的浓度均是3mol/L,如图是向X溶液和Y溶液中分别加入NaOH和HCl时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法不正确的是( )
A.b曲线表示的是向X溶液中加入NaOH溶液
B.在O点时两方案中所得溶液浓度相等
C.方案②中对应的O点HCl恰好反应完
D.X溶液显酸性,Y溶液显碱性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com