
【题目】查阅资料知:Br2的沸点为58.78℃,密度为3.119gcm﹣3,微溶于水,有毒。
Ⅰ.(1)常温下,单质溴通常呈__态,保存时通常在盛溴的试剂瓶中加入少量__液封。
Ⅱ.工业生产中,海水提取溴常用空气吹出法。其生产流程可用如图表示:
浓缩海水![]() 低浓度溴水
低浓度溴水![]() 含Br﹣的溶液
含Br﹣的溶液![]() 溴的浓溶液→液溴
溴的浓溶液→液溴
某化学实验小组模拟该法设计了如图实验装置(夹持装置略去)从浓缩的海水中提取液溴实验步骤如下:
①关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl2,至反应结束;
②关闭a、c,打开b、d,向A中鼓入足量热空气;
③关闭b,打开a,再通过A向B中通入足量的Cl2;
④将B中所得液体进行蒸馏,收集液溴。
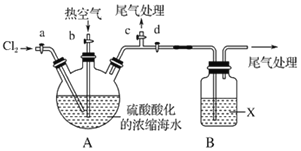
(2)当观察到A中液面上方出现____(实验现象)即可判断步骤①中反应已经结束。
(3)X试剂可以是___,尾气处理选用___(填序号,试剂不重复使用)。
a.H2O b.饱和食盐水 c.NaOH溶液 d.饱和Na2SO3溶液
B中X试剂发生反应的离子方程式为____________________________________。
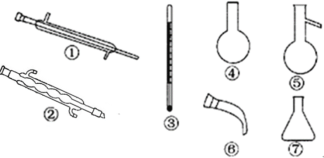
(4)蒸馏时应该选择下列仪器_____(填序号),实验过程中应控制温度为_________时收集液溴。
【答案】 液 水 黄绿色 d c Br2+H2O+SO32-=2Br-+SO42-+2H+ ①③⑤⑥⑦ 59℃
【解析】Ⅰ.(1)根据溴的状态以及液溴易挥发分析;
Ⅱ.(2)根据氯气是黄绿色气体分析;
(3)根据氯气、溴的性质分析判断;
(4)根据蒸馏装置选择仪器,根据溴的沸点控制蒸馏时的温度。
Ⅰ.(1)溴在常温下为液态,液溴易挥发,密度大于水,微溶于水,所以保存时通常在盛溴的试剂瓶中加入少量水进行水封。
Ⅱ.(2)氯气与溴离子反应生成溴单质,由于氯气是黄绿色气体,因此当反应完成时,A中液面上方出现黄绿色气体时即可判断步骤①中反应已经结束;
(3)溴检验氧化性,能够与亚硫酸钠反应,因此可以用饱和亚硫酸钠溶液吸收溴,反应的离子方程式为Br2+H2O+SO32-=2Br-+SO42-+2H+,答案选d;溴、氯气都有毒,可用碱液吸收,答案选c;
(4)蒸馏操作的主要仪器是:带铁圈的铁架台,酒精灯,石棉网,蒸馏烧瓶,温度计,冷凝管,牛角管,锥形瓶,所以选择的仪器有①③⑤⑥⑦;蒸馏实验依据的是液体的沸点不同分离物质,所以实验中应控制的关键实验条件为温度,Br2的沸点为58.78℃,则应该控制温度在59℃(或58.8℃)。


科目:高中化学 来源: 题型:
【题目】室温下,有两种溶液:①0.01 mol·L-1 NH3·H2O溶液、②0.01 mol·L-1 NH4Cl溶液,下列操作可以使两种溶液中c(NH4+)都增大的是
A.通入少量HCl气体 B.加入少量NaOH固体
C.加入少量H2O D.适当升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下列四种有关性质的叙述,可能属于金属晶体的是( )
A. 由分子间作用力结合而成,熔点低
B. 固体或熔融后易导电,熔点在1000 ℃左右
C. 由共价键结合成网状结构,熔点高
D. 固体和熔融状态不导电,但溶于水后可能导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有以下物质:①蔗糖 ②熔融的氯化钠 ③二氧化碳 ④硫酸 ⑤铁 ⑥烧碱 ⑦氯气 ⑧漂白粉 (填写编号)
(1)其中能导电的有________
(2)属于非电解质的有______
(3)属于电解质的有________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是

A. 通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B. 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C. 负极反应为2H2O–4e–=O2+4H+,负极区溶液pH降低
D. 当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:
(1)以天然气为原料制H2是合成氨的一条重要的路线。甲烷的部分氧化可得到合成氨的原料气H2,其反应式如下:①CH![]() (g)+1/2O
(g)+1/2O![]() (g)══CO(g)+2H
(g)══CO(g)+2H![]() (g) ΔH1=-35.6kJ·mol
(g) ΔH1=-35.6kJ·mol![]() ,试判断常温下,上述反应能否自发进行:___________(填”能”或”否”)。
,试判断常温下,上述反应能否自发进行:___________(填”能”或”否”)。
有研究认为甲烷部分氧化的机理为:
②CH![]() (g)+2O
(g)+2O![]() (g)=CO2(g)+2H2O(g) ΔH2=-890.3kJ·mol
(g)=CO2(g)+2H2O(g) ΔH2=-890.3kJ·mol![]() ;
;
③CH![]() (g)+CO
(g)+CO![]() (g)=2CO(g)+2H
(g)=2CO(g)+2H![]() (g) ΔH3=+247.3kJ·mol
(g) ΔH3=+247.3kJ·mol![]() ,请结合以上三个反应与条件写出CH4和H2O(g)生成CO和H2的热化学反应方程式:________________________________。
,请结合以上三个反应与条件写出CH4和H2O(g)生成CO和H2的热化学反应方程式:________________________________。
(2)恒温下,向一个2L的密闭容器中充入1 mol N2和2.6 molH2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
c(NH3)/( mol ·/L-1) | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
此条件下,该反应达到化学平衡时,氮气的浓度为_______________。
(3)如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。
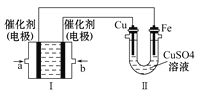
①b处电极上发生的电极反应式是_____________________________。
②电镀结束后,装置Ⅰ中溶液的pH___________(填写“变大”、“变小”或“不变”,下同),装置Ⅱ中Cu![]() 的物质的量浓度___________________。
的物质的量浓度___________________。
③若完全反应后,装置Ⅱ中阴极质量增加12.8g,则装置Ⅰ中理论上消耗甲烷_________L (标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. HClO是弱酸,所以NaClO是弱电解质
B. 0.1 mol·L-1CH3COOH溶液的pH>1,可知CH3COOH溶液中存在CH3COOH![]() CH3COO-+H+
CH3COO-+H+
C. 能导电的物质一定是电解质
D. 弱电解质的电离程度越大,导电能力越强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子或离子中都存在着配位键的是( )
A.NH3、H2O B.NH4+、H3O+ C.N2、HClO D.[Cu(NH3)4]2+、PCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氧磷(化学式:POCl3)常用作半导体掺杂剂及光导纤维原料。氯化水解法生产三氯氧磷的流程如下:

⑴氯化水解法生产三氯氧磷的化学方程式为______。
⑵通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
Ⅰ.取ag产品于锥形瓶中,加入足量NaOH溶液,待完全水解后加稀硝酸至酸性。
Ⅱ.向锥形瓶中加入0.1000 mol·L-1的AgNO3溶液40.00 mL,使Cl-完全沉淀。
Ⅲ.向其中加入2 mL硝基苯,用力摇动,使沉淀表面被有机物覆盖。
Ⅳ.加入指示剂,用cmol·L-1NH4SCN溶液滴定过量Ag+至终点,记下所用体积。
已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12
①滴定选用的指示剂是______(选填字母),滴定终点的现象为______。
a.NH4Fe(SO4)2 b.FeCl2 c.甲基橙 d.淀粉
②实验过程中加入硝基苯的目的是_____________________,如无此操作所测Cl元素含量将会______(填“偏大”、“偏小”或“不变”)
⑶氯化水解法生产三氯氧磷会产生含磷(主要为H3PO4、H3PO3等)废水。在废水中先加入适量漂白粉,再加入生石灰调节pH将磷元素转化为磷酸的钙盐沉淀并回收。
①在沉淀前先加入适量漂白粉的作用是_________________。
②下图是不同条件对磷的沉淀回收率的影响图像。
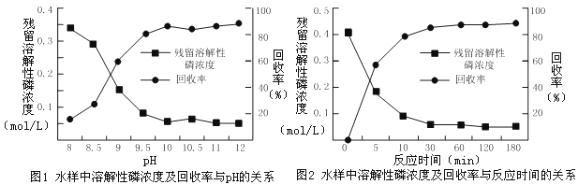
处理该厂废水最合适的工艺条件为______(选填字母)。
a.调节pH=9 b.调节pH=10 c.反应时间30 min d.反应时间120 min
③若处理后的废水中c(PO43-)=4×10-7mol·L-1,溶液中c(Ca2+)=__________mol·L-1。
(已知Ksp[Ca3(PO4)2]=2×10-29)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com