
【题目】三氯氧磷(化学式:POCl3)常用作半导体掺杂剂及光导纤维原料。氯化水解法生产三氯氧磷的流程如下:

⑴氯化水解法生产三氯氧磷的化学方程式为______。
⑵通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
Ⅰ.取ag产品于锥形瓶中,加入足量NaOH溶液,待完全水解后加稀硝酸至酸性。
Ⅱ.向锥形瓶中加入0.1000 mol·L-1的AgNO3溶液40.00 mL,使Cl-完全沉淀。
Ⅲ.向其中加入2 mL硝基苯,用力摇动,使沉淀表面被有机物覆盖。
Ⅳ.加入指示剂,用cmol·L-1NH4SCN溶液滴定过量Ag+至终点,记下所用体积。
已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12
①滴定选用的指示剂是______(选填字母),滴定终点的现象为______。
a.NH4Fe(SO4)2 b.FeCl2 c.甲基橙 d.淀粉
②实验过程中加入硝基苯的目的是_____________________,如无此操作所测Cl元素含量将会______(填“偏大”、“偏小”或“不变”)
⑶氯化水解法生产三氯氧磷会产生含磷(主要为H3PO4、H3PO3等)废水。在废水中先加入适量漂白粉,再加入生石灰调节pH将磷元素转化为磷酸的钙盐沉淀并回收。
①在沉淀前先加入适量漂白粉的作用是_________________。
②下图是不同条件对磷的沉淀回收率的影响图像。
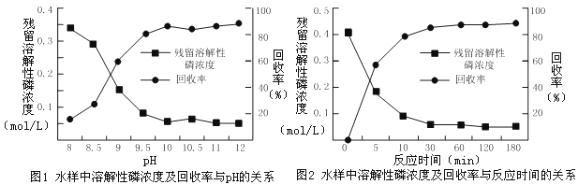
处理该厂废水最合适的工艺条件为______(选填字母)。
a.调节pH=9 b.调节pH=10 c.反应时间30 min d.反应时间120 min
③若处理后的废水中c(PO43-)=4×10-7mol·L-1,溶液中c(Ca2+)=__________mol·L-1。
(已知Ksp[Ca3(PO4)2]=2×10-29)
【答案】 PCl3+H2O+Cl2=POCl3+2HCl b 溶液变为红色,而且半分钟内不褪色 防止在滴加NH4SCN时,将AgCl沉淀转化为AgSCN沉淀 偏小 将废水中的H3PO3氧化为PO43-,使其加入生石灰后转化为磷酸的钙盐 bc 5×10-6
【解析】(1)氯化水解法产物是三氯氧磷和盐酸,结合原子守恒分析;
(2)①当滴定达到终点时NH4SCN过量,Fe3+与SCN-反应溶液变红色,半分钟内不褪色,即可确定滴定终点;②由于AgSCN沉淀的溶解度比AgCl小,可加入硝基苯用力摇动,使AgCl沉淀表面被有机物覆盖,避免在滴加NH4SCN时,将AgCl沉淀转化为AgSCN沉淀;若无此操作,NH4SCN标准液用量偏多;
(3)①在沉淀前先加入适量漂白粉使废水中的H3PO3氧化为PO43-,加入生石灰后能完全转化为磷酸的钙盐,达到较高的回收率;②根据图1、2分析磷的沉淀回收率;③根据Ksp[Ca3(PO4)2]= c3(Ca2+)×c2(PO43-)计算。
(1)氯化水解法是用三氯化磷、氯气与水反应生成三氯氧磷和盐酸,其化学方程式为:PCl3+H2O+Cl2=POCl3+2HCl,故答案为:PCl3+H2O+Cl2=POCl3+2HCl;
(2)①用c molL-1NH4SCN溶液滴定过量Ag+至终点,当滴定达到终点时NH4SCN过量,加NH4Fe(SO4)2作指示剂,Fe3+与SCN-反应溶液会变红色,半分钟内不褪色,即可确定滴定终点;故答案为:b;溶液变为红色,而且半分钟内不褪色;
②已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12,则AgSCN沉淀的溶解度比AgCl小,可加入硝基苯用力摇动,使AgCl沉淀表面被有机物覆盖,避免在滴加NH4SCN时,将AgCl沉淀转化为AgSCN沉淀;若无此操作,NH4SCN与AgCl反应生成AgSCN沉淀,则滴定时消耗的NH4SCN标准液的体积偏多,即银离子的物质的量偏大,则与氯离子反应的银离子的物质的量偏小,所以测得的氯离子的物质的量偏小,故答案为:防止在滴加NH4SCN时,将AgCl沉淀转化为AgSCN沉淀;偏小;
(3)①氯化水解法生产三氯氧磷会产生含磷(主要为H3PO4、H3PO3等)废水,在废水中先加入适量漂白粉,使废水中的H3PO3氧化为PO43-,使其加入生石灰后能完全转化为磷酸的钙盐,达到较高的回收率;故答案为:将废水中的H3PO3氧化为PO43-,使其加入生石灰后转化为磷酸的钙盐;
②根据图1、2可确定pH=10、反应时间30 min时磷的沉淀回收率较高,则处理该厂废水最合适的工艺条件为pH=10、反应时间30 min;故答案为:bc;
③若处理后的废水中c(PO43-)=4×10-7 molL-1,Ksp[Ca3(PO4)2]=c3(Ca2+)×c2(PO43-)=2×10-29,c(Ca2+)=![]() =5×10-6molL-1,故答案为:5×10-6。
=5×10-6molL-1,故答案为:5×10-6。


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案科目:高中化学 来源: 题型:
【题目】查阅资料知:Br2的沸点为58.78℃,密度为3.119gcm﹣3,微溶于水,有毒。
Ⅰ.(1)常温下,单质溴通常呈__态,保存时通常在盛溴的试剂瓶中加入少量__液封。
Ⅱ.工业生产中,海水提取溴常用空气吹出法。其生产流程可用如图表示:
浓缩海水![]() 低浓度溴水
低浓度溴水![]() 含Br﹣的溶液
含Br﹣的溶液![]() 溴的浓溶液→液溴
溴的浓溶液→液溴
某化学实验小组模拟该法设计了如图实验装置(夹持装置略去)从浓缩的海水中提取液溴实验步骤如下:
①关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl2,至反应结束;
②关闭a、c,打开b、d,向A中鼓入足量热空气;
③关闭b,打开a,再通过A向B中通入足量的Cl2;
④将B中所得液体进行蒸馏,收集液溴。
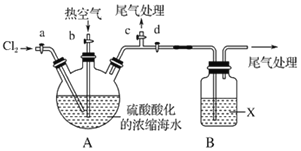
(2)当观察到A中液面上方出现____(实验现象)即可判断步骤①中反应已经结束。
(3)X试剂可以是___,尾气处理选用___(填序号,试剂不重复使用)。
a.H2O b.饱和食盐水 c.NaOH溶液 d.饱和Na2SO3溶液
B中X试剂发生反应的离子方程式为____________________________________。
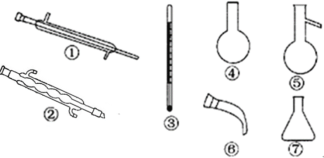
(4)蒸馏时应该选择下列仪器_____(填序号),实验过程中应控制温度为_________时收集液溴。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应:mA(g)+nB(?)![]() xC(g) △H,在不同温度及压强(p1,p2)条件下,反应物A的转化率如图所示,下列判断正确的是
xC(g) △H,在不同温度及压强(p1,p2)条件下,反应物A的转化率如图所示,下列判断正确的是
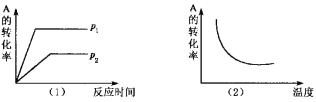
A. △H >0,m+n>x,同时B为非气态
B. △H >0,m+n<x,同时B为气态
C. △H <0,m+n>x,同时B为气态
D. △H <0,m<x,同时B为非气态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物存在如下转化关系:
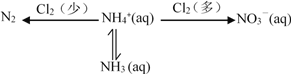
(1)在氨氮废水中通入一定量的氯气,利用产生的HClO可除去废水中含有的游离氨或铵盐。
已知 NH4+ + HClO ![]() NH2Cl + H+ + H2O H = a kJmol-1
NH2Cl + H+ + H2O H = a kJmol-1
2NH2Cl + HClO ![]() N2 + H2O + 3H+ + 3Cl- H = b kJmol-1
N2 + H2O + 3H+ + 3Cl- H = b kJmol-1
则 2NH4+ + 3HClO ![]() N2 + 3H2O + 5H+ + 3Cl- H =______kJmol-1
N2 + 3H2O + 5H+ + 3Cl- H =______kJmol-1
(2)电解法也可除去水中的氨氮,实验室用石墨电极电解一定浓度的(NH4)2SO4与NaCl的酸性混合溶液来模拟。
① 电解时,阳极的电极反应式为________。
② 电解过程中,溶液初始Cl-浓度和pH对氨氮去除速率与能耗(处理一定量氨氮消耗的电能)的影响关系如图1和图2所示。

图1 Cl-浓度对氨氮去除速率、能耗的影响 图2初始pH对氨氮去除速率、能耗的影响
图1中当Cl-浓度较低时、图2中当初始pH达到12时,均出现氨氮去除速率低而能耗高的现象,共同原因是________;图2中,pH为6时处理效果最佳,当pH过低时,处理效果不佳的原因可能是________。
③ 当溶液中Cl-浓度较高时,测得溶液中的NO![]() 浓度会随之增大,可能的原因是________。
浓度会随之增大,可能的原因是________。
(3)某工厂将含NH4+废水的去除与工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分)的去除结合起来,设计了如下方案:
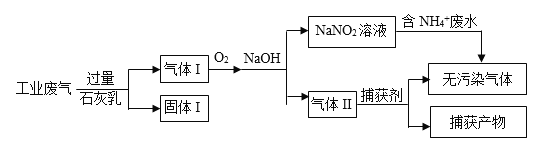
① 固体I的成分为________。
② 为使100L 150 mg/L(浓度均以氮原子计,下同)的含NH4+ 废水达到国家二级排放标准10mg/L,图中通入的氧气在标准状况下的体积至少为________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由丙烯经下列反应可得到F、G两种高分子化合物,它们都是常用材料
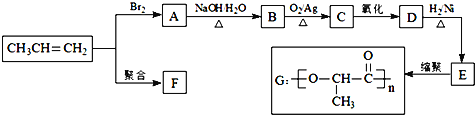
(1)E中官能团的名称_________.
(2)写出D的结构简式_________.
(3)聚合物F的结构简式是____________________.
(4)B转化为C的化学方程式是______________________________.
(5)在一定条件下,两分子E能脱去两分子水形成一种六元环化合物,该化合物的结构简式是_________.
(6)E有多种同分异构体,写出与E含有相同官能团的同分异构体的结构简式_________,其核磁共振氢谱显示为__________组峰,峰面积之比为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置进行实验,下列有关说法正确的是( )
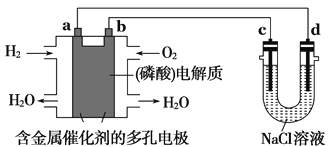
A. 电子流向为:电极a → 电极d →电极c →电极b
B. 电极b发生的电极反应为O2 + 2H2O + 4e- = 4OH-
C. 在电极a参与反应的气体体积在相同状况下与在电极c产生的气体体积为1:1
D. 为了防止大气污染,应在d端的U形管出口连接导管通入到NaOH溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1 CH3COOH溶液所得滴定曲线如图。下列说法不正确的是( )
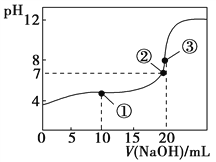
A. 在曲线上任一点均存在:c(Na+)c(OH-) = c(CH3COO-)c(H+)
B. 点①所示溶液中:c(CH3COO-)+2c(OH-) = c(CH3COOH)+2c(H+)
C. 点②所示溶液中:c(Na+) = c(CH3COO-)
D. 点③所示溶液中:c(Na+) > c(OH-) > c(CH3COO-) > c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com