
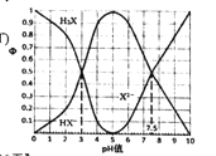
【题目】在25°C时,某二元酸H2X及其钠盐的溶液中,H2X、HX-、 X2-分别在三者中所占的物质的量分数(Φ)随溶液pH变化关系如下图所示,下列叙述不正确的是( )
A.在pH=5 的溶液中,存在 =10-4.5
=10-4.5
B.在pH=7.5的溶液中,存在3c(HX-)=c(Na+)+c(H+)-c(OH-)
C.将相同物质的量的Na2X和NaHX完全溶于水所得溶中液的pH值为7.5
D.等体积等浓度的NaOH溶液与H2X溶液混合,溶液显酸性且存在c(H+)+(H2X)=c(OH-)+c(X2-)
【答案】C
【解析】
如图当pH值为3,c(HX-)=c(H2X),Ka1(H2X)=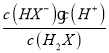 =1.0×10- 3,当pH值为7.5,c(X2- ) = c(HX-),Ka2(H2X)=
=1.0×10- 3,当pH值为7.5,c(X2- ) = c(HX-),Ka2(H2X)= = 1.0×10-7.5, X2-发生两步水解,
= 1.0×10-7.5, X2-发生两步水解,![]() ,
, ![]() 。
。
A. 二元酸H2X存在两步电离,H2X![]() HX-+H+,Ka1=1.0×10- 3,HX-
HX-+H+,Ka1=1.0×10- 3,HX-![]() X2- + H+,Ka2=1.0×10-7.5,
X2- + H+,Ka2=1.0×10-7.5,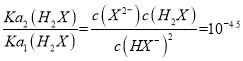 ,A说法正确;
,A说法正确;
B. 在pH=7.5的溶液中,HX-和 X2-物质的量分数相同,c(HX-)= c(X2--),此时溶液中存在电荷守恒c(OH-)+2c(X2--)+c(HX-)=c(Na+)+c(H+),故3c(HX-)=c(Na+)+c(H+)-c(OH-)等式正确,B说法正确;
C. NaHX中HX-的水解能力(![]() =1.0×10-11)小于其电离能力(
=1.0×10-11)小于其电离能力(![]() =1.0×10-7.5),以电离为主。Na2X中X2-的水解能力(
=1.0×10-7.5),以电离为主。Na2X中X2-的水解能力(![]() =1.0×10-6.5)大于NaHX中HX-的电离,故若将相同物质的量的Na2X和NaHX完全溶于水,那么溶液中c(HX-)>c(X2--),此时pH值>7.5,C说法错误;
=1.0×10-6.5)大于NaHX中HX-的电离,故若将相同物质的量的Na2X和NaHX完全溶于水,那么溶液中c(HX-)>c(X2--),此时pH值>7.5,C说法错误;
D. 等体积等浓度的NaOH溶液与H2X溶液混合,二者按照一比一恰好反应完全生成NaHX,其质子守恒为c(H+)+(H2X)=c(OH-)+c(X2-),D说法正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】I.《自然》杂志曾报道我国科学家通过测量SiO2中26Al和10Be两种元素的比例确定“北京人”年龄的研究结果,这种测量方法叫“铝铍测年法”。完成下列填空:
(1)l0Be和9Be_____________(填序号)。
a.是同一种原子 b.具有相同的中子数 c.具有相同的化学性质 d.互为同位素
(2)写出A1(OH)3与NaOH溶液反应的化学方程式:_________________________。
(3)研究表明28A1可以衰变为26Mg,可以比较这两种元素金属性强弱的方法是____________(填序号)。
a.比较Mg(OH)2与A1(OH)3的碱性强弱
b.比较这两种元素的最高正化合价
c.将打磨过表面积相同的镁条和铝片分别和100℃热水作用,并滴入酚酞溶液
d.比较这两种金属的硬度和熔点
II.下表列出了①~⑩10种元素在周期表中的位置。
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑤ | ⑥ | ⑩ | |||||
3 | ① | ③ | ④ | ⑦ | ⑧ | |||
4 | ② | ⑨ |
(1)上述元素中,金属性最强的是(填元素符号,下同)________,③④⑤三种元素的原子半径由大到小的顺序是____________。
(2)上述元素的最高价氧化物对应的水化物中酸性最强的是________(填化学式)
(3)元素⑥的氢化物的电子式为____________,该氢化物与元素⑥的最高价氧化物对应的水化物反应的化学方程式为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是短周期主族元素,且原子序数依次增大。在短周期中A元素原子半径最小,D元素原子半径最大,B的简单氢化物的水溶液呈碱性,C、E同主族,形成的化合物为EC2、EC3。回答下列问题:
(1)E在元素周期表中的位置为_____________________________。
(2)比较B与C简单氢化物的热稳定性:_____> 。(填化学式)
(3)D,C两元素组成的化合物D2C2的电子式为_____________________,D2C2与水反应的化学方程式为 ______________________________________________。
(4)下列事实能说明元素F的非金属性比元素E的非金属性强的是______。
A.元素F形成的单质比元素E形成的单质的熔点低
B.F和E两元素的简单氢化物受热分解,前者的分解温度高
C.F2通入到D2E的溶液中出现浑浊
D.F氢化物的酸性比E氢化物的酸性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知碳碳单键可以旋转,结构简式为 ![]() 的烃,下列说法中正确的是
的烃,下列说法中正确的是
A. 分子中最多有6个碳原子处于同一直线上
B. 该烃苯环上的一氯代物有3种
C. 分子中至少有12个碳原子处于同一平面上
D. 该烃属于苯的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2020年以来,世界多地发生了新冠病毒肺炎,威胁着人们的身体健康。抗击新冠肺炎疫情中,“84”消毒液、双氧水和“一次性口罩”起了非常重要的作用。下列正确的有( )
A.医用口罩中的过滤层所用的材料是熔喷聚丙烯,聚丙烯的结构可表示![]()
B.“84”消毒液的主要有效成分是NaClO,在NaClO固体中含有的化学键只有离子键
C.双氧水的结构式为 H-O-O-H,分子间可形成氢键
D.NaClO的电子式为 ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA是阿伏加德罗常数的值,下列说法正确的是
A. 16.25 g FeCl3水解形成的Fe(OH)3胶体粒子数为0.1NA
B. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
C. pH=1的HCl溶液中,含有0.1NA个H+
D. 0.1mol苯乙烯分子中,含有碳碳双键的数目为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,在盛有稀 H2SO4 的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
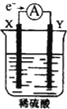
A.外电路的电流方向为:X→外电路→Y
B.若两电极分别为Fe和碳棒,则X为碳棒,Y为Fe
C.X极上发生的是还原反应,Y极上发生的是氧化反应
D.若两电极都是金属,则它们的活动性顺序为X>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某浓度的氨水中存在下列平衡:NH3H2O![]() NH4++OH-,若想增大NH4+的浓度,而不增加OH-的浓度,应采取的措施是( )
NH4++OH-,若想增大NH4+的浓度,而不增加OH-的浓度,应采取的措施是( )
①适当升高温度 ②加入NH4Cl 固体 ③通入NH3 ④加入少量盐酸
A. ①②B. ②③C. ③④D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】开发清洁能源是当今化工研究的一个热点问题。二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用,工业上以CO和H2为原料生产CH3OCH3。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g)CH3OH(g) ΔH1=-99kJ·mol1
②2CH3OH(g)CH3OCH3(g)+H2O(g) ΔH2=-23.5kJ·mol1
③CO(g)+H2O(g)CO2(g)+H2(g) ΔH3=-41.2kJ·mol1
(1)催化反应室中的总反应3CO(g)+3H2(g)CH3OCH3(g)+CO2(g),计算ΔH=_______。反应来自煤的气化。已知该反应的平衡常数表达式为K=![]() ,每生成1mol H2需要吸收131.3kJ的热量。写出该反应的热化学方程式____________。
,每生成1mol H2需要吸收131.3kJ的热量。写出该反应的热化学方程式____________。
(2)在该条件下,若反应①的起始浓度分别为:c(CO)=0.6mol·L1,c(H2)=1.4mol·L1,8min后达到平衡,CO的转化率为50%,则8min内H2的平均反应速率为__________。
(3)在t℃时,反应②的平衡常数为400,此温度下,在1L的密闭容器中加入一定的甲醇,反应到某时刻测得各组分的物质的量浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
c(mol·L1) | 0.46 | 1.0 | 1.0 |
此时刻v正___v逆(填“>”“<”或“=”),平衡时c(CH3OCH3)的物质的量浓度是___。
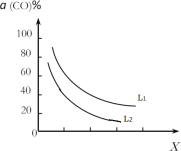
(4)在(1)小题中催化反应室的总反应3CO(g)+3H2(g)CH3OCH3(g)+CO2(g),CO的平衡转化率a(CO)与温度、压强的关系如图所示,图中X代表___(填“温度”或“压强”),且L1___L2(填“>”“<”或“=”)。
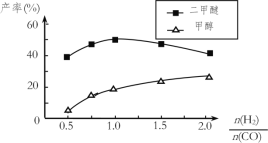
(5)在催化剂的作用下同时进行三个反应,发现随着起始投料比![]() 的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:_____。
的改变,二甲醚和甲醇的产率(产物中的碳原子占起始CO中碳原子的百分率)呈现如图的变化趋势。试解释投料比大于1.0之后二甲醚产率和甲醇产率变化的原因:_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com