
【题目】(1)在某一化学反应中,反应物B的浓度在5s内从2.0mol/L变成0.5mol/L,在这5s 内B的化学反应速率为多少______?
(2)一个5L的容器中,盛入8.0mol某气体反应物,5min后,测得这种气体反应物还剩余 6.8mol,这种反应物的化学反应速率为多少_________?
科目:高中化学 来源: 题型:
【题目】具有抗菌作用的白头翁素衍生物 H 的合成路线如下图所示:

已知:i.RCH2Br![]() R—HC=CH—R′
R—HC=CH—R′
ii.R—HC=CH—R′![]()
![]()
iii.R—HC=CH—R′![]()
 (以上R、R′、R″代表氢、烷基或芳基)
(以上R、R′、R″代表氢、烷基或芳基)
(1)A 属于芳香烃,其名称是_____________。
(2)B 的结构简式是___________________。
(3)由 C 生成 D 的化学方程式是___________________。
(4)由 E 与 I2 在一定条件下反应生成 F 的化学方程式是_____________;此反应同时生成另外一个有机副产物且与 F 互为同分异构体,此有机副产物的结构简式是_________________。
(5)试剂 b 是__________________。
(6)下列说法正确的是______________(选填字母序号)。
a.G 存在顺反异构体
b.由 G 生成 H 的反应是加成反应
c.1 mol G 最多可以与 1 mol H2 发生加成反应
d.1 mol F 或 1 mol H 与足量 NaOH 溶液反应,均消耗 2 molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室采用下图所示装置制备乙酸乙酯。实验结束后,取下盛有饱和碳酸钠溶液的试管,再沿该试管内壁缓缓加入石蕊溶液1毫升,发现石蕊溶液存在于饱和碳酸钠溶液层与乙酸乙酯液层之间(整个过程不振荡试管)。下列有关该实验的描述不正确的是( )
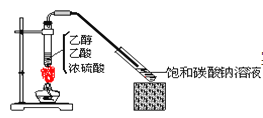
A.制备的乙酸乙酯中混有乙酸和乙醇杂质
B.该实验中浓硫酸的作用是催化和吸水
C.饱和碳酸钠溶液主要作用是降低乙酸乙酯的溶解度及吸收乙醇和乙酸
D.石蕊层为三层,由上而下是蓝、紫、红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图;研究发现在以Fe2O3为主的催化剂上可能发生的反应过程如图.下列说法正确的是 ( )
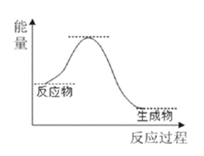

A.NH3催化还原NO为吸热反应
B.过程Ⅰ中NH3断裂非极性键
C.过程Ⅱ中NO为氧化剂,Fe2+为还原剂
D.脱硝的总反应为: 4NH3(g)+4NO(g)+ O2(g) ![]() 4N2(g)+6H2O(g)
4N2(g)+6H2O(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下,将下列各组气体分别充入到容积可变的密闭容器中,充分反应后,体积由大到小的顺序是
①2molNH3和1molHCl,②2molSO2和1molO2,③2molH2S和1molSO2,④2molNO和1molO2,⑤1molH2和1mol Cl2
A. ②>④>⑤>①>③
B. ②>⑤>④>①>③
C. ④>②=⑤>③>①
D. ④=⑤>②>③>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知草酸是二元弱酸,0.2 mol·L-1NaHC2O4 溶液显酸性,关于 NaHC2O4 溶液中离子浓度关系的叙述不正确的是
A.c(Na+)>c(![]() )>c(
)>c(![]() )>c(H2C2O4)
)>c(H2C2O4)
B.c(Na+)=c(![]() )+c(
)+c(![]() )+c(H2C2O4)
)+c(H2C2O4)
C.c(Na+)+c(H+)=c(![]() )+c(
)+c(![]() )+c(OH-)
)+c(OH-)
D.c(H+)+c(H2C2O4)=c(![]() )+c(OH-)
)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是含某元素的A→G的七种物质分别与X、Y、Z反应的价类二维图。其中X是一种强碱;G为正盐;通常条件下,Z是无色液体;D的相对分子质量比C小16,各物质转化关系如图所示。下列说法正确的是![]()
![]()

A.该元素在周期表中位于第二周期第V族
B.上述转化中发生5个氧化还原反应
C.稳定性:气态F<气态Z
D.A、B、X、G四种物质分别含有离子键和共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,将0.1 mol Fe(NO3)3和2 mol HCl溶于水得到2L混合溶液,然后向该溶液中投入m g铁粉,充分反应后,滴加KSCN溶液不变红色。下列有关说法正确的是
A.由于氧化性:Fe3+>H+,故首先发生的反应是Fe+2Fe3+=3Fe2+
B.充分反应后,共消耗56 g铁
C.m=28时,溶液剩余0.9 mol H+
D.当加入16.8 g铁粉时,可生成标准状况下6.72 L气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,盐酸只作氧化剂的是( )
A.Zn+2HCl = ZnCl2+H2↑B.MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
C.Cl2+H2O = H++Cl–+HClOD.CaCO3+2HCl=CaCl2+CO2↑+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com