
【题目】下列说法正确的是
A. 元素的种类由最外层电子数决定
B. 化学键是存在于分子、原子和离子间的作用力
C. 原子的种类由原子核内质子数与中子数共同决定
D. 化学反应速率可以决定反应的限度
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是:
A. 在一个氧化还原反应中,氧化剂的氧化性强于氧化产物
B. 在一个氧化还原反应中,还原产物的还原性弱于还原剂
C. amolH2SO4中,含有b个氧原子,则阿伏加德罗常数可以表示为b/4a/mol
D. 配制0.05mol/LNa2CO3溶液90mL,需Na2CO3固体5.3g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的值为NA,下列说法中正确的是
A. 17g甲基(—14CH3)所含中子数为9NA
B.常温常压下,2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA
C.0.1molC5H12分子中含有的C-C键数为0.5NA
D.标准状况下,2.24L辛烷在氧气中完全燃烧生成CO2分子数为0.8 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国劳伦斯·利弗莫尔国家实验室2006年成功合成了118号超重元素,并观察到其存在了不到1毫秒时间。该元素符号为:Uuo,质量数为293,以下叙述不正确的是
A. 该元素原子核外含有118个电子,核内有175个中子
B. 该元素属于第七周期
C. 该元素一定是一种金属元素
D. 该元素位于零族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用粗盐(含Ca2+、Mg2+、SO42-等杂质)为主要原料采用“侯氏制碱法” 生产纯碱和化肥NH4Cl,工艺流程如下图所示.下列有关说法正确的是
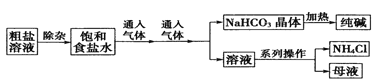
A. 对粗盐溶液除杂可依次加入NaOH、Na2CO3、BaCl2,再加入盐酸调节溶液pH
B. 饱和食盐水中先通入的气体为CO2
C. 流程图中的系列操作中一定需要玻璃棒
D. 如图所示装置可以比较Na2CO3和NaHCO3晶体的热稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质的水溶液中存在电离平衡.
(1)醋酸是常见的弱酸.
① 醋酸在水溶液中的电离方程式为________________________________________________;
②下列方法中,可以使醋酸稀溶液中CH3COOH电离程度增大的是_________(填字母序号) 。
A.滴加少量浓盐酸 B.微热溶液 C.加水稀释 D.加入少量醋酸钠晶体
(2)用0.1 molL-1 NaOH溶液分别滴定体积均为20.00 mL、浓度均为0.1 molL-1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。

① 滴定醋酸的曲线是______________(填“I”或“Ⅱ”);
② 滴定开始前,三种溶液中由水电离出的c(H+)最大的是_____________________;
③ V1和V2的关系:V1 _____ V2(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关晶体的下列说法中正确的是( )
A.晶体中分子间作用力越大,分子越稳定
B.冰熔化时水分子中共价键发生断裂
C.原子晶体中共价键越强,熔点越高
D.氯化钠熔化时离子键未被破坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如果ag某气体中含有的分子数为b,则cg该气体的物质的量是( )
A. bc/(aNA)mol B. ac/(bNA)mol C. ab/(cNA)mol D. b/(acNA)mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】计算后填空:
(1)在标准状况下,448 mL某气体的质量为0.64 g,这种气体的相对分子质量为________。
(2)某氯化铁与氯化钠的混合液,已知c(Fe3+)=0.2 mol·L-1,c(Cl-)=1 mol·L-1。则c(Na+)为_____________。
(3)19 g某二价金属的氯化物RCl2中含有0.4 mol的Cl-,则R的相对原子质量为__________。
(4)V L Fe2(SO4)3溶液中含Fe3+ m g,则溶液中SO42-的物质的量浓度为___________mol·L-1。
(5)在无土栽培中,配制1 L含5 mol NH4Cl、1.6 mol KCl、2.4 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需KCl、NH4Cl的物质的量分别为________、________。
(6)如图所示, 分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的1/4)、H2和O2的混合气体,在标准状况下,若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来H2、O2的体积之比可能为_________________。
分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的1/4)、H2和O2的混合气体,在标准状况下,若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来H2、O2的体积之比可能为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com