
【题目】按要求填空
催化剂能改变化学反应的速率,原因是改变化学反应的路径.某同学在实验中发现,向2mL5%H2O2溶液中分别滴入FeCl3和FeCl2溶液,都立即产生大量气泡;向反应后的溶液中滴入几滴KSCN溶液,溶液均变为红色.查阅资料知:FeCl3在H2O2分解中发生如下反应:
①2Fe3++H2O2═2Fe2++2H++O2↑ ②2Fe2++2H++H2O2═2Fe3++2H2O
(1)在反应①中Fe3+作;在反应②中Fe3+是 . 有同学认为Fe2+也可作H2O2分解的催化剂,你认为该观点是否正确,并简述理由
.
(2)反应2MnO4﹣+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O,加入少许MnSO4固体能明显观察到溶液紫色褪去时间变短.在试管中加入4mL0.01mol/LKMnO4酸性溶液和2mL0.1mol/LH2C2O4溶液,实验初始阶段时间﹣速率图象合理的是图1中的(填序号). 
(3)某反应体系中存在A、B、C、D四种物质,反应过程中各物质的物质的量变化如图2所示,请写出该反应的化学方程式 .
(4)焙烧明矾产生的SO2可用于制硫酸.已知25℃、101kPa时:
2SO2(g)+O2(g)═2SO3(g)△H1=﹣197kJmol﹣1;
H2O(g)═H2O(l)△H2=﹣44kJmol﹣1;
2SO2(g)+O2(g)+2H2O(g)═2H2SO4(l)△H3=﹣545kJmol﹣1 .
则SO3(g)与H2O(l)反应的热化学方程式是 .
【答案】
(1)氧化剂;氧化产物;正确;Fe2+先被H2O2氧化:2Fe2++2H++H2O2═2Fe3++2H2O,再发生反应:2Fe3++H2O2═2Fe2++2H++O2↑,总反应为:2H2O2 ![]() 2H2O+O2↑,在反应前后Fe2+性质和质量不变,Fe2+作H2O2分解的催化剂
2H2O+O2↑,在反应前后Fe2+性质和质量不变,Fe2+作H2O2分解的催化剂
(2)B
(3)2C?3A+B
(4)SO3(g)+H2O(l)=H2SO4(l)△H=﹣130kJ/mol
【解析】解:(1)Fe3+化合价降低,得到电子做氧化剂,Fe2+化合价升高被氧化得到Fe3+ , Fe3+是氧化产物;Fe2+先被H2O2氧化:2Fe2++2H++H2O2═2Fe3++2H2O,再发生反应:2Fe3++H2O2═2Fe2++2H++O2↑,总反应为:2H2O2 ![]() 2H2O+O2↑,在反应前后Fe2+性质和质量不变,Fe2+作H2O2分解的催化剂,
2H2O+O2↑,在反应前后Fe2+性质和质量不变,Fe2+作H2O2分解的催化剂,
所以答案是:氧化剂;氧化产物;正确;Fe2+先被H2O2氧化:2Fe2++2H++H2O2═2Fe3++2H2O,再发生反应:2Fe3++H2O2═2Fe2++2H++O2↑,总反应为:2H2O2 ![]() 2H2O+O2↑,在反应前后Fe2+性质和质量不变,Fe2+作H2O2分解的催化剂;
2H2O+O2↑,在反应前后Fe2+性质和质量不变,Fe2+作H2O2分解的催化剂;
(2.)加入少许MnSO4固体能明显观察到溶液紫色褪去时间变,说明Mn2+对该反应有催化作用,则实验开始反应速率慢,当生成的Mn2+越来越多,反应速率加快,只有B符合先慢后快,
所以答案是:B;
(3.)反应物物质的量减少,生成物物质的量增加,最终各物质的量不再变化,该反应是可逆反应,则C是反应物,A、B是生成物,D一直没变,没有参加反应,根据相同时间A、B、C变化量之比为4:6:2,则各物质计量数之比为2:3:1,方程式为2C3A+B,
所以答案是:2C3A+B;
(4.)2SO2(g)+O2(g)=2SO3(g)△H1=一197kJ/mol ①
H2O (g)=H2O(1)△H2=﹣44kJ/mol ②
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)△H3=一545kJ/mol③
利用盖斯定律:(③﹣①﹣②×2)× ![]() 得SO3 (g)+H2O(l)=H2SO4(l)△H=﹣130kJ/mol,所以答案是:SO3(g)+H2O(l)=H2SO4(l)△H=﹣130kJ/mol.
得SO3 (g)+H2O(l)=H2SO4(l)△H=﹣130kJ/mol,所以答案是:SO3(g)+H2O(l)=H2SO4(l)△H=﹣130kJ/mol.


科目:高中化学 来源: 题型:
【题目】1902年德国化学家哈伯研究出合成氨的方法.
(1)某温度时,N2与H2反应(可逆反应)过程中的能量变化如图1所示. 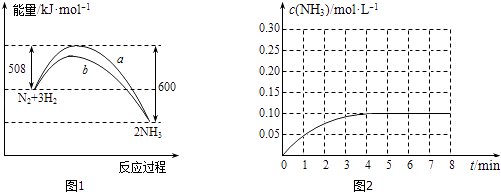
①写出合成氨的热化学方程式 .
②下列叙述正确的是 .
A.b曲线是加入催化剂时的能量变化曲线
B.在密闭容器中加入28gN2、6gH2 , 充分反应放出的热量小于92kJ
C.由图可知,断开1molN≡N键与3molH﹣H键吸收的能量和小于形成6molN﹣氮氢键所放出的能量
D.反应物的总能量低于生成物的能量
(2)在一容积为4L的密闭容器中,加入0.4molN2和1.2molH2 , 在一定条件下发生反应,反应中NH3的物质的量浓度变化情况如图2所示.据图计算从反应开始到平衡时,平均反应速率(H2)为mol/(Lmin),平衡时,c(N2)为 .
(3)哈伯因证实N2、H2在固体催化剂(Fe)表面吸附和解吸以合成氨的过程而获诺贝尔奖.若用 ![]() 分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用如图表示.吸附后,能量状态最高的是(填字母序号).
分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用如图表示.吸附后,能量状态最高的是(填字母序号). 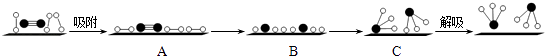
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于铁及其化合物的说法正确的是( )
A. 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红,可以检验Fe(NO3)2晶体是否已氧化变质
B. 浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体
C. 1 mol FeI2与足量氯气反应时转移的电子数为2NA
D. 水溶液中Fe2+、H+、SO![]() 、ClO-不能大量共存
、ClO-不能大量共存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017 年世界地球日我国的主题为“节约集约利用资源,倡导绿色简约生活”。下列做法应提倡的是( )
A. 夏天设定空调温度尽可能的低 B. 推广使用一次性塑料袋和纸巾
C. 少开私家车多乘公共交通工具 D. 对商品进行豪华包装促进销售
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S水溶液中存在电离平衡H2S![]() H++HS-和HS-
H++HS-和HS-![]() H++S2-。若向H2S溶液中 ( )
H++S2-。若向H2S溶液中 ( )
A. 加水,平衡向右移动,溶液中氢离子浓度增大
B. 通入过量SO2气体,平衡向左移动,溶液pH值增大
C. 滴加新制氯水,溶液pH值减小
D. 加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现代以石油化工为基础的三大合成材料是
①合成氨 ②塑料 ③医药 ④合成橡胶 ⑤合成尿素 ⑥合成纤维 ⑦合成洗涤剂
A.①③⑤B.②④⑥C.②④⑦D.④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列仪器:①烧杯;②蒸发皿;③平底烧瓶;④试管;⑤坩埚;⑥锥形瓶。其中可以用酒精灯直接加热的仪器是
A. ①②④⑤⑥ B. ②④⑤ C. ①③⑥ D. ④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com