
【题目】铝制品具有较强的抗腐蚀性能,主要是因为
A. 铝具有银白色的金属光泽B. 铝表面形成致密的氧化物薄膜
C. 铝不与碱反应D. 铝不与酸反应
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】右图表示在某溶液中滴加Ba(OH)2 溶液时,沉淀的物质的量随Ba(OH)2 的物质的量的变化关系。该溶液的成分可能是
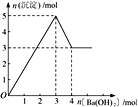
A. MgSO4 B. Al2 (SO4 )3 C. Fe2 (SO4 )3 D. NaAlO2
【答案】B
【解析】A、氢氧化镁不溶于氢氧化钡溶液,沉淀量达最大后,再加氢氧化钡溶液,沉淀量不变,A错误;B、由图可知溶解氢氧化铝需要1mol氢氧化钡,由Al(OH)3+OH-===AlO2-+2H2O可知沉淀中Al(OH)3为2mol,故Al2(SO4)3为1mol,加入3mol氢氧化钡,可以生成硫酸钡3mol,n(Al3+):n(OH-)=2mol:6mol=1:3,发生反应Al3++3OH-===Al(OH)3↓,可以得到2molAl(OH)3,沉淀为3mol+2mol=5mol,B正确;C、硫酸铁与氢氧化钡溶液反应生成氢氧化铁,氢氧化铁不溶于氢氧化钡,则沉淀量达最大后,再加氢氧化钡溶液,沉淀的量不变,与图象不一致,C错误;D、偏铝酸钠与氢氧化钡不反应,不能产生沉淀,D错误;答案选B。
点睛:本题以图象为载体考查镁铝化合物的性质,明确发生的化学反应是解答的关键,反应发生的先后顺序是学生解答中的难点,注意图象比例关系,注意氢氧化铝两性特点。
【题型】单选题
【结束】
15
【题目】如图所示是向MgCl2和AlCl3的混合溶液中加入NaOH溶液和盐酸时沉淀的物质的量y mol与加入NaOH溶液和盐酸的体积x mL的关系图,根据图示判断,下列结论中不正确的是
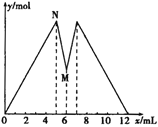
A. N点时溶液中的溶质只有NaCl
B. 原混合溶液中c (MgCl2)∶c (AlCl3)=1∶2
C. c (NaOH)=c (HCl)
D. M点之前加入的是NaOH溶液,M点之后加入的是盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A图是课本中“四种基本反应类型与氧化还原反应的关系”图,A图中用I~IV阴影部分表示反应所属的区域正确的是
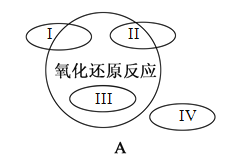
A. 粗硅提纯:Si(粗)+3HCl![]() SiHCl3+H2 所属区域可能是I或II
SiHCl3+H2 所属区域可能是I或II
B. 金属钠在空气中燃烧:2 Na + O2 ![]() Na2O2 所属的区域一定是III
Na2O2 所属的区域一定是III
C. 实验室制取氯气:4HCl(浓)+MnO2![]() MnCl2+Cl2↑+2H2O所属的区域可能是III
MnCl2+Cl2↑+2H2O所属的区域可能是III
D. 土法制碱:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓ 所属的区域一定是IV
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫和氮的氧化物是大气的主要污染物,防止和治理其对环境的污染是当前环保工作的重要研究内容之一.
(1)一定条件下,发生反应2SO2(g)+O2(g)2SO3(g),向2L密闭容器中通入2mol SO2(g)、1mol O2(g)和0.2mol SO3(g),2min后反应达到平衡时,测得SO2的物质的量为1mol,则该可逆反应的平衡常数K=;恒温下,若往容器中再加入2mol SO2(g),则重新达到平衡时SO2的总转化率 0%(填“>”、“<”或“=”).
(2)在一密闭容器中发生反应2NO22NO+O2△H>0,反应过程中NO2的浓度随时间变化的情况如图所示.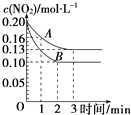
请回答:
①依曲线A,反应在前3min内氧气的平均反应速率为 .
②若曲线A、B分别表示的是该反应在某不同条件下的反应情况,则此条件可能是(填“浓度”、“压强”、“温度”或“催化剂”).
(3)一定温度下,在密闭容器中N2O5可发生下列反应:
①2N2O5(g)4NO2(g)+O2(g)
②2NO2(g)2NO(g)+O2(g)
若达平衡时,c(NO2)=0.4molL﹣1 , c(O2)=1.3molL﹣1 , 则反应②中NO2的转化率为 , N2O5(g)的起始浓度应不低于 molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1000ml某无色待测液中除含有0.2molL﹣1的Na+外,还可能含有下列离子中的一种或多种:
阳离子 | K+、NH4+、Fe3+、Ba2+ |
阴离子 | Cl﹣、CO32﹣、HCO3﹣、SO42﹣ |
现进行如下实验操作(所加试剂均过量):(已知:NH4++OH﹣(浓)=NH3↑+H2O)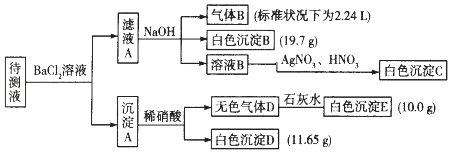
(1)原溶液中肯定存在的离子是(除Na+) , 肯定不存在的离子是 .
(2)写出生成白色沉淀B的离子方程式: . 写出沉淀A溶于稀硝酸的离子方程式: .
(3)将滤液A和沉淀A分开的操作是过滤,洗涤.洗涤的操作是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
A.30 g乙烷中所含的极性共价键数为7NA
B.标准状况下,22.4 L N2和CO2混合气体所含的分子数为2NA
C.1 L浓度为1 molL﹣1的 H2O2水溶液中含有的氧原子数为2NA
D.MnO2和浓盐酸反应生成1 mol氯气时,转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氯化亚铁的熔点674℃、沸点1023℃;三氯化铁在300℃以上易升华,易溶于水并且有强烈的吸水性.在500℃条件下氯化亚铁与氧气可能发生多种反应,反应之一为:12FeCl2+3O2 ![]() 2Fe2O3+8FeCl3 . 某研究小组选用以下装置(夹持装置省略,装置可重复选用)进行反应的探究.回答下列问题:
2Fe2O3+8FeCl3 . 某研究小组选用以下装置(夹持装置省略,装置可重复选用)进行反应的探究.回答下列问题: 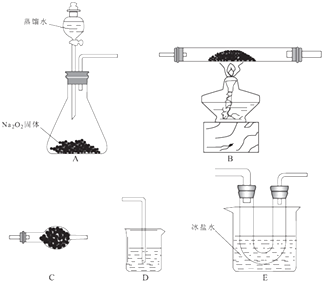
(1)装置的合理连接顺序为A、、D,其中E装置U形管左边设计为粗导管的目的是 .
(2)A装置中发生反应的化学方程式为 .
(3)反应过程发现,装置B中除生成红棕色固体外,还观察到黄绿色气体,生成该气体的化学方程式为 .
(4)待B中充分反应后,停止加热后,还需持续通氧气至 .
(5)设计实验: ①利用E装置U形管里的固体验证Fe(OH)3是弱碱: .
②测定装置B的残留固体中铁元素的质量分数: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应Na2CO3+2HCl=2NaCl+H2O + CO2↑的离子方程式是
A. CO32-+2H+ = H2O+CO2↑B. CO32-+H+=H2O+CO2↑
C. CO32-+2HCl=2Cl-+H2O+CO2↑D. Na2CO3+2H+=2Na++H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)下列物质中:①能导电的是________(填代号,以下同);
②属于电解质的是____________;
③属于非电解质的是____________。
A.NaOH溶液 B.Cu C.液态HCl D.蔗糖溶液
E.液氯 F.氨水 G.胆矾晶体 H.无水乙醇
(2)若将0.2mol钠、镁、铝分别投入到100mL1mol·L-1的盐酸中,在标准状况下,产生氢气体积之比是_____________。
(3)取等质量的铁硅合金样品两份,分别投入到足量的稀盐酸和足量的稀氢氧化钠溶液中,充分反应后,收集到等量的氢气,则原合金样品中铁和硅的物质的量之比为______________________。
(4)向盛有10mL1mol·L-1NH4Al(SO4)2溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:
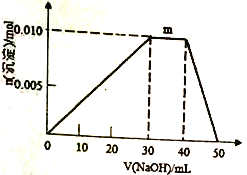
①写出m点反应的离子方程式____________________________________。
②若NH4Al(SO4)2溶液改加20mL1.2mol/LBa(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com