
ΓΨΧβΡΩΓΩ25oC ±Θ§≈®Ε»ΨυΈΣ0.1 molΓΛL®C1ΒΡΦΗ÷÷»ή“ΚΒΡpH»γœ¬ΘΚ
»ή“Κ | ΔΌCH3COONa»ή“Κ | ΔΎNaHCO3»ή“Κ | ΔέCH3COONH4»ή“Κ |
pH | 8.88 | 8.33 | 7.00 |
œ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «
A.ΔΌ÷–Θ§ cΘ®Na+Θ© ΘΫ cΘ®CH3COO®CΘ© ΘΪ cΘ® CH3COOHΘ©
B.”…ΔΌΔΎΩ…÷ΣΘ§CH3COO®CΒΡΥ°Ϋβ≥ΧΕ»¥σ”Ύ![]() ΒΡΥ°Ϋβ≥ΧΕ»
ΒΡΥ°Ϋβ≥ΧΕ»
C.Δέ÷–Θ§cΘ®CH3COO®CΘ© ΘΫ cΘ®NH4+Θ© ΘΦ 0.1 molΓΛL®C1
D.ΆΤ≤β25oCΘ§0.1 molΓΛL®C1 NH4HCO3»ή“ΚΒΡpH ΘΦ8.33
ΓΨ¥πΑΗΓΩB
ΓΨΫβΈωΓΩ
A. CH3COO-ΈΣ»θΥαΗυάκΉ”Θ§‘Ύ»ή“Κ÷–Υ°Ϋβ…ζ≥…¥ΉΥαΘ§ΗυΨί‘ΣΥΊ ΊΚψΘ§ΔΌ÷–Θ§ cΘ®Na+Θ©ΘΫcΘ®CH3COO®CΘ©ΘΪcΘ® CH3COOHΘ©ΘΜ
B.¥ΉΥαΒΡΥα–‘¥σ”ΎΧΦΥαΘ§Ι CH3COO®CΒΡΥ°Ϋβ≥ΧΕ»–Γ”Ύ![]() ΒΡΥ°Ϋβ≥ΧΕ»ΘΜ
ΒΡΥ°Ϋβ≥ΧΕ»ΘΜ
C. CH3COONH4»ή“Κ≥ ÷––‘Θ§CH3COO-ΓΔNH4+ΒΡΥ°Ϋβ≥ΧΕ»œύΆ§Θ§Ι Δέ÷–Θ§cΘ®CH3COO®CΘ© ΘΫ cΘ®NH4+Θ©ΘΦ0.1 molΓΛL®C1ΘΜ
D. NH4+ΒΡΥ°Ϋβœ‘Υα–‘Θ§Ι 0.1 molΓΛL®C1 NH4HCO3»ή“ΚΒΡpH ΘΦ8.33ΘΜ
¥πΑΗ―ΓBΓΘ


 ΚΘΒμΜΤΗ‘Οϊ ΠΒΦΚΫœΒΝ–¥πΑΗ
ΚΘΒμΜΤΗ‘Οϊ ΠΒΦΚΫœΒΝ–¥πΑΗ Τ’Ά®ΗΏ÷–Ά§≤ΫΝΖœΑ≤αœΒΝ–¥πΑΗ
Τ’Ά®ΗΏ÷–Ά§≤ΫΝΖœΑ≤αœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΟή±’ΚψΈ¬»ίΤς÷–Ϋχ––œ¬Ν–Ζ¥”ΠΘΚaA(g)![]() bB(g)Θ§Ζ¥”Π¥οΒΫΤΫΚβΉ¥Χ§ΚσΘ§ΫΪ»ίΤς»ίΜΐ‘ω¥σ1±ΕΘ§Β±Ζ¥”Π¥οΒΫ–¬ΒΡΤΫΚβΉ¥Χ§ ±Θ§Ζ¥”ΠΈοAΒΡ≈®Ε» «‘≠ά¥ΒΡ46%Θ§‘ρœ¬Ν––π ω’ΐ»ΖΒΡ «Θ® Θ©
bB(g)Θ§Ζ¥”Π¥οΒΫΤΫΚβΉ¥Χ§ΚσΘ§ΫΪ»ίΤς»ίΜΐ‘ω¥σ1±ΕΘ§Β±Ζ¥”Π¥οΒΫ–¬ΒΡΤΫΚβΉ¥Χ§ ±Θ§Ζ¥”ΠΈοAΒΡ≈®Ε» «‘≠ά¥ΒΡ46%Θ§‘ρœ¬Ν––π ω’ΐ»ΖΒΡ «Θ® Θ©
A.Μ·―ßΦΤΝΩ ΐa>b
B.»ίΤς»ίΜΐ‘ω¥σΘ§ΤΫΚβœρΡφΖ¥”ΠΖΫœρ“ΤΕ·
C.»ίΤς»ίΜΐ‘ω¥σΘ§…ζ≥…ΈοBΒΡ÷ ΝΩΖ÷ ΐ‘ω¥σ
D.ΗΟΖ¥”ΠΒΡ’ΐΖ¥”ΠΖ≈≥ω»»ΝΩ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΜΖ÷°ΦδΙ≤”Ο“ΜΗωΧΦ‘≠Ή”ΒΡΜ·ΚœΈο≥ΤΈΣ¬ίΜΖΜ·ΚœΈοΘ§¬ί[2Θ§2]ΈλΆιΘ®![]() Θ© «ΉνΦρΒΞΒΡ“Μ÷÷ΓΘœ¬Ν–ΙΊ”ΎΗΟΜ·ΚœΈοΒΡΥΒΖ®≤Μ’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
Θ© «ΉνΦρΒΞΒΡ“Μ÷÷ΓΘœ¬Ν–ΙΊ”ΎΗΟΜ·ΚœΈοΒΡΥΒΖ®≤Μ’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
A.”κΜΖΈλœ©ΜΞΈΣΆ§Ζ÷“λΙΙΧε
B.Ε଻¥ζΈο≥§ΙΐΝΫ÷÷
C.Υυ”–ΧΦ‘≠Ή”Ψυ¥ΠΆ§“ΜΤΫΟφ
D.1mol¬ί[2Θ§2]ΈλΆι≥δΖ÷»Φ…’–η“Σ7molO2
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΕ‘œ¬Ν–Ιΐ≥ΧΒΡΜ·―ß”Ο”ο±μ ω’ΐ»ΖΒΡ «
A.Α―ΡΤΦ”»κΥ°÷–Θ§”–ΤχΧε…ζ≥…ΘΚ2Na + H2O = Na2OΘΪH2Γϋ
B.”ΟœΓΝρΥαΉωΒΦΒγ Β―ιΘ§ΒΤ≈ίΖΔΙβΘΚ H2O![]() H+ΘΪOH-
H+ΘΪOH-
C.œρAl2Θ®SO4Θ©3»ή“Κ÷–ΒΈΦ”Α±Υ°Θ§…ζ≥…ΑΉ…Ϊ≥ΝΒμΘΚAl3+ + 3OH- =AlΘ®OHΘ©3Γΐ
D.”ΟΒγΉ” Ϋ±μ ΨNaClΒΡ–Έ≥…Ιΐ≥ΧΘΚ![]()
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΘ®1Θ©Α¥»γΆΦΥυ Ψ≤ΌΉςΘ§≥δΖ÷Ζ¥”ΠΚσΘΚ

ΔΌΔώ÷–ΖΔ…ζΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ_____________________________________________ΘΜ
ΔΎΔρ÷–Ά≠ΥΩ…œΙέ≤λΒΫΒΡœ÷œσ «________________________________________________ΘΜ
ΔέΫαΚœΔώΓΔΔρ Β―ιœ÷œσΩ…÷ΣFe2ΘΪΓΔCu2ΘΪΓΔAgΘΪΒΡ―θΜ·–‘”…«ΩΒΫ»θΒΡΥ≥–ρΈΣ______________________ΓΘ
Θ®2Θ©Ρ≥“ΜΖ¥”ΠΧεœΒ÷–”–Ζ¥”ΠΈοΚΆ…ζ≥…ΈοΙ≤5÷÷Έο÷ ΘΚSΓΔH2SΓΔHNO3ΓΔNOΓΔH2OΓΘΗΟΖ¥”ΠΈο÷–ΜΙ‘≠≤ζΈο «____________ΘΜ»τΖ¥”ΠΖΫ≥Χ Ϋ÷–ΉΣ“ΤΝΥ0.3 molΒγΉ”Θ§‘ρ―θΜ·≤ζΈοΒΡ÷ ΝΩ «________gΓΘ
Θ®3Θ©ΫΪ…ΌΝΩCl2Ά®»κFeBr2ΒΡ»ή“Κ÷–Θ§Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ2Fe2ΘΪΘΪCl2===2Fe3ΘΪΘΪ2ClΘ≠Θ§’βΗω ¬ ΒΥΒΟςΨΏ”–ΜΙ‘≠–‘ΒΡΝΘΉ”ΜΙ‘≠–‘«Ω»θΈΣ_________________________________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ»γΆΦΥυ ΨΉΑ÷ΟΘ§ΝΫΗωœύΆ§ΒΡ≤ΘΝßΙή÷– Δ¬ζNaClœΓ»ή“ΚΘ®ΒΈ”–Ζ”ΧΣΘ©Θ§aΓΔbΈΣΕύΩΉ ·ΡΪΒγΦΪΓΘ±’ΚœS1“ΜΕΈ ±ΦδΚσΘ§aΗΫΫϋ»ή“Κ÷πΫΞ±δΚλΘΜΕœΩΣS1Θ§±’ΚœS2Θ§ΒγΝς±μ÷Η’κΖΔ…ζΤΪΉΣΓΘ
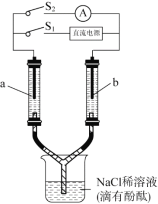
œ¬Ν–Ζ÷Έω≤Μ’ΐ»ΖΒΡ «
A.±’ΚœS1 ±Θ§aΗΫΫϋΒΡΚλ…Ϊ÷πΫΞœρœ¬ά©…Δ
B.±’ΚœS1 ±Θ§ aΗΫΫϋ“ΚΟφ±»bΗΫΫϋΒΡΒΆ
C.ΕœΩΣS1ΓΔ±’ΚœS2 ±Θ§bΗΫΫϋΜΤ¬Χ…Ϊ±δ«≥
D.ΕœΩΣS1ΓΔ±’ΚœS2 ±Θ§a…œΖΔ…ζΖ¥”ΠΘΚH2 2e- = 2H+
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘Ύ“ΜΕ®ΧθΦΰœ¬Θ§Οή±’»ίΤς÷–ΖΔ…ζΖ¥”ΠΘΚA(g)ΘΪ3B(g) ![]() 2C(g)Θ§œ¬Ν–”–ΙΊΥΒΖ®’ΐ»ΖΒΡ «
2C(g)Θ§œ¬Ν–”–ΙΊΥΒΖ®’ΐ»ΖΒΡ «
A.»τΦ”»κ¥ΏΜ·ΦΝΘ§‘ρΖ¥”ΠΒΡΓςH ‘ω¥σ
B.Φ”―Ι ±Θ§ΤΫΚβœρ’ΐΖ¥”ΠΖΫœρ“ΤΕ·Θ§Ζ¥”ΠΒΡΤΫΚβ≥Θ ΐ‘ω¥σ
C.»τΖ¥”ΠΈ¬Ε»…ΐΗΏΘ§‘ρΜνΜ·Ζ÷Ή”ΒΡΑΌΖ÷ ΐ‘ω¥σΘ§Ζ¥”ΠΥΌ¬ ‘ω¥σ
D.»τΒΆΈ¬ ±Θ§ΗΟΖ¥”ΠΈΣ’ΐœρΉ‘ΖΔΫχ––Θ§‘ρΓςHΘΨ0
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥«ΩΥα–‘»ή“ΚX÷–ΫωΚ§”–H+ΓΔNH4ΘΪΓΔAl3ΘΪΓΔBa2+ΓΔFe2ΘΪΓΔFe3ΘΪΓΔCO32-ΓΔSO32-ΓΔSO42-ΓΔCl-ΓΔNO3-÷–ΒΡ“Μ÷÷ΜρΦΗ÷÷(Κω¬‘Υ°ΒΡΒγάκΚΆάκΉ”ΒΡΥ°Ϋβ)Θ§»ΓΗΟ»ή“ΚΫχ––Ν§–χ Β―ιΘ§ Β―ιΙΐ≥Χ»γœ¬ΘΚ

œ¬Ν–”–ΙΊΆΤΕœΚœάμΒΡ «
A. ΗυΨί…œ ωΝ§–χ Β―ι≤ΜΡή»ΖΕ®»ή“ΚX÷– «ΖώΚ§”–Fe3ΘΪ
B. ≥ΝΒμHΈΣAl(OH)3ΓΔBaCO3ΒΡΜλΚœΈο
C. »ή“Κ÷–“ΜΕ®Κ§”–H+ΓΔAl3ΘΪΓΔNH4ΘΪΓΔFe2ΘΪΓΔSO42-ΓΔCl-
D. »τ»ή“ΚXΈΣ100 mLΘ§≤ζ…ζΒΡΤχΧεAΈΣ112 mLΘ®±ξΩωΘ©Θ§‘ρX÷–c(Fe2+)=0.05molΓΛL-1
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΫΪΝΫ÷÷Ϋπ τΒΞ÷ Ήι≥…ΒΡΜλΚœΈο11gΘ§Φ”ΒΫΉψΝΩœΓΝρΥα÷–Θ§Ήν÷’ΒΟΒΫ11.2LΘ®±ξΉΦΉ¥Ωωœ¬Θ©ΒΡ«βΤχΘ§’βΝΫ÷÷Ϋπ τΩ…Ρή «Θ® Θ©
A.ZnΚΆFeB.AgΚΆMgC.AlΚΆ CuD.MgΚΆZn
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com