
【题目】一定量的盐酸跟过量的铁粉反应时,为了减缓反应速度,且不影响生成氢气的总量,可向盐酸中加入适量的( )
①NaOH固体 ②H2O ③HCl气体 ④CH3COONa固体 ⑤NaNO3固体 ⑥KCl溶液
A.②④⑥B.①②C.②③⑤D.②④⑤⑥
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】关于下列各图的叙述错误的是![]()
化学方程式 | 平衡常数K |
|
|
|
|
|
|
|
|
A.已知1molCO燃烧放出的热为283kJ,![]() ;
;![]() 则
则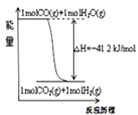 表示CO和
表示CO和![]() 生成
生成![]() 和
和![]() 的能量变化
的能量变化
B.常温下![]()
![]() HB溶液和
HB溶液和![]()
![]() 溶液等体积混合后溶液的
溶液等体积混合后溶液的![]() ,则混合溶液中离子浓度的大小顺序为:
,则混合溶液中离子浓度的大小顺序为:![]()
C.常温下,![]() 和
和![]() 反应生成HX的平衡常数如表所示,仅依据K的变化,就可以说明在相同条件下,平衡时
反应生成HX的平衡常数如表所示,仅依据K的变化,就可以说明在相同条件下,平衡时![]() 从
从![]() 到
到![]() 的转化率逐减小,且HX的还原性逐渐减弱
的转化率逐减小,且HX的还原性逐渐减弱
D.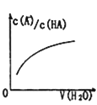 中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,
中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,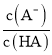 的变化情况
的变化情况
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是有机化学中的几个重要实验。图一是制取乙酸乙酯,图二是验证醋酸、碳酸、苯酚酸性强弱;图三是实验室制取乙炔并检验其部分性质。请根据要求填空。
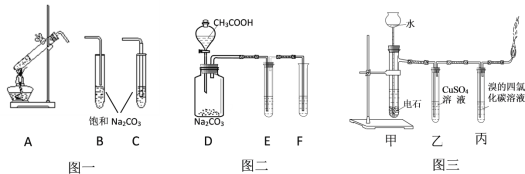
(1)图一中A发生的化学方程式为__________, A的导管应与_______相连(填字母)。
(2)图二中的E和F分别盛装的药品应为_____________和______________。
A.石蕊溶液 B.苯酚钠溶液 C.碳酸氢钠溶液 D.碳酸钠溶液
(3)图三中乙装置的作用是_______________,实验过程中发现燃烧非常剧烈,分析其主要原因是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,二元弱酸 H2Y 溶液中滴加 KOH 溶液,所得混合溶液的 pH 与离子浓度变化的关系如图所示,下列有关说法错误的是( )

A. 曲线 M 表示 pH与lg![]() 的变化关系
的变化关系
B. Ka2(H2Y)=10-4.3
C. d 点溶液中: c(H+)-c(OH -)=2c(Y2-)+ c(HY-)-c(K+)
D. 交点 e 的溶液中: c(H2Y) = c(Y2-) > c(HY-)> c(H+)> c(OH -)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家合成了一种新的化合物,其结构式如图所示。该物质中 W、X、Y、Z、M是短周期中常见元素,且原子序数依次增大;已知M元素原子核外电子总数是Y元素原子核外 电子总数的两倍。下列说法中错误的是
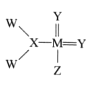
A.由X和Y两种元素形成的化合物有多种
B.W和Z元素位于周期表中同一主族
C.元素的非金属性强弱顺序为:Z>Y>X
D.Y、M元素的气态氢化物沸点高低为:Y>M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求完成下列各题。
(1)25℃时,向AgCl的悬浊液中加入KI固体,有黄色沉淀生成。说明Ksp(AgCl)___Ksp(AgI)(填“<”、“>”或“=”下同)。
(2)已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-。若浓硫酸与氢氧化钠溶液发生中和反应生成1mol水,则ΔH的数值___57.3kJ·mol-;若稀盐酸与氨水发生中和反应生成1mol水,则ΔH的数值___57.3kJ·mol-1。
(3)在化学反应里只有活化分子才可能发生化学反应,使普通分子变成活化分子所需提供的最低限度的能量叫活化能。根据如图回答问题。
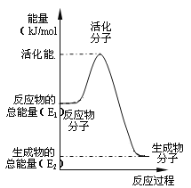
①图中所示反应是___(填“吸热”或“放热”)反应,该反应___(填“需要”或“不需要”)加热,该反应的△H=___(用含E1、E2的代数式表示)。
②已知热化学方程式:H2(g)+![]() O2(g)=H2O(g) △H=-241.8kJ·mol-1,该反应的活化能为167.2kJ·mol-1,则其逆反应的活化能为___。
O2(g)=H2O(g) △H=-241.8kJ·mol-1,该反应的活化能为167.2kJ·mol-1,则其逆反应的活化能为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气溶于水形成的饱和溶液中,存在以下的溶解平衡和电离平衡:NH3+H2O![]() NH3H2O,NH3H2O
NH3H2O,NH3H2O![]() NH4++OH-,这些平衡都满足勒夏特列原理,若向已达到平衡的体系中通入下列物质,请填空。
NH4++OH-,这些平衡都满足勒夏特列原理,若向已达到平衡的体系中通入下列物质,请填空。
(1)加入少量氨气,平衡向___(填“正”或“逆”,下同)反应方向移动。
(2)通入HCl气体,平衡向___反应方向移动,c(NH4+)___(填“增大”或“减小”,下同)。
(3)加入NaOH固体,平衡向___反应方向移动,c(OH-)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物在我们的生产生活当中有着重要的作用,探究有机物结构有助于对物质的性质进行研究。
(1)a.![]() b.
b.![]() c.
c.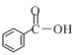
①上述三种物质中b,c中官能团名称分别是__________,__________。
②三种物质在一定条件分别与氢气发生加成反应,同温同压下消耗氢气量关系为______(填“相同”或“不相同”)。
(2)欲区分乙醛和乙酸,应选用 ____(填字母)。
a.NaOH溶液 b.HCl溶液 c.银氨溶液 d.新制氢氧化铜悬浊液
(3)工业上或实验室提纯以下物质的方法不合理的是(括号内为杂质)______。
A. 溴苯(溴):加NaOH溶液,分液 B. 乙烷(乙烯):通入溴水,洗气
C. 乙酸(水):加新制生石灰,蒸馏 D. 乙酸乙酯(乙酸):氢氧化钠溶液,分液
(4)苹果酸(![]() )与NaOH溶液反应的化学方程式___________。
)与NaOH溶液反应的化学方程式___________。
(5)以KOH为电解质的甲醇燃料电池总反应为2CH3OH+3O2+4KOH=2K2CO3+6H2O。电池放电时电解质溶液中OH-向_______(填“正”或“负”)极移动,负极反应式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的铜粉加入到0.5 L 0.3 mol·L-1 Fe2(SO4)3和0.1 mol·L-1 H2SO4的混合溶液中,铜粉完全溶解后,得到溶液X。下列说法正确的是( )
A.溶液X中Cu2+与Fe2+的物质的量之比为2∶1
B.向溶液X中加入足量铁粉,充分反应后,铁粉质量减少11.2 g
C.向溶液X中滴加KSCN溶液,未变红色,则加入铜粉质量为12.8 g
D.向溶液X中加入0.18 L 5 mol·L-1 NaOH溶液可使溶液中的金属离子完全沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com