
【题目】根据要求完成下列各题。
(1)25℃时,向AgCl的悬浊液中加入KI固体,有黄色沉淀生成。说明Ksp(AgCl)___Ksp(AgI)(填“<”、“>”或“=”下同)。
(2)已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-。若浓硫酸与氢氧化钠溶液发生中和反应生成1mol水,则ΔH的数值___57.3kJ·mol-;若稀盐酸与氨水发生中和反应生成1mol水,则ΔH的数值___57.3kJ·mol-1。
(3)在化学反应里只有活化分子才可能发生化学反应,使普通分子变成活化分子所需提供的最低限度的能量叫活化能。根据如图回答问题。
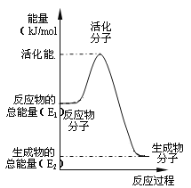
①图中所示反应是___(填“吸热”或“放热”)反应,该反应___(填“需要”或“不需要”)加热,该反应的△H=___(用含E1、E2的代数式表示)。
②已知热化学方程式:H2(g)+![]() O2(g)=H2O(g) △H=-241.8kJ·mol-1,该反应的活化能为167.2kJ·mol-1,则其逆反应的活化能为___。
O2(g)=H2O(g) △H=-241.8kJ·mol-1,该反应的活化能为167.2kJ·mol-1,则其逆反应的活化能为___。
【答案】> > < 放热 需要 E2-E1 409kJ/mol
【解析】
(1)根据沉淀转化的规律分析解答;
(2)浓硫酸溶于水放热,氨水的电离需要吸热,据此分析判断;
(3)①依据图象分析反应物的能量大于生成物的能量,且反应的活化能较大,结合反应的焓变=生成物的能量-反应物的能量分析判断;②根据焓变等于正逆反应的活化能之差计算。
(1)KSP(AgCl)>KSP(AgI),沉淀转化为溶解度更小的物质容易发生,因此向AgCl的悬浊液中加入KI溶液,沉淀由白色转化为黄色,故答案为:>;
(2)浓硫酸溶于水放热,因此浓硫酸与氢氧化钠溶液发生中和反应生成1mol水,放出的热量多于57.3kJ;氨水的电离需要吸热,因此稀盐酸与氨水发生中和反应生成1mol水,放出的热量少于57.3kJ,故答案为:>;<;
(3)①依据图象,反应物的能量大于生成物的能量,反应放热;该反应的活化能较大,引发反应需要加热,反应的焓变△H=生成物的能量-反应物的能量=(E2-E1)kJ/mol,故答案为:放热;需要;E2-E1;
②焓变等于正逆反应的活化能之差,则逆反应的活化能为167.2kJmol-1-(-241.8kJmol-1)=409.0 kJmol-1,故答案为:409.0 kJmol-1。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】某温度下HF的电离常数Ka=3.3×10-4 ,CaF2的溶度积常数Ksp=1.46×10-10。在该温度下取浓度为0.31 mol·L-1的HF与浓度为0.002 mol·L-1的CaCl2溶液等体积混合。下列说法正确的是
A. 该温度下,0.31 mol·L-1的HF溶液的pH=2
B. 升高温度或增大浓度,HF的电离平衡常数都将增大
C. 两溶液混合不会产生沉淀
D. 向饱和的CaF2溶液中加入少量CaCl2固体后,溶度积常数Ksp一定比之前减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向2L恒容密闭容器中充入1.0molA和1.0molB,发生反应A(g)+B(g)![]() C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
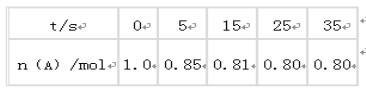
A.反应在前5s的平均速率v(A)= 0. 17mol/(L·s)
B.保持其他条件不变,升高温度,平衡时c(A)=0.41mol/L,则反应的△H>0
C.相同温度下,起始时向容器中充入2.0molC,达到平衡时,C的转化率大于80%
D.相同温度下,起始时向容器中充入0.20 molA、0.20 molB和1.0molC,反应达到平衡前v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),发生H2(g)+CO2(g)CO(g)+H2O(g),其起始浓度如表所示。已知:平衡时甲中CO气体的浓度为0.006mol/L。下列判断不正确的是( )
起始浓度(mol/L) | 甲 | 乙 | 丙 |
c(H2) | 0.010 | 0.020 | 0.020 |
c(CO2) | 0.010 | 0.010 | 0.020 |
A.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
B.平衡时,甲、乙、丙中CO2的转化率有如下关系:乙>甲=丙=60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L
D.改变条件使乙中温度降低,新平衡中H2的浓度增大,则正反应的△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的盐酸跟过量的铁粉反应时,为了减缓反应速度,且不影响生成氢气的总量,可向盐酸中加入适量的( )
①NaOH固体 ②H2O ③HCl气体 ④CH3COONa固体 ⑤NaNO3固体 ⑥KCl溶液
A.②④⑥B.①②C.②③⑤D.②④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T0时,在容积固定的密闭容器中发生反应:X(g)+Y(g)![]() Z(g)(未配平),4 min 时达到平衡,各物质浓度随时间变化的关系如图a所示。其他条件相同,温度分别为T1、T2时发生反应,Z的浓度随时间变化的关系如图b所示。下列叙述正确的是
Z(g)(未配平),4 min 时达到平衡,各物质浓度随时间变化的关系如图a所示。其他条件相同,温度分别为T1、T2时发生反应,Z的浓度随时间变化的关系如图b所示。下列叙述正确的是
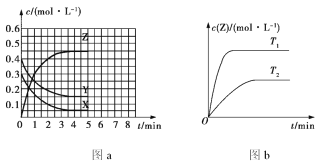
A. 发生反应时,各物质的反应速率大小关系为v(X)=v(Y)=2v(Z)
B. 图a中反应达到平衡时,Y的转化率为37.5%
C. T0时,该反应的平衡常数为33.3
D. 该反应正反应的反应热ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇燃料电池被认为是21世纪电动汽车候选动力源
(1)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H1= + 49.0kJmol﹣1
②CH3OH(g)+![]() O2(g)═CO2(g)+2H2(g)△H2
O2(g)═CO2(g)+2H2(g)△H2
已知H2(g)+![]() O2(g)═H2O(g)△H=﹣241.8kJmol﹣1,则反应②的△H2=_____.
O2(g)═H2O(g)△H=﹣241.8kJmol﹣1,则反应②的△H2=_____.
(2)工业上一般可采用如图1所示反应来合成甲醇:CO(g)+2H2(g) CH3OH(g),现实验室模拟该反应并进行分析,图1是该反应在不同温度下CO的转化率随时间变化的曲线

①该反应的焓变△H_____0(填“>”“<”或“=”).
②T1和T2温度下的平衡常数大小关系是K1_____K2(填“>”“<”或“=”)
③现进行如下实验,在体积为1L的密闭容器中,充入1molCO和3molH2,测得CO 和CH3OH(g)的浓度随时间变化如图2所示.从反应开始到平衡,CO的平均反应速率v(CO)=_____,该反应的平衡常数为K=________
④恒容条件下,达到平衡后,下列措施中能使n(CH3OH)/n(CO)增大的有_______
A.升高温度 B.充入He(g)
C.再充入1molCO 和3molH2 D.使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中进行反应:X2(g)+Y2(g)![]() 2Z(g),若X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡状态时,下列说法正确的是
2Z(g),若X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡状态时,下列说法正确的是
A、Z的浓度可能为0.3mol/L
B、平衡时X2、Y2的转化率相等
C.平衡时,Y2和Z的生成速率之比为2:1
D、若平衡后再改变外界条件,升高温度,则反应的平衡常数将变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组探究在加热条件下FeSO4分解的气体产物及相关性质。已知:SO2的沸点为-10 ℃、SO3的沸点为44.8 ℃。
用如图所示装置设计实验,验证分解FeSO4生成的气态产物。
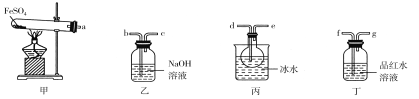
(1)实验前必须进行的操作是________。
(2)按气流方向连接各仪器,用字母表示接口的连接顺序:a→________。
(3)若观察到装置甲中固体变为红棕色,装置丙中有无色液体产生,装置丁中溶液变成无色,则FeSO4分解的化学方程式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com