
【题目】2009年2月,日本产业技术综合研究所能源技术研究部门能源界面技术研究小组组长周豪慎和日本学术振兴会(JSPS)外籍特别研究员王永刚共同开发出了新构造的大容量锂空气电池。下列说法不正确的是

A.放电时的正极反应为O2+2H2O+4e-→4OH-
B.充电时正极附近pH降低
C.若用该电池作电源电解硫酸镁溶液,当电路中有0.02mol e-转移时,阴极增重0.24g
D.在该电池中,放电反应生成的不是固体的Li2O,而是容易溶解在水性电解液中的LiOH(氢氧化锂)。因此,氧化锂在空气电极堆积后,不会导致工作停止
科目:高中化学 来源: 题型:
【题目】硼(B)及其化合物在化学中具有十分重要的地位,请回答下列有关问题。
(1)基态硼原子中有_______种能量不同的电子,第一电离能介于B和N之间的第二周期元素有_______种。
(2)硼酸(![]() )能够屏蔽核辐射,其晶体具有层状结构(每一层结构如图所示),成片状,有滑腻感,可作润滑剂。
)能够屏蔽核辐射,其晶体具有层状结构(每一层结构如图所示),成片状,有滑腻感,可作润滑剂。
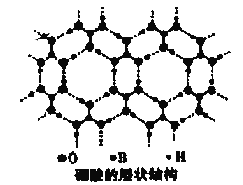
①硼酸晶体内所含有作用力类型有__________________,根据硼酸的分子结构判断硼酸应属于________(填“强酸”“中强酸”或“弱酸”),你的判断依据是_________________________。
②三氟化硼(![]() )水解生成硼酸和氟硼酸(
)水解生成硼酸和氟硼酸(![]() ),与
),与![]() 互为等电子体的一种阴离子是_________(写化学式)。
互为等电子体的一种阴离子是_________(写化学式)。
(3)六方氮化硼的结构与石墨结构相类似(如图甲),上、下层平行,B、N原子相互交替,层内B—N核间距为acm,层间距为![]() ,晶体密度为
,晶体密度为![]() ,晶胞如图乙所示。六方氮化硼晶体中硼原子的杂化类型为___________,其结构与石墨相似却不导电,原因是___________________,网状加德罗常数
,晶胞如图乙所示。六方氮化硼晶体中硼原子的杂化类型为___________,其结构与石墨相似却不导电,原因是___________________,网状加德罗常数![]() ________。(用含
________。(用含![]() 的式子表示)。
的式子表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水在25℃和95℃时,其电离平衡曲线如图所示:

(1)则95℃时,水的电离平衡曲线应为B,请说明理由______________________.
25℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,所得混合溶液的pH=7,则NaOH溶液与硫酸溶液的体积比为______________。
(2)95℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈中性,则a与b之间应满足的关系是______________.
(3)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的电离程度分别用α1、α2表示,则α1______________α2(填“大于”、“小于”、“等于”或“无法确定”)。
(4)曲线B对应温度下,将0.02mol/LBa(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合后,混合溶液的pH=________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列说法正确的是
A.6.8g熔融KHSO4与3.9g Na2O2阴离子数目相同
B.某金属阳离子的结构为![]() 与Cl-形成的强电解质都是离子化合物
与Cl-形成的强电解质都是离子化合物
C.二硫化碳是直线型的非极性分子,其电子式是![]()
D.因为氯、溴、碘非金属性逐渐减弱,所以其氢化物酸性HCl>HBr>HI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:C(s)+2NO(g)![]() CO2(g)+N2(g),平衡时c(NO)与温度T的关系如图所示,则下列说法正确的是( )
CO2(g)+N2(g),平衡时c(NO)与温度T的关系如图所示,则下列说法正确的是( )
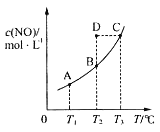
A.该反应的ΔH>0
B.若该反应在T1、T2℃时的平衡常数分别为K1、K2,则K1<K2
C.在T2℃时,若反应体系处于状态D,则此时v正>v逆
D.若状态B、C、D的压强分别为p(B)、p(C)、p(D),则p(C)=p(D)>p(B)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下述转化关系,回答问题:

已知:①+CH3Br![]() CH3+HBr;
CH3+HBr;
②C物质苯环上一卤代物只有两种。
(1)写出B物质的名称__________;D物质的结构简式________。
(2)写出反应②的类型________;反应⑤的条件________。
(3)写出反应⑥的化学方程式:________________________________。
(4)写出D+E反应的化学方程式:_______________。
(5)反应②还有可能生成一种C16H18的有机物,其苯环上一卤代物也只有两种,写出它的结构简式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活中常用的净水剂KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐( 主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:
![]()
(1)为尽量少引入杂质,试剂①应选用__________ (填标号)。
A.HCl溶液 B.H2SO4 溶液 C.氨水 D.NaOH溶液
(2)沉淀B的化学式为______________;将少量明矾溶于水,溶液呈弱酸性,其原因是_________________________________ (用离子方程式表示)。
(3)科学研究证明NaAlO2 在水溶液中实际上是Na[Al(OH)4](四羟基合铝酸钠),易拉罐溶解过程中主要反应的化学方程式为_______________________________________。
(4)常温下,等pH的NaAlO2 和NaOH两份溶液中,由水电离出的c(OH-)前者为后者
的108倍,则两种溶液的pH=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃、101kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5kJ/mol、285.8kJ/mol、890.3kJ/mol、2800kJ/mol,则热化学方程式正确的是
A.C(s)+![]() O2(g)=CO(g) △H=-393.5kJ/mol
O2(g)=CO(g) △H=-393.5kJ/mol
B.2H2(g)+O2(g)=2H2O(g) △H=+571.6kJ/mol
C.CH4(g)+2O2(g)=2H2O(l)+CO2(g) △H=-890.3kJ/mol
D.![]() C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(g) △H=-1400kJ/mol
C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(g) △H=-1400kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应3A(g)+B(g)![]() 2C(g)+2D(g) ΔH<0,图中,a、b曲线分别表示在不同条件下,A与B反应时,D的体积分数随时间t的变化情况。若想使曲线b(实线)变为曲线a(虚线),可采用的措施是
2C(g)+2D(g) ΔH<0,图中,a、b曲线分别表示在不同条件下,A与B反应时,D的体积分数随时间t的变化情况。若想使曲线b(实线)变为曲线a(虚线),可采用的措施是

①增大A的浓度 ②升高温度 ③增大D浓度 ④加入催化剂 ⑤恒温下,缩小反应容器体积 ⑥加入稀有气体,保持容器内压强不变
A. ①②③ B. ④⑤ C. ③④⑤ D. ④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com