
【题目】镍是银白色金属,具有磁性。图1为一种含镍配合物及其配体。

(1)Ni2+基态核外电子排布式为__________________。
(2)物质A中碳原子采取的杂化类型为__________,所含有的非金属元素的第一电离能 由小到大顺序为__________(用元素符号表示)。
(3)1 mol物质B中所含σ键的物质的量为__________mol。
(4)物质B在一定条件下水解生成 的沸点为197 ℃,而
的沸点为197 ℃,而![]() 的沸点为247 ℃,导致两种物质沸点相差较大的原因是____________。
的沸点为247 ℃,导致两种物质沸点相差较大的原因是____________。
(5)红镍矿是一种重要的含镍矿物,其主要成分的晶胞如图2所示,则每个 Ni原子周围与之紧邻的As原子数为__________。
 。
。
【答案】1s22s22p63s23p63d8或[Ar]3d8 sp2 C<O<N 16 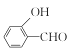 形成分子内氢键,
形成分子内氢键,![]() 形成分子间氢键,故前者沸点低于后者 6
形成分子间氢键,故前者沸点低于后者 6
【解析】
(1)镍是28号元素,Ni2+核外有26个电子,根据构造原理写电子排布式。
(2)苯环碳原子有3个![]() 键,无孤电子对,所以采取sp2杂化,侧链(-CH=N-)碳原子含有3个
键,无孤电子对,所以采取sp2杂化,侧链(-CH=N-)碳原子含有3个![]() 键,没有孤电子对,故也采取sp2杂化。物质A中含有的非金属元素有C、H、O、N,根据第一电离能的递变规律排序。
键,没有孤电子对,故也采取sp2杂化。物质A中含有的非金属元素有C、H、O、N,根据第一电离能的递变规律排序。
(3)单键是σ键,双键中只有1个σ键,苯环上相邻的两个碳原子间只有1个σ键,据此分析。
(4) ![]() 分子中O-H与-CHO之间形成分子内氢键,而
分子中O-H与-CHO之间形成分子内氢键,而![]() 中O-H与-CHO距离较远,只能形成分子间氢键,从氢键角度分析沸点差异。
中O-H与-CHO距离较远,只能形成分子间氢键,从氢键角度分析沸点差异。
(5)以顶点为中心,结合晶体图像分析即可。
(1)镍是28号元素,Ni2+核外有26个电子,根据构造原理可得Ni2+基态核外电子排布式为1s22s22p63s23p63d8或[Ar]3d8。
(2)苯环碳原子有3个![]() 键,无孤电子对,所以采取sp2杂化,侧链(-CH=N-)碳原子含有3个
键,无孤电子对,所以采取sp2杂化,侧链(-CH=N-)碳原子含有3个![]() 键,没有孤电子对,故也采取sp2杂化,所以物质A中碳原子都采取sp2杂化。物质A中含有的非金属元素有C、H、O、N,根据第一电离能的递变规律可知,第一电离能由小到大顺序为C<O<N(H不参与比较)。
键,没有孤电子对,故也采取sp2杂化,所以物质A中碳原子都采取sp2杂化。物质A中含有的非金属元素有C、H、O、N,根据第一电离能的递变规律可知,第一电离能由小到大顺序为C<O<N(H不参与比较)。
(3)单键是σ键,双键中只有1个σ键,苯环上相邻的两个碳原子间只有1个σ键。物质B中单键数有5个C-H,1个N-H,1个O-H,侧链1个C-C,1个C-O;含双键数为1个C=N;苯环共有6个σ键,所以1mol物质B中所含σ键的物质的量为16mol。
(4) ![]() 分子中O-H与-CHO之间形成分子内氢键,而
分子中O-H与-CHO之间形成分子内氢键,而![]() 中O-H与-CHO距离较远,只能形成分子间氢键,所以
中O-H与-CHO距离较远,只能形成分子间氢键,所以![]() 沸点低于
沸点低于![]() 的沸点。
的沸点。
(5)以顶点为中心,结合晶体图像分析可知,晶体中每个Ni原子周围与之紧邻的As原子数为6。


科目:高中化学 来源: 题型:
【题目】氟利昂是饱和碳氢化合物的卤族衍生物的总称,其破坏臭氧层的化学反应机理如下(以二氯二氟甲烷为例,二氯二氟甲烷可由四氯化碳与氟化氢在催化剂存在下、控制回流冷凝温度为﹣5℃时得到):
①CF2Cl2![]() CF2Cl+Cl
CF2Cl+Cl
②Cl+O3→ClO+O2
③ClO+ClO→ClOOCl(过氧化氯)
④ClOOCl![]() 2Cl+O2
2Cl+O2
下列说法中不正确的是
A. 紫外线使CF2Cl2分解产生的是臭氧生成氧气的催化剂
B. 反应③中的氯子与反应④中生成的氯原子化学性质相同
C. ClOOCl分子中各原子最外层均达到8电子稳定結构
D. 气态氢化物的稳定性:HF>H2O>HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸晶体的组成可用H2C2O4·xH2O表示,为了测定x 值,进行如下实验:
①称取wg草酸晶体,配成100.00 mL水溶液。
②量取25.00 mL所配制的草酸溶液置于锥形瓶内,加入适量稀硫酸。
③用浓度为a mol/L的KMnO4溶液滴定到终点。
所发生的反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O 。试回答:
(1)实验中不需要的仪器有___________(填序号),还缺少的玻璃仪器有________(填名称)。
a.托盘天平(带砝码,镊子) b.滴定管 c.100mL量筒 d.100mL容量瓶 e.烧杯 f.漏斗 g.锥形瓶 h.玻璃棒 i.药匙 j.烧瓶
(2)实验中,标准液KMnO4溶液应装在_____________式滴定管中。
(3)若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,则所测得的x值会____________(填“偏大”、“ 偏小”、“ 无影响”)
(4)滴定时,根据_______________现象,即可确定反应达到终点。
(5)在滴定过程中若用amol/L的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为_______mol/L,由此可计算x的值是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定某有机物A的结构,做如下实验:

①将4.4g该有机物完全燃烧,生成 0.2mol CO2和3.6g水;
②用质谱仪测定其相对分子质量,得如图1所示的质谱图;
③A的核磁共振氢谱如图2:
试回答下列问题:
(1)有机物A的相对分子质量是_____________
(2)有机物A的实验式是_____________
(3)有机物A的分子式是_____________
(4)红外光谱上发现A有﹣COOH和2个﹣CH3则有机物A的结构简式 ________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将甘油(C3H8O3)转化成高附加值产品是当前热点研究方向,甘油和水蒸气经催化重整可制得氢气,反应主要过程如下:
反应Ⅰ: C3H8O3(l)+3H2O(g)![]() 3CO2(g)+7H2(g) ΔH1
3CO2(g)+7H2(g) ΔH1
反应Ⅱ: 2C3H8O3(l)+3O2(g)![]() 6CO2(g)+8H2(g) ΔH2=a kJ·mol-1
6CO2(g)+8H2(g) ΔH2=a kJ·mol-1
反应Ⅲ: 2H2(g)+O2(g)![]() 2H2O(g) ΔH3=b kJ·mol-1
2H2O(g) ΔH3=b kJ·mol-1
(1)ΔH1=__________。
(2)酸性条件下,甘油可在纳米TiO2Pt复合膜阳极上转化为甘油醛(C3H6O3),该电极方程式为________________________________。
(3)硝化甘油(C3H5O9N3)是治疗心绞痛的速效药,也可用作开采矿物的炸药。
①硝化甘油能治疗心绞痛的原理是在人体中释放NO,实验室中也可通过干法制备NO,方程式为3KNO2+KNO3+Cr2O3![]() 2K2CrO4+4NO↑。若有1 mol NO生成,则被KNO3氧化的Cr2O3的物质的量为________mol。
2K2CrO4+4NO↑。若有1 mol NO生成,则被KNO3氧化的Cr2O3的物质的量为________mol。
②硝化甘油爆炸时会彻底分解为N2、O2、CO2和H2O,反应的化学方程式为__________________________________________。
(4)①反应Ⅰ制备H2时的副产物很多,主要有CH4、C2H4等,生产过程中必须采取措施抑制副产物产生,目的是__________________________________________________________。
②为了有效提高反应Ⅰ氢气的产率,研究人员还采用CaO吸附增强制氢的方法。如图1所示,请分析加入CaO提高氢气产率的原因_________________________________________。

(5)高效的催化剂是这种制氢方法能大规模应用的重要因素。图2为三种不同催化剂在一段时间内与甘油转化率的关系,则Ni/SiC催化剂的优点是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2002年诺贝尔化学奖获得者的贡献之一是发明了对有机分子的结构进行分析的质谱法。其方法是让极少量(10-9g左右)的化合物通过质谱仪的离子化室使样品分子大量离子化,少量分子碎裂成更小的离子。如C2H6离子化后可得到C2H6+、C2H5+、C2H4+、……然后测定其质荷比β。设H+的质荷比为1,某有机物样品的质荷比如下图(假设离子均带一个单位正电荷,信号强度与该离子多少有关),则该有机物可能

A. CH3OH B. C3H8 C. C2H4 D. CH4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学”是当今社会提出的一个新概念。在“绿色化学”工艺中,理想状态是反应物中的原子全部转化为欲制的产物,即原子利用率为100%。下列反应最符合绿色化学中“原子经济”要求的是
A. nCH2=CH2![]()
![]()
B. CH4+2Cl2![]() CH2Cl2+2HCl
CH2Cl2+2HCl
C. Cl2+2NaOH===NaCl+NaClO+H2O
D. 3NO2+H2O===2HNO3+NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)。请填空:

(1)试管a中需要加入浓硫酸、冰醋酸和乙醇各2 mL,正确的加入顺序及操作是______________________。
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是________。
(3)实验中加热试管a的目的是:①______________;②______________。
(4)试管b中加有饱和Na2CO3溶液,其作用是________________。
(5)反应结束后,振荡试管b,静置。观察到的现象是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取O2和Cl2的化学反应方程式分别为①2KClO3 ![]() 2KCl+3O2↑;②MnO2+4HCl(浓)
2KCl+3O2↑;②MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,则下列说法正确的是( )
MnCl2+Cl2↑+2H2O,则下列说法正确的是( )
A. 均为氧化还原反应
B. ②中MnO2为还原剂
C. ①中反应前后MnO2质量不发生变化
D. ①中反应前后MnO2化学性质改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com