
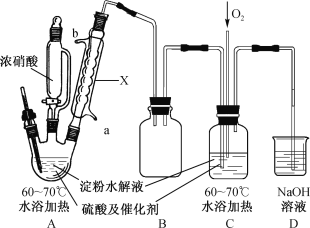
【题目】某实验小组制备草酸晶体(H2C2O4·2H2O)的实验装置如下:
已知:I.草酸(H2C2O4)是二元弱酸,熔点101~102℃;
II.草酸的溶解度如下表所示:
温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 |
溶解度/g·(100g水)-1 | 9.5 | 14.3 | 21.2 | 31.4 | 46.0 | 84.5 |
III.在催化剂和硫酸存在下,用浓硝酸氧化淀粉水解液可制备草酸,发生的主要反应为:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O。
回答下列问题:
(1)装置A中仪器X名称为___________,水从接口___________(填“a”或“b”)进入。
(2)装置B的作用是___________;设计装置C的目的是_________________________。
(3)反应C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O中,每生成1 mol H2C2O4转移电子的物质的量为____________。
(4)将装置A和C中反应液浓缩、静置结晶并过滤得粗草酸晶体,提纯H2C2O4·2H2O的方法是_________________________。
(5)探究草酸的性质:
①向Na2CO3溶液中滴加H2C2O4溶液,产生大量气体,说明草酸的酸性比碳酸________(填“强”或“弱”)。
②向NaClO溶液中加入过量H2C2O4溶液,有气泡产生,能解释这一现象的离子方程式为___。
【答案】(球形)冷凝管 a 安全瓶 提高HNO3的利用率 6mol 重结晶 强 ClO-+H2C2O4= Cl-+2CO2↑+H2O
【解析】
(1)装置A中仪器X名称为(球形)冷凝管,冷却水流向都是下进上出。
(2)装置B中两导管都短,主要是防止倒吸;在装置C中,NO、NO2、O2反应生成HNO3,能将淀粉水解液中的葡萄糖氧化为草酸。
(3)反应C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O中,有机物中C元素价态不一定相同,计算变价数比较麻烦,当然也可从平均化合价进行分析,还可从N元素的价态变化判断电子转移的数目。
(4)装置A和C最终都发生葡萄糖氧化为酸的反应,最终所得溶液中都含草酸,从粗草酸晶体提纯H2C2O4·2H2O的方法是溶解后再结晶。
(5)①向Na2CO3溶液中滴加H2C2O4溶液,产生大量气体,应为CO2,反应满足强酸制弱酸的原则。
②向NaClO溶液中加入过量H2C2O4溶液,有气泡产生,则生成CO2,ClO-被还原为Cl-。
(1)装置A中仪器X名称为(球形)冷凝管,冷却水从接口a进入。答案为:(球形)冷凝管;a;
(2)装置B主要是为了防止倒吸,其作用为安全瓶;设计装置C的目的是将A中产生的NO、NO2转化为HNO3,提高HNO3的利用率。答案为:安全瓶;提高HNO3的利用率;
(3)从反应C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O中N元素分析,生成3molH2C2O4,同时生成(9molNO2+3molNO),N元素共得电子(9×1+3×3)mol;则每生成1 mol H2C2O4转移电子的物质的量为6mol。答案为:6mol;
(4)从粗草酸晶体提纯H2C2O4·2H2O的方法是加水溶解后,再让草酸结晶析出。答案为:重结晶;
(5)①向Na2CO3溶液中滴加H2C2O4溶液,产生大量气体,应为CO2,反应满足强酸制弱酸的原则,从而说明草酸的酸性比碳酸。答案为:强;
②向NaClO溶液中加入过量H2C2O4溶液,有气泡产生,则生成CO2,ClO-被还原为Cl-,发生反应的离子方程式为:ClO-+H2C2O4= Cl-+2CO2↑+H2O。答案为:ClO-+H2C2O4= Cl-+2CO2↑+H2O。


科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)常用于催化剂、颜料、防腐等工业。某兴趣小组设计实验制备氯化亚铜。回答下列问题:

制法一:将铜粉加入B反应器中,与一定浓度的食盐—盐酸溶液相互作用,在60~70℃通入氧气,充分反应(部分仪器略去)。
①仪器X的名称___,X中盛有二氧化锰,分液漏斗中盛放双氧水,则A装置中发生反应的化学方程式是___。

②反应结束后,打开瓶塞 a,倾出反应液于大烧杯中,为防止外溅,通常采用的操作方法是___。
制法二:将氯化铜与氯化钠加水溶解,并调节酸度,加入铜粉一起加热,Cu2+被单质铜还原,生成可溶性的配合物Na[CuCl2],再经水解后产生白色沉淀。抽滤,沉淀依次用水、无水乙醇洗涤多次,得白色固体产品
①写出该法生成Na[CuCl2]的化学反应方程式___。
②用水洗涤CuCl沉淀的具体操作为___,沉淀水洗后再用无水乙醇洗涤的原因是___。
③判断CuCl是共价化合物还是离子化合物的实验方法是___。
制法三:以铜为电极,电解饱和食盐水也可制得CuCl。阳极的电极反应式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有 关汉黄芩素的叙述正确的是

A. 汉黄芩素的分子式为 C16H13O5
B. 该物质遇 FeCl3 溶液显色
C. 1 mol 该物质与溴水反应,最多消耗 1 mol Br2
D. 与足量 H2 发生加成反应后,该分子中官能团的种类减少 1 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验装置图回答问题:
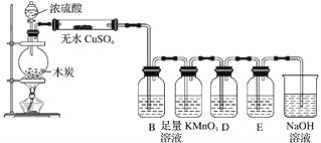
(1)浓H2SO4和木炭在加热时发生反应的化学方程式是__,如果有0.2mol电子转移,则在标准状况下产生气体__。
(2)若用图示中的装置检验上述反应的全部产物,写出有关仪器中应加入的试剂和作用:无水CuSO4试剂作用是__,B中加入的试剂是__,作用是__,足量KMnO4溶液作用是___,D中加入的试剂是__,作用是__,NaOH溶液的作用是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体:
①D的化学式是________;
②在工业生产中,B气体的大量排放被雨水吸收后形成了________而污染了环境。
(2)若A在常温下为气体,C是红棕色的气体:
①A、C的化学式分别是:A________;C________。
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式_______________________________________________。该反应________(填“属于”或“不属于”)氧化还原反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备光敏材料KaFeb(C2O4)c·xH2O的工艺流程如下:
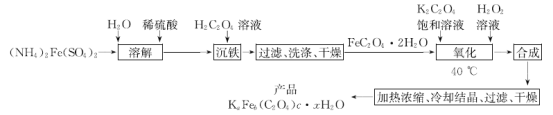
回答下列问题:
(1)“溶解”时,为使所用的水中不含O2,采用的操作方法是_________________。
(2)用H2C2O4(弱酸)“沉铁”时,反应的离子方程式为______________。
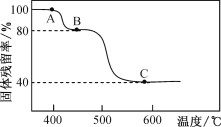
(3)FeC2O4·2H2O热分解与气氛及温度有关,在N2气氛中热分解时,固体的残留率(固体样品的剩余质量/固体样品的起始质量×100%)与温度的关系如图所示,则B→C的变化中,发生反应的化学方程式为___________________。
(4)“氧化”时,温度不宜超过40℃,其原因是_______。
(5)为测定产品KaFeb(C2O4)c·xH2O(铁元素为+3价)的组成,称取产品0.2455g用硫酸溶解后,用0.02000 mol·L-1的KMnO4标准溶液滴定至终点,消耗标准溶液30.00 mL。在上述滴定过C2O42-的保留液中加入足量锌粉,加热至黄色消失,过滤洗涤,滤液及洗涤液再用0.02000 mol·L-1的KMnO4标准溶液滴定至终点,消耗标准溶液5.00 mL。则该产品的化学式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100mL 0.1mol/L的H2A溶液中滴加0.1mol/LNaOH溶液,含A元素相关微粒物质的量随pH的变化如图所示。下列说法正确的是
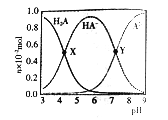
A. H2A在水中的电离方程式是:H2A=H++HA-, HA-![]() H++A2-
H++A2-
B. 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
C. Y点溶液中存在以下关系: c(H+)+c(Na+)=c(OH-)+3c(HA-)
D. X点溶液中含A元素相关微粒:c(H2A)+c(HA-)+c(A2-)=0.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为Zn-聚苯胺二次电池的示意图,下列说法正确的是( )
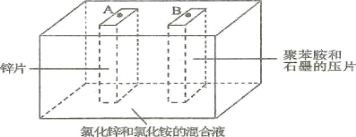
A.放电时,Zn片做负极,发生的电极方程式为Zn + 2e-=Zn2+
B.放电时,混合液中的Cl-向B移动
C.充电时,聚苯胺被氧化
D.充电时,A端接电源的正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼是新型无机材料中的明星元素。

(1)磷化硼是一种耐磨涂料,可由三溴化硼和三溴化磷高温下在氢气中反应合成,其化学方程式为 ______,图为磷化硼晶体结构中最小的重复单元,磷化硼的晶体类型是 ______,一个晶胞中含 ______个P原子,每个B或P均形成4个共价键,其中有一个配位键,提供空轨道的是 ______原子。
(2)氮化硼是一种重要的功能陶瓷材料,其结构与磷化硼相似,B和N相比,电负性较大的是 ______(填元素符号),其基态原子的电子排布式为 ______,氮化硼中B元素的化合价为 ______。
(3)环硼氮烷与苯是等电子体,其一氯代物有两种结构、二氯代物有四种结构,写出环硼氮烷分子结构式 ______。
(4)BF3用作有机合成中的催化剂,也用于制造火箭的高能燃料。在BF3分子中,F-B-F的键角是 ______ 度,B原子采用 ______ 杂化;BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为 ______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com