
ˇľĚâÄżˇżÂČ»ŻŃÇÍŁ¨CuClŁ©łŁÓĂÓÚ´ß»ŻĽÁˇ˘ŃŐÁϡ˘·Ŕ¸ŻµČą¤ŇµˇŁÄłĐËȤС×éÉčĽĆʵŃéÖƱ¸ÂČ»ŻŃÇ͡Ł»Ř´đĎÂÁĐÎĘĚ⣺

ÖĆ·¨Ň»Łş˝«Í·ŰĽÓČëB·´Ó¦Ć÷ÖĐŁ¬ÓëŇ»¶¨Ĺ¨¶ČµÄĘłŃΡŞŃÎËáČÜŇşĎ໥×÷ÓĂŁ¬ÔÚ60ˇ«70ˇćͨČëŃőĆřŁ¬łä·Ö·´Ó¦Ł¨˛ż·ÖŇÇĆ÷ÂÔČĄŁ©ˇŁ
˘ŮŇÇĆ÷XµÄĂűłĆ___Ł¬XÖĐʢÓжţŃő»ŻĂĚŁ¬·ÖҺ©¶·ÖĐʢ·ĹË«ŃőË®Ł¬ÔňA×°ÖĂÖĐ·˘Éú·´Ó¦µÄ»ŻŃ§·˝łĚĘ˝ĘÇ___ˇŁ

˘Ú·´Ó¦˝áĘřşóŁ¬´ňżŞĆżČű aŁ¬Çăłö·´Ó¦ŇşÓÚ´óÉŐ±ÖĐŁ¬ÎŞ·ŔÖąÍ⽦Ł¬Í¨łŁ˛ÉÓõIJŮ×÷·˝·¨ĘÇ___ˇŁ
ÖĆ·¨¶ţŁş˝«ÂČ»ŻÍÓëÂČ»ŻÄĆĽÓË®Čܽ⣬˛˘µ÷˝ÚËá¶ČŁ¬ĽÓČëÍ·ŰŇ»ĆđĽÓČČŁ¬Cu2+±»µĄÖĘÍ»ąÔŁ¬ÉúłÉżÉČÜĐÔµÄĹäşĎÎďNa[CuCl2]Ł¬Ôپˮ˝âşó˛úÉú°×É«łÁµíˇŁłéÂËŁ¬łÁµíŇŔ´ÎÓĂË®ˇ˘ÎŢË®ŇŇ´ĽĎ´µÓ¶ŕ´ÎŁ¬µĂ°×É«ąĚĚĺ˛úĆ·
˘ŮĐ´łö¸Ă·¨ÉúłÉNa[CuCl2]µÄ»ŻŃ§·´Ó¦·˝łĚĘ˝___ˇŁ
˘ÚÓĂˮϴµÓCuClłÁµíµÄľßĚĺ˛Ů×÷ÎŞ___Ł¬łÁµíˮϴşóÔŮÓĂÎŢË®ŇŇ´ĽĎ´µÓµÄÔŇňĘÇ___ˇŁ
˘ŰĹжĎCuClĘÇą˛ĽŰ»ŻşĎÎﻹĘÇŔë×Ó»ŻşĎÎďµÄʵŃé·˝·¨ĘÇ___ˇŁ
ÖĆ·¨ČýŁşŇÔÍÎŞµçĽ«Ł¬µç˝â±ĄşÍĘłŃÎˮҲżÉÖƵĂCuClˇŁŃôĽ«µÄµçĽ«·´Ó¦Ę˝ÎŞ___ˇŁ
ˇľ´đ°¸ˇż×¶ĐÎĆż 2H2O2 ![]() 2H2ˇü+O2ˇü ÓòŁÁ§°ôŇýÁ÷ Cu+CuCl2+2NaCl
2H2ˇü+O2ˇü ÓòŁÁ§°ôŇýÁ÷ Cu+CuCl2+2NaCl![]() 2Na[CuCl2] ŃزŁÁ§°ôĎňąýÂËĆ÷ÖĐĽÓŐôÁóË®ÖÁ˝ţĂ»łÁµíŁ¬´ýË®×ÔČ»Á÷ľˇŁ¬Öظ´˛Ů×÷2~3´Î ´ĽĎ´żÉŇÔżěËŮČĄłýCuCl±íĂćµÄË®Ł¬·ŔÖąĆä±»Ńő»Ż ˛â¶¨ČŰČÚ̬µÄCuClµÄµĽµçĐÔ Cu+Cl- -e-=CuCl
2Na[CuCl2] ŃزŁÁ§°ôĎňąýÂËĆ÷ÖĐĽÓŐôÁóË®ÖÁ˝ţĂ»łÁµíŁ¬´ýË®×ÔČ»Á÷ľˇŁ¬Öظ´˛Ů×÷2~3´Î ´ĽĎ´żÉŇÔżěËŮČĄłýCuCl±íĂćµÄË®Ł¬·ŔÖąĆä±»Ńő»Ż ˛â¶¨ČŰČÚ̬µÄCuClµÄµĽµçĐÔ Cu+Cl- -e-=CuCl
ˇľ˝âÎöˇż
ÖĆ·¨Ň»Łş˘Ů¸ůľÝŇÇĆ÷˝áąąşÍĐÔÄÜČ·¶¨ŇÇĆ÷XµÄĂűłĆŁ»A×°ÖĂH2O2ÔÚMnO2µÄ´ß»Ż×÷ÓĂĎ·ֽâÉúłÉŃőĆřŁ»
˘ÚתŇĆŇşĚĺʱżÉĘąÓòŁÁ§°ôŇýÁ÷Ł»
ÖĆ·¨¶ţŁş˘ŮÂČ»ŻÍÓëÂČ»ŻÄĆĽÓË®Čܽ⣬˛˘µ÷˝ÚËá¶ČŁ¬ĽÓČëÍ·ŰŇ»ĆđĽÓČČŁ¬Cu2+±»µĄÖĘÍ»ąÔŁ¬ÉúłÉżÉČÜĐÔµÄĹäşĎÎďNa[CuCl2]Ł¬˝áşĎÔ×ÓĘŘşăżÉĐ´łö»ŻŃ§·´Ó¦·˝łĚĘ˝Ł»
˘ÚĎ´µÓCuClłÁµíżÉÔÚąýÂËĆ÷ÖĐÖ±˝ÓĽÓČëŐôÁóË®Ľ´żÉŁ¬CuCl˛»ČÜÓÚ´ĽŔࣻ
˘ŰŔë×Ó»ŻşĎÎďČŰČÚ״̬ĎÂÄÜ·˘ÉúµçŔ룬¶řą˛ĽŰ»ŻşĎÎďÔÚČŰČÚ״̬Ď²»ÄÜ·˘ÉúµçŔ룻
ÖĆ·¨ČýŁşµç˝âłŘµÄŃôĽ«·˘ÉúŃő»Ż·´Ó¦Ł¬ÇŇCuÎŞ»îĐԵ缫Ł¬˝áşĎµç˝â˛úÎďÎŞCuĐ´łöŃôĽ«µçĽ«·´Ó¦Ę˝ˇŁ
ÖĆ·¨Ň»Łş˘Ů×°ÖĂAÖĐŇÇĆ÷XµÄĂűłĆΪ׶ĐÎĆżŁ»×¶ĐÎĆżÖĐH2O2ÔÚMnO2µÄ´ß»Ż×÷ÓĂĎ·ֽâÉúłÉŃőĆřŁ¬·˘Éú·´Ó¦µÄ»ŻŃ§·˝łĚʽΪ2H2O2 ![]() 2H2ˇü+O2ˇüŁ»
2H2ˇü+O2ˇüŁ»
˘Ú·´Ó¦˝áĘřşóŁ¬´ňżŞĆżČű aŁ¬Çăłö·´Ó¦ŇşÓÚ´óÉŐ±ÖĐŁ¬ÎŞ·ŔÖąÍ⽦Ł¬żÉĘąÓòŁÁ§°ôŇýÁ÷Ł»
ÖĆ·¨¶ţŁş˘ŮÂČ»ŻÍÓëÂČ»ŻÄĆĽÓË®Čܽ⣬˛˘µ÷˝ÚËá¶ČŁ¬ĽÓČëÍ·ŰŇ»ĆđĽÓČČŁ¬Cu2+±»µĄÖĘÍ»ąÔŁ¬ÉúłÉżÉČÜĐÔµÄĹäşĎÎďNa[CuCl2]Ł¬·˘Éú·´Ó¦µÄ»ŻŃ§·´Ó¦·˝łĚʽΪCu+CuCl2+2NaCl![]() 2Na[CuCl2]Ł»
2Na[CuCl2]Ł»
˘ÚĎ´µÓCuClłÁµíµÄľßĚĺ˛Ů×÷ÎŞŃزŁÁ§°ôĎňąýÂËĆ÷ÖĐĽÓŐôÁóË®ÖÁ˝ţĂ»łÁµíŁ¬´ýË®×ÔČ»Á÷ľˇŁ¬Öظ´˛Ů×÷2~3´ÎŁ»łÁµíˮϴşóÔŮÓĂÎŢË®ŇŇ´ĽĎ´µÓµÄÔŇňĘÇ´ĽĎ´żÉŇÔżěËŮČĄłýCuCl±íĂćµÄË®Ł¬Í¬Ę±·ŔÖąĆä±»Ńő»ŻŁ»
˘ŰŔë×Ó»ŻşĎÎďČŰČÚ״̬ĎÂÄÜ·˘ÉúµçŔ룬¶řą˛ĽŰ»ŻşĎÎďÔÚČŰČÚ״̬Ď²»ÄÜ·˘ÉúµçŔ룬ÔňżÉͨąý˛â¶¨ČŰČÚ̬µÄCuClÄÜ·ńµĽµçĹжĎĹжĎCuClĘÇą˛ĽŰ»ŻşĎÎﻹĘÇŔë×Ó»ŻşĎÎ
ÖĆ·¨ČýŁşµç˝âłŘµÄŃôĽ«·˘ÉúŃő»Ż·´Ó¦Ł¬ÇŇCuÎŞ»îĐԵ缫Ł¬ÔňŃôĽ«µçĽ«·´Ó¦Ę˝ÎŞCu+Cl- -e-=CuClˇŁ


 »Ć¸ÔşŁµíČ«łĚĹŕÓŲâĘÔľíϵÁĐ´đ°¸
»Ć¸ÔşŁµíČ«łĚĹŕÓŲâĘÔľíϵÁĐ´đ°¸
| Ä꼶 | ¸ßÖĐżÎłĚ | Ä꼶 | łőÖĐżÎłĚ |
| ¸ßŇ» | ¸ßŇ»Ăâ·ŃżÎłĚÍĆĽöŁˇ | łőŇ» | łőŇ»Ăâ·ŃżÎłĚÍĆĽöŁˇ |
| ¸ß¶ţ | ¸ß¶ţĂâ·ŃżÎłĚÍĆĽöŁˇ | łő¶ţ | łő¶ţĂâ·ŃżÎłĚÍĆĽöŁˇ |
| ¸ßČý | ¸ßČýĂâ·ŃżÎłĚÍĆĽöŁˇ | łőČý | łőČýĂâ·ŃżÎłĚÍĆĽöŁˇ |
żĆÄżŁş¸ßÖĐ»ŻŃ§ Ŕ´Ô´Łş ĚâĐÍŁş
ˇľĚâÄżˇżĎÂÁĐÖ¸¶¨·´Ó¦µÄ·˝łĚĘ˝ŐýČ·µÄĘÇ
A.µç˝âÂČ»ŻĂľČÜŇşŁş2Cl¨C+2H2O![]() H2ˇü+Cl2ˇü+2OH¨C
H2ˇü+Cl2ˇü+2OH¨C
B.ĚĽËáÇâď§ČÜŇşÖĐĽÓČë×ăÁżĘŻ»ŇË®ŁşCa2++![]() +OH¨C=CaCO3ˇý+H2O
+OH¨C=CaCO3ˇý+H2O
C.Al2(SO4)3ČÜŇşÖĐĽÓČëąýÁż°±Ë®ŁşAl3++3NH3ˇ¤H2O=Al(OH)3ˇý+3NH4+
D.ÇâŃő»Ż±µČÜŇşÖĐĽÓČëϡÁňË᣺HŁ«(aq)Ł«OHŁ(aq)=H2O(l)ˇˇ¦¤HŁ˝Ł57.3 kJˇ¤molŁ1
˛éż´´đ°¸şÍ˝âÎö>>
żĆÄżŁş¸ßÖĐ»ŻŃ§ Ŕ´Ô´Łş ĚâĐÍŁş
ˇľĚâÄżˇżŃˇÓĂČçÍĽËůĘľŇÇĆ÷ÖеÄÁ˝¸ö»ňĽ¸¸ö(ÄÚş¬ÎďÖĘ)×é×°łÉʵŃé×°ÖĂŁ¬ŇÔŃé֤ľ̿żÉ±»Ĺ¨ÁňËáŃő»ŻłÉCO2Ł¬ĎÂÁĐ˵·¨ŐýČ·µÄĘÇ(ˇˇˇˇ)
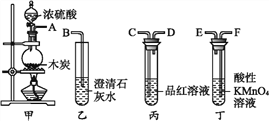
A.°´ĆřÁ÷´Ó×óĎňÓŇÁ÷¶ŻŁ¬Á¬˝Ó×°ÖõÄŐýČ·ËłĐňĘÇAˇúFˇúEˇúCˇúDˇúB
B.¶ˇÖĐČÜŇşÍĘÉ«Ł¬ŇŇÖĐČÜŇş±ä»ë×ÇŁ¬ËµĂ÷Ľ×ÖĐÉúłÉCO2
C.±űÖĐĆ·şěČÜŇşÍĘÉ«Ł¬ŇŇÖĐČÜŇş±ä»ë×ÇŁ¬ËµĂ÷Ľ×ÖĐÉúłÉCO2
D.¶ˇşÍ±űÖĐČÜŇş¶ĽÍĘÉ«Ł¬ŇŇÖĐČÜŇş±ä»ë×ÇŁ¬ËµĂ÷Ľ×ÖĐÓĐCO2ÉúłÉ
˛éż´´đ°¸şÍ˝âÎö>>
żĆÄżŁş¸ßÖĐ»ŻŃ§ Ŕ´Ô´Łş ĚâĐÍŁş
ˇľĚâÄżˇżÄłą¤ł§ÓĂÁůË®şĎÂČ»ŻĂľşÍ´ÖĘŻ»ŇÖĆȡµÄÇâŃő»ŻĂľş¬ÓĐÉŮÁżÇâŃő»ŻĚúÔÓÖĘŁ¬Í¨ąýČçĎÂÁ÷łĚ˝řĐĐĚá´żľ«ÖĆŁ¬»ńµĂ×čČĽĽÁÇâŃő»ŻĂľˇŁĎÂÁĐ˵·¨˛»ŐýČ·µÄĘÇ
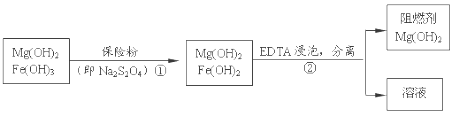
A. ˛˝Öč˘ÚÖĐ·ÖŔë˛Ů×÷µÄĂűłĆĘÇąýÂËŁ¬Mg(OH)2żÉŇÔ×÷×čČĽĽÁĘÇŇňÎŞËü·Ö˝âĐčŇŞÎüĘŐ´óÁżµÄČČ
B. ˛˝Öč˘ŮÖеķ´Ó¦Ę˝Łş3Fe(OH)3 Ł«S2O42-Ł«2OH- Ł˝3Fe(OH)2 Ł«2SO42-Ł«4H2O
C. ˛˝Öč˘ŮÖбŁĎŐ·ŰĘÇ×÷»ąÔĽÁ
D. ´Ó˛˝Öč˘Ú ÖĐżÉÖŞOH- şÍEDTAą˛´ćʱŁ¬Fe2+¸üŇ׺ÍEDTA˝áşĎŁ¬ÉúłÉżÉČÜĐÔ»ŻşĎÎď
˛éż´´đ°¸şÍ˝âÎö>>
żĆÄżŁş¸ßÖĐ»ŻŃ§ Ŕ´Ô´Łş ĚâĐÍŁş
ˇľĚâÄżˇżÔÚ1-18şĹµÄ¶ĚÖÜĆÚÖ÷×ĺÔŞËŘÖĐŁ¬±íÖеÄ×Öĸ´ú±íŇ»ÖÖÔŞËŘŁ¬»Ř´đĎÂÁĐÎĘĚ⣺
A | |||||||||
C | D | ||||||||
B | E | F | |||||||
Ł¨1Ł©»łöDµÄÔ×ӽṹʾŇâÍĽ________ Ł»
Ł¨2Ł©AşÍFÁ˝ÖÖÔŞËŘ×éłÉµÄ»ŻşĎÎďÖĐş¬ÓеĻŻŃ§ĽüĘÇ_____Ł¨Ěą˛ĽŰˇ±»ňˇ°Ŕë×Óˇ±Ł©ĽüˇŁŁ»
Ł¨3Ł©EşÍF·Ö±đĐγɵÄĆř̬Ç⻯ÎďÖĐ×îÎȶ¨µÄĘÇ_________Ł¨ĚîĐ´Ç⻯ÎďµÄ»ŻŃ§Ę˝Ł©
Ł¨4Ł©BµÄ×î¸ßĽŰŃő»ŻÎďµÄË®»ŻÎďµÄ»ŻŃ§Ę˝_____________ˇŁ
˛éż´´đ°¸şÍ˝âÎö>>
żĆÄżŁş¸ßÖĐ»ŻŃ§ Ŕ´Ô´Łş ĚâĐÍŁş
ˇľĚâÄżˇżČçÍĽÖĐŁ¬Á˝µçĽ«ÉĎ·˘ÉúµÄµçĽ«·´Ó¦ÎŞaĽ«ŁşCu2Ł«Ł«2e-=CuŁ»bĽ«ŁşFeŁ2e-=Fe2Ł«ˇŁĎÂÁĐ˵·¨˛»ŐýČ·µÄĘÇ
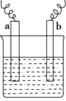
A.µç˝âÖĘČÜŇşş¬ÓĐCu2Ł«
B.¸Ă×°ÖĂĘÇ»ŻŃ§ÄÜת»ŻÎ޵çÄÜ
C.aˇ˘bżÉÄÜĘÇͬÖֵ缫˛ÄÁĎ
D.aĽ«ÉĎ·˘Éú»ąÔ·´Ó¦
˛éż´´đ°¸şÍ˝âÎö>>
żĆÄżŁş¸ßÖĐ»ŻŃ§ Ŕ´Ô´Łş ĚâĐÍŁş
ˇľĚâÄżˇżÓĐAˇ˘Bˇ˘Cˇ˘Dˇ˘EÎĺÖÖ¶ĚÖÜĆÚÔŞËŘŁ¬ĆäÖĐDÓëAˇ˘Bˇ˘CľůÄÜĐÎłÉÔ×Ó¸öĘý±ČÎŞ1ˇĂ1Óë1ˇĂ2µÄÁ˝Ŕ໯şĎÎďXˇ˘YŁ¬EµÄÄłÖÖş¬ŃőËá»ňş¬ŃőËáŃÎÔÚŇ»¶¨ĚőĽţĎ¿ɷֽâÉúłÉDµÄµĄÖʡŁ
(1)ÓÉÉĎĘöĚőĽţżÉŇÔČ·¶¨µÄÔŞËرŕşĹĽ°¶ÔÓ¦ÔŞËŘĂűłĆĘÇ____________Ł¬ĆäÖĐÔ×ÓĽäͨąýą˛ÓĂŇ»¶Ôµç×Ó¶řĐγɵĵĄÖʵĵç×ÓʽΪ________________Ł¬EÄÜĐγɶŕÖÖş¬ŃőËᣬĆäÖĐËáĐÔ×îÇżµÄş¬ŃőËáµÄ·Ö×ÓʽΪ______________ˇŁ
(2)ČôËůÓĐżÉÄܵÄXˇ˘YÖĐŁ¬Cˇ˘DĐγɵÄĘÇŔë×Ó»ŻşĎÎĆäÖĐŇ»ÖÖÎďÖĘÖĐş¬ÓĐÁ˝Ŕ໯ѧĽüŁ¬ÄÇĂ´ÁíŇ»ÖÖÎďÖʵÄĐγɹýłĚÓõç×ÓĘ˝żÉ±íʾΪ______________________________________ˇŁ
(3)ČôÉĎĘöXˇ˘Y´ćÔÚČçϱ仯ŁşXŁ«YˇúZŁ«D2Ł¬ÇŇXˇ˘YÖи÷Ô×Ó(Ŕë×Ó)×îÍâ˛ăÉĎľůÓĐ8¸öµç×ÓŁ¬Ôň¸Ă·´Ó¦µÄ»ŻŃ§·˝łĚʽΪ__________________Ł¬·´Ó¦ÎďÖĐ´ćÔÚ·ÇĽ«ĐÔĽüµÄÎďÖĘĘÇ__________Ł¬ÉúłÉÎďÖĐ´ćÔÚ·ÇĽ«ĐÔĽüµÄÎďÖĘĘÇ_____________Ł¬ÓÉ´Ë˵Ă÷»ŻŃ§·´Ó¦µÄ±ľÖĘĘÇ________________ˇŁ
˛éż´´đ°¸şÍ˝âÎö>>
żĆÄżŁş¸ßÖĐ»ŻŃ§ Ŕ´Ô´Łş ĚâĐÍŁş
ˇľĚâÄżˇżÄłżą˝áł¦Ń×Ň©ÎďµÄÓĐЧłÉ·ÖŁ¨RŁ©µÄ˝áąąĽňĘ˝ČçĎ¡ŁĎÂÁĐ˵·¨˛»ŐýČ·µÄĘÇ

A. RÄÜ·˘ÉúĽÓłÉˇ˘Čˇ´ú·´Ó¦
B. R·Ö×ÓÖĐËůÓĐCşÍNÔ×ÓŇ»¶¨ą˛Ć˝Ăć
C. RµÄ±˝»·ÉĎąŮÄÜÍĹλÖĂŇěąąĚĺÓĐ10ÖÖ
D. RµÄ·Ö×ÓʽΪC7H7O3N
˛éż´´đ°¸şÍ˝âÎö>>
żĆÄżŁş¸ßÖĐ»ŻŃ§ Ŕ´Ô´Łş ĚâĐÍŁş
ˇľĚâÄżˇżÄłĘµŃéС×éÖƱ¸˛ÝËᾧĚĺ(H2C2O4ˇ¤2H2O)µÄʵŃé×°ÖĂČçĎÂŁş
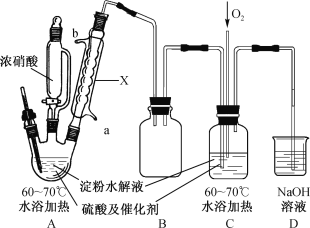
ŇŃÖŞŁşI.˛ÝËá(H2C2O4)ĘǶţÔŞČőËᣬČ۵ă101ˇ«102ˇćŁ»
II.˛ÝËáµÄČÜ˝â¶ČČçϱíËůĘľŁş
ζČ/ˇć | 20 | 30 | 40 | 50 | 60 | 70 |
ČÜ˝â¶Č/gˇ¤(100gË®)Ł1 | 9.5 | 14.3 | 21.2 | 31.4 | 46.0 | 84.5 |
III.ÔÚ´ß»ŻĽÁşÍÁňËá´ćÔÚĎÂŁ¬ÓĂŨĎőËáŃő»Żµí·ŰË®˝âŇşżÉÖƱ¸˛ÝËᣬ·˘ÉúµÄÖ÷ŇŞ·´Ó¦ÎŞŁş
C6H12O6Ł«12HNO3ˇú3H2C2O4Ł«9NO2ˇüŁ«3NOˇüŁ«9H2OˇŁ
»Ř´đĎÂÁĐÎĘĚ⣺
(1)×°ÖĂAÖĐŇÇĆ÷XĂűłĆÎŞ___________Ł¬Ë®´Ó˝ÓżÚ___________(Ěaˇ±»ňˇ°bˇ±)˝řČ롣
(2)×°ÖĂBµÄ×÷ÓĂĘÇ___________Ł»ÉčĽĆ×°ÖĂCµÄÄżµÄĘÇ_________________________ˇŁ
(3)·´Ó¦C6H12O6Ł«12HNO3ˇú3H2C2O4Ł«9NO2ˇüŁ«3NOˇüŁ«9H2OÖĐŁ¬ĂżÉúłÉ1 mol H2C2O4תŇƵç×ÓµÄÎďÖʵÄÁżÎŞ____________ˇŁ
(4)˝«×°ÖĂAşÍCÖĐ·´Ó¦ŇşĹ¨Ëőˇ˘ľ˛Öýᾧ˛˘ąýÂ˵ôֲÝËᾧĚ壬Ěá´żH2C2O4ˇ¤2H2OµÄ·˝·¨ĘÇ_________________________ˇŁ
(5)Ě˝ľż˛ÝËáµÄĐÔÖĘŁş
˘ŮĎňNa2CO3ČÜŇşÖеμÓH2C2O4ČÜŇşŁ¬˛úÉú´óÁżĆřĚ壬˵Ă÷˛ÝËáµÄËáĐÔ±ČĚĽËá________(Ěǿˇ±»ňˇ°Čőˇ±)ˇŁ
˘ÚĎňNaClOČÜŇşÖĐĽÓČëąýÁżH2C2O4ČÜŇşŁ¬ÓĐĆřĹݲúÉúŁ¬ÄÜ˝âĘÍŐâŇ»ĎÖĎóµÄŔë×Ó·˝łĚʽΪ___ˇŁ
˛éż´´đ°¸şÍ˝âÎö>>
ąúĽĘѧУÓĹѡ - Á·Ď°˛áÁбí - ĘÔĚâÁбí
şţ±±Ęˇ»ĄÁŞÍřÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨Ć˝Ě¨ | ÍřÉĎÓĐş¦ĐĹϢľŮ±¨×¨Çř | µçĐĹթƾٱ¨×¨Çř | ÉćŔúĘ·ĐéÎŢÖ÷ŇĺÓĐş¦ĐĹϢľŮ±¨×¨Çř | ÉćĆóÇÖȨľŮ±¨×¨Çř
ÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨µç»°Łş027-86699610 ľŮ±¨ÓĘĎ䣺58377363@163.com