
【题目】甲、乙两烧瓶中各盛有100mL 5mol·L-1的盐酸和氢氧化钾溶液;向两烧瓶中分别加入等质量的铝粉,反应结束测得生成的气体体积甲∶乙=2∶3(相同状况),则加入铝粉的质量为( )
A.2.7gB.3.6gC.5.4gD.6.75g
【答案】D
【解析】
铝的质量相同,盐酸和氢氧化钠溶液中溶质的物质的量相同,若Al都完全反应,则生成氢气应相等,而应结束后测得生成的气体体积比为甲:乙=2:3,由方程式:![]() 、
、![]() ,可知相同物质的量的Al反应时,消耗HCl较多,故酸与金属反应时酸不过量,碱与金属反应时碱过量,结合方程式计算解答.
,可知相同物质的量的Al反应时,消耗HCl较多,故酸与金属反应时酸不过量,碱与金属反应时碱过量,结合方程式计算解答.
盐酸与铝的离子反应式为:![]() ,KOH与铝的离子反应式为:
,KOH与铝的离子反应式为:![]() ,所以等物质的量的铝分别与足量的盐酸和氢氧化钾溶液反应,消耗的氢氧化钾溶液的量比盐酸少;而本题中反应结束测得生成的气体体积甲∶乙=2∶3,故盐酸少量,则与盐酸反应生成的氢气为
,所以等物质的量的铝分别与足量的盐酸和氢氧化钾溶液反应,消耗的氢氧化钾溶液的量比盐酸少;而本题中反应结束测得生成的气体体积甲∶乙=2∶3,故盐酸少量,则与盐酸反应生成的氢气为![]() ,故与KOH溶液反应生成的氢气为
,故与KOH溶液反应生成的氢气为![]() 。KOH溶液足量,加入其中的铝完全反应。故可求得
。KOH溶液足量,加入其中的铝完全反应。故可求得![]() 。
。
综上所述,本题正确答案为D。


科目:高中化学 来源: 题型:
【题目】有机化合物 X(![]() )是合成重要医药中间体的原料。下列关于化合物X说法错误的是
)是合成重要医药中间体的原料。下列关于化合物X说法错误的是
A.分子中有 7 个碳原子共平面
B.能使酸性 KMnO4 溶液褪色
C.能与 HBr 发生加成反应
D.X 的同分异构体中不存在芳香族化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一镁铝合金共51 g,把其加入到1 L 5 mol·L-1的盐酸中,恰好反应完。
(1)关于合金的下列说法正确的有________。
A.合金只能由两种或两种以上的金属组成
B.合金的硬度一般比其组成成分金属的硬度大
C.镁铝熔成合金的过程是一个化学过程
D.合金的熔点一般比其组成成分的熔点低
E.合金具备金属的特性
(2) 该合金中镁铝的质量分别为________g、________g。
(3) 反应中共收集到标况下的氢气的体积为___________L。
(4)向反应后的溶液中逐滴加入5 mol·L-1的NaOH溶液,若要使沉淀恰好达到最大值,需要加入NaOH________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某组甲乙同学进行稀硫酸与锌制取氢气的实验,请回答下列问题:
(1)甲同学发现加入少量硫酸铜溶液可加快氢气的生成速率。为了进一步研究硫酸铜的量对氢气生成速率的影响,设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
实验 混合溶液 | A | B | C | D | E | F |
4 mol·L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1=___,V6=___,V9=___;
②反应一段时间后,实验A中的金属呈___色,实验E中的金属呈___色;
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因___________________________。
(2)乙同学为了探究锌与稀硫酸反应过程中的速率及能量的变化,进行以下实验,分析影响反应速率的因素。
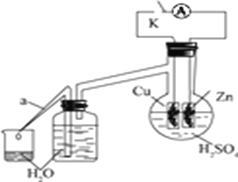
实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1分钟内从a管流出的水滴数,得到的水滴数如下表所示:
1分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
1分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
分析反应过程中的水滴数,请回答:
① 由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率快,主要原因是__________________________________________________________。
② 由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像中的曲线(纵坐标为沉淀或气体的量,横坐标为加入物质的量),其中错误的是
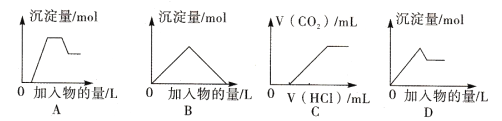
A. 图A表示向含H+、Mg2+、Al3+、NH4+的溶液中滴加NaOH溶液产生沉淀量的关系曲线
B. 图B表示向澄清石灰水中通入二氧化碳直至过量产生沉淀量的关系曲线
C. 图C表示向NaOH和Na2CO3的混合液中滴加盐酸产生CO2气体的关系曲线
D. 图D表示向明矾溶液中滴加Ba(OH)2溶液产生沉淀量的关系曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究硫酸亚铁的分解产物,将硫酸亚铁装入下图所示的装置a中,打开K1和K2缓缓通入N2加热。实验后反应管中残留固体为红色粉末。下列说法中正确的是
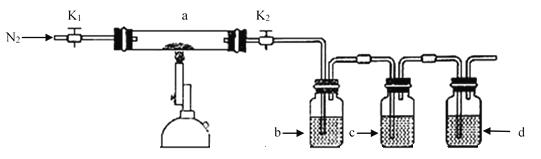
A.分解的气体产物中有SO3、SO2应该先检验SO3
B.装置b中的试剂为Ba(NO3)2溶液,反应后有白色沉淀生成,证明分解产物中有SO3气体
C.装置c中的试剂为酸性KMnO4溶液,作用是除去混合气体中的SO2
D.装置d之后需要增加尾气处理装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫单质及其化合物在化工生成等领城应用广泛。
(1)工业尾气中的SO2一直是环境污染的主要原因之一,工业上常采用如下方法降低尾气中的含硫量:
①方法 1: 燃煤中加入生石灰,将SO2转化为 CaSO3,再氧化为CaSO4。
已知:a. CaO(s) +CO2 (g)=CaCO3 △H=-1 78.3kJmol-1
b. 2CaCO3(s) +2SO2(g) +O2(g)=2CaSO4(s) +2CO2(g) △H=-2762.2kJmol-1
c.2 CaSO3(s) + O2(g)=2CaSO4(s) △H =-2314.8 kJmol-1
写出CaO(s)与SO2(g)反应生成CaSO3(s)的热化学方程式:_____________。
②方法 2:用氨水将SO2转化为NH4HSO3 ,再氧化为(NH4)2SO4。实验测得NH4HSO3溶液中![]() = 1500 ,则溶液的pH 为_____________(已知:HSO3-的Ka1=1.5×l0-2, Ka2=l.0×l0-7)。
= 1500 ,则溶液的pH 为_____________(已知:HSO3-的Ka1=1.5×l0-2, Ka2=l.0×l0-7)。
(2)煤制得的化工原料气中含有羰基硫(O=C =S),该物质可转化为H2S,反应为COS(g)+ H2( g ) ![]() H2S(g) +CO(g) △H > 0。
H2S(g) +CO(g) △H > 0。
①恒温恒容条件下,密闭容器中发生上述反应,下列事实不能说明反应达到平衡状态的是________________(填字母)。
a.COS的浓度保持不变 b. 化学平衡常数不再改变
c.混合气体的密度不再改变 d. 形成 2 mol H-S 键的同时形成 1 mol H-H 键
②T℃时 ,在恒容的密闭容器中 ,将定量的CO和H2S 混合加热并达到下列平衡:H2S(g) + CO(g)![]() COS(g) + H2(g),K=0.25,则该温度下反应 COS(g) +H2(g)=H2S(g) +CO(g)的平衡常数K __________。T1℃ 时,向容积为 10 L 的恒容密闭容器中充入 1 molCOS(g)和1 mol H2 (g),达到平衡时 COS 的转化率为_______。
COS(g) + H2(g),K=0.25,则该温度下反应 COS(g) +H2(g)=H2S(g) +CO(g)的平衡常数K __________。T1℃ 时,向容积为 10 L 的恒容密闭容器中充入 1 molCOS(g)和1 mol H2 (g),达到平衡时 COS 的转化率为_______。
(3)过二硫酸(H2S2O8)是一种强氧化性酸,其结构式如图所示: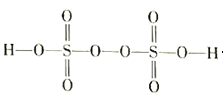
①在Ag+催化作用下,S2O82-能与 Mn2+ 在水溶液中发生反应生成SO42-和 MnO4-,1 molS2O82-能氧化的 Mn2+ 的物质的量为_____________mol。
②工业上可用惰性电极电解硫酸和硫酸铵混合溶液制备过二硫酸铵。则阳极的电极反应式为______________________。
(4)NaHS 可用作处理含 Hg2+的污水的沉淀剂,已知 25℃时,反应 Hg2+(aq) + HS-( aq) ![]() HgS(s) + H+(aq) 的平衡常数 K=l.75×l038 ,H2S的电离平衡常数Ka1=1.3×l0-7 , Ka2= 7.0×l 0-15,则Ksp(HgS) =__________________。
HgS(s) + H+(aq) 的平衡常数 K=l.75×l038 ,H2S的电离平衡常数Ka1=1.3×l0-7 , Ka2= 7.0×l 0-15,则Ksp(HgS) =__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)25 ℃时,将体积Va、pH=a的某一元强碱与体积为Vb、pH=b的某二元强酸混合。
①若所得溶液的pH=11,且a=13,b=2,则Va∶Vb=____________。
②为了更好的表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG的定义为AG=lg![]() 。25 ℃时,若溶液呈中性,则AG=___,溶液的pH与AG的换算公式为AG=_____。
。25 ℃时,若溶液呈中性,则AG=___,溶液的pH与AG的换算公式为AG=_____。
(2)常温下,浓度均为0.1molL-1的下列五种钠盐溶液的pH如下表:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
①上述盐溶液中的阴离子,结合H+能力最强的是____。
②根据表中数据,浓度均为0.01 molL-1的下列四种酸的溶液分别稀释100倍,pH变化最大的是__(填编号)。
A.HCN B.HClO C.CH3COOH D.H2CO3
(3)已知常温下,Ksp[Fe(OH)3]=4.0×10-38,在FeCl3溶液中加入NaHCO3溶液产生沉淀和气体,反应的离子方程式为:_______;若将所得悬浊液的pH调整为4,则溶液中Fe3+浓度为__mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应:2SO2(g)+O2(g)![]() 2SO3(g)(正反应放热),如图是某次实验的化学反应速率随时间变化的图像,推断在t1时刻突然变化的条件可能是( )
2SO3(g)(正反应放热),如图是某次实验的化学反应速率随时间变化的图像,推断在t1时刻突然变化的条件可能是( )

A. 催化剂失效 B. 减小生成物的浓度
C. 降低体系温度 D. 增大容器的体积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com