
���� ��1������CO2��g��+H2��g��?CO ��g��+H2O ��g����H=+41kJ/mol����H��0Ϊ���ȷ�Ӧ��
��2����ѧƽ���־�����淴Ӧ������ͬ������ֺ������ֲ��䣬���ɴ�������һЩ������Ҳ���䣬�Դ˽��
��3��Ҫ���CO2��ת���ʣ�Ӧʹƽ��������Ӧ����ϻ�ѧƽ���ƶ�ԭ��������
��4����2C��ʯī��+O2��g��=2CO��g����H1=-222kJ/mol��
��H2��g��+$\frac{1}{2}$O2��g��=H2O ��g����H2=-242kJ/mol��
��CO2��g��+H2��g��?CO ��g��+H2O ��g����H=+41kJ/mol��
���ݸ�˹���ɣ��١�$\frac{1}{2}$+��-�ۼ���õ���
��� �⣺��1����ΪCO2��g��+H2��g��?CO ��g��+H2O ��g����H=+41kJ/mol����H��0����÷�Ӧ����Ϊ���ȷ�Ӧ���ʴ�Ϊ�����ȣ���H��0��
��2��a���淴Ӧ����CO��Ũ�������������n��CO�����䣬˵����Ӧ����ƽ�⣬��a��ȷ��
b��v������CO2��=v������CO��������ָ������Ӧ��������˵����Ӧ����ƽ�⣬��b����
c����Ϊ��Ӧǰ����������ʵ������䣬���Ի�����������ʵ���һֱ���䣬����˵����Ӧ����ƽ�⣬��c����
d����������ɫ���䣬˵��������Ũ�Ȳ��䣬˵����Ӧ����ƽ�⣬��d��ȷ��
e��c��CO��=c��H2O��ʱ���ܴ���ƽ��״̬�����ܲ�����ƽ��״̬���뷴Ӧ�������йأ��������̼��ת�����йأ���e����
��ѡ��ad��
��3��a������ϵ��ͨ��CO2����Ȼƽ��������Ӧ�����ƶ�������Ϊ���ӵ���CO2������CO2ת���ʼ�С���ʴ���
b�����ڷ�Ӧ���ȣ������¶�ƽ��������Ӧ�����ƶ���CO2ת����������ȷ��
c����Ϊһ�������µ��ܱ������У�����ϵ��ͨ��������壬ƽ�ⲻ�ƶ�������CO2ת���ʲ��䣬�ʴ���
d������ϵ��ͨ��H2��ƽ��������Ӧ�����ƶ���CO2ת����������ȷ��
e�����������ƽ�ⲻ�ƶ�������CO2ת���ʲ��䣬�ʴ���
�ʴ�Ϊ��bd��
��4����2C��ʯī��+O2��g��=2CO��g����H1=-222kJ/mol��
��H2��g��+$\frac{1}{2}$O2��g��=H2O ��g����H2=-242kJ/mol��
��CO2��g��+H2��g��?CO ��g��+H2O ��g����H=+41kJ/mol��
���ݸ�˹���ɣ��١�$\frac{1}{2}$+��-�۵�C��ʯī��+O2��g��=CO2��g����H=-222 kJ/mol��$\frac{1}{2}$-242 kJ/mol-41kJ/mol=-394 kJ/mol��
�ʴ�Ϊ��C��ʯī��+O2��g��=CO2��g����H=-394 kJ/mol��
���� ���⿼���˸�˹���ɵļ���Ӧ�ã���ѧƽ���Ӱ�����ط�������ƽ��״̬���жϵȣ���Ŀ�Ѷ��еȣ�


 �п������п��Ծ����ϵ�д�
�п������п��Ծ����ϵ�д� ��������״Ԫ��ϵ�д�
��������״Ԫ��ϵ�д� �ƸԿ�����ҵ��ϵ�д�
�ƸԿ�����ҵ��ϵ�д� ��Ԫ����ĩ��ϰ�ȷ��ϵ�д�
��Ԫ����ĩ��ϰ�ȷ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
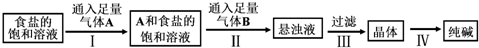
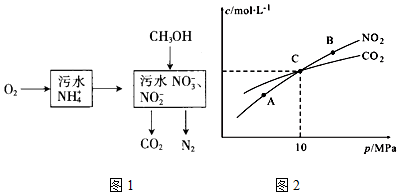
| A�� | ����A��NH3������B��CO2 | |
| B�� | �����Ƽ�Ĺ��չ�����Ӧ���������ܽ�ȵIJ��� | |
| C�� | ��III�������õ�����Ҫ�����������ձ���©���������� | |
| D�� | �ڢ�����������Ҫ�������ܽ⡢�������ᾧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 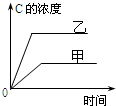 �о������¶ȶԷ�Ӧ��Ӱ�죬���ҵ��¶Ƚϸ� | |
| B�� | 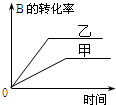 �о�����ѹǿ�Է�Ӧ��Ӱ�죬�Ҽ�ѹǿ�ϸ� | |
| C�� | 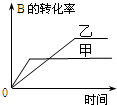 �о������¶ȶԷ�Ӧ��Ӱ�죬���ҵ��¶Ƚϸ� | |
| D�� | 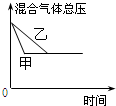 �о����Dz�ͬ�����Է�Ӧ��Ӱ�죬�Ҽ�ʹ�õĴ���Ч�ʽϸ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| t�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1molKClO4 | B�� | 0.1molKClO3 | C�� | 0.1molKClO2 | D�� | 0.2molKClO |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com