
【题目】化合物H为抗肿瘤药物吡柔比星的活性物质,其一种合成路线如下:
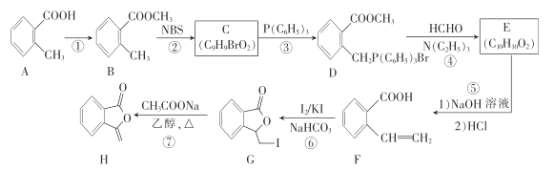
回答下列问题:
(1)A的化学名称是______________。
(2)反应①所需的试剂和条件是__________________。
(3)C的结构简式为_________________。
(4)写出E到F的反应方程式:___________________。
(5)⑦的反应类型是___________________________。
(6)芳香化合物X是H的一-种同分异构体,X中除苯环外不含其他环状结构,X能发生银镜反应、水解反应,写出X的结构简式:____________________________(只需写出3种)。
(7)设计以环已醇(![]() )为原料制备
)为原料制备![]() 的合成路线[无机试剂、P(C6H5)3及N(C2H5)3任用]。________________
的合成路线[无机试剂、P(C6H5)3及N(C2H5)3任用]。________________
【答案】2—甲基苯甲酸(或邻甲基苯甲酸) CH3OH/浓H2SO4、加热 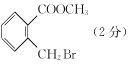
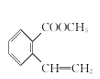 +NaOH
+NaOH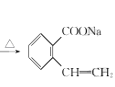 +CH3OH,
+CH3OH,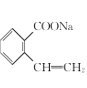 +HCl→
+HCl→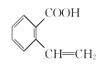 +NaCl 消去反应
+NaCl 消去反应 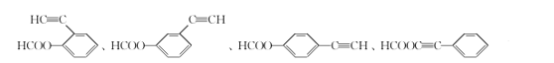

【解析】
A与甲醇发生酯化反应生成B,B和NBS发生反应生成C(![]() ),C与P(C6H5)3反应生成D,D与HCHO、N(C2H5)3反应生成E(
),C与P(C6H5)3反应生成D,D与HCHO、N(C2H5)3反应生成E(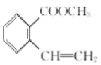 ),E先和NaOH水解,再酸化得到F,G到H发生消去反应。
),E先和NaOH水解,再酸化得到F,G到H发生消去反应。
(1)根据A的结构简式得到A的化学名称是2-甲基苯甲酸(或邻甲基苯甲酸);故答案为:2-甲基苯甲酸(或邻甲基苯甲酸)。
(2)反应①是发生酯化反应,所需的试剂和条件是CH3OH/浓硫酸、加热;故答案为:CH3OH/浓硫酸、加热。
(3)根据B到C反应和D的结构得到C的结构简式为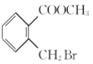 ;故答案为:
;故答案为: 。
。
(4) E和氢氧化钠发生水解反应,再和盐酸发生酸化反应得到F,其反应的方程式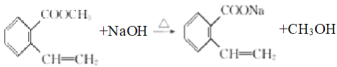 ,
,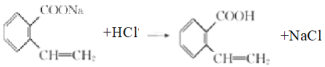 ;故答案为:
;故答案为: ,
, 。
。
(5)根据G和H的结构得到⑦的反应类型是消去反应;故答案为:消去反应。
(6)芳香化合物X是H的一种同分异构体,X中除苯环外不含其他环状结构,X能发生银镜反应,说明有醛基,能水解反应,说明有酯基,但只有两个氧原子,则说明是甲酸酯,因此X的结构简式: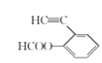 、
、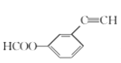 、
、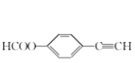 、
、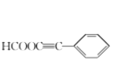 (只需写出3种);故答案为:
(只需写出3种);故答案为: 、
、 、
、 、
、 (只需写出3种)。
(只需写出3种)。
(7)![]() 催化氧化变为
催化氧化变为![]() ,
,![]() 和HBr反应生成
和HBr反应生成![]() ,与P(C6H5)3反应生成
,与P(C6H5)3反应生成![]() ,
,![]() 与
与![]() 在N(C2H5)3作用下反应生成
在N(C2H5)3作用下反应生成![]() ,因此合成路线为
,因此合成路线为 ;故答案为:
;故答案为: 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.氢氧化钡溶液与稀硫酸反应:Ba2++S![]() +H++OH-BaSO4↓+H2O
+H++OH-BaSO4↓+H2O
B.刻制印刷电路板的反应:Fe3++CuFe2++Cu2+
C.氯气与氢氧化钠溶液反应:Cl2+2OH-Cl-+ClO-+H2O
D.稀硫酸滴到铁片上:2Fe+6H+2Fe3++3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用氨气和氢气直接合成氨,并通过下列转化过程制备硝酸:
![]()
(1)上述物质中为红棕色气体的是____(填化学式);
(2)NH3溶于水所得溶液呈___(填“酸性”、 “碱性”或“中性” );
(3)配平NO2→HNO3的化学方程式:3NO2 +H2O = ___HNO3 + NO。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。请根据要求回答问题:
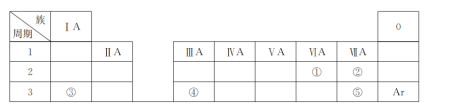
(1)①的元素符号是________;
(2)②和⑤的原子半径大小关系是②________⑤(填“>”“<”或“=”);
(3)③和⑤形成的化合物含有的化学键是__________(填“离子键”或“共价键”);
(4)③、④的最高价氧化物对应的水化物相互反应的离子方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成气用途非常广泛,可以煤、天然气等为原料生产。回答下列问题:
(1)用H2O(g)和O2重整CH4制合成气的热化学方程式如下:
(水蒸气重整)CH4(g)+ H2O(g)=CO(g)+3H2(g) H=+ 206 kJ●mol -1
(氧气重整)CH4(g)+0.5O2(g)=CO(g)+2H2(g) H=-36 kJ●mol-1
①2H2(g)+O2(g)=2H2O(g)的 H=_______kJ●mol-1。
②为了保持热平衡,同时用两种方式重整,不考虑热量损失,理论上得到的合成气中n(CO): n(H2)=1 :____(保留两位小数)。
③用水蒸气电催化重整甲烷的装置如图。装置工作时,O2-向_____(填“A"或“B’)极迁移;阳极发生的电极反应为___________。
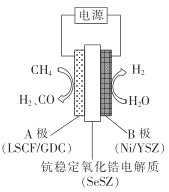
(2)焦炭与水蒸气在恒容密闭容器中反应制合成气的主要反应( I )、(II )的lgKp(Kp为以分压表示的平衡常数)与T的关系如下图所示。
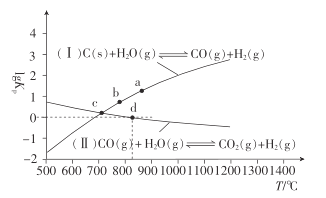
①反应(II)的H_____(填“大于”“等于”或“小于”)0。
②气体的总压强:a点_____ (填“大于”“等 于”或“小于”)b点,理由是_________。
③c点时,反应C(s) +CO2(g)![]() 2CO(g)的Kp=_____ (填数值)。
2CO(g)的Kp=_____ (填数值)。
④在恒容密闭容器中充入0. 5 mol CO、2 mol H2O(g)只发生反应(II),图中d点处达到平衡时,CO的转化率为_______;达到平衡时,向容器中再充入0.5 mol CO、2 mol H2O(g),重新达到平衡时,CO的平衡转化率_______(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁的氧化物可用于脱除煤气中的H2S,有一步反应为:Fe3O4(s)+3H2S(g)+H2(g)![]() 3 FeS(s)+4 H2O(g),其温度与平衡常数的关系如图所示。对此反应原理的理解正确的是
3 FeS(s)+4 H2O(g),其温度与平衡常数的关系如图所示。对此反应原理的理解正确的是
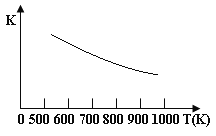
A.H2S是还原剂
B.脱除H2S的反应是放热反应
C.温度越高H2S的脱除率越大
D.压强越小H2S的脱除率越高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图所示,铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号)_______________。
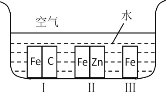
(2)氟氯代烷是一种能破坏臭氧层的物质。在大气平流层中,氟氯代烷受紫外线的照射分解出氯原子,氯原子参与下列有关反应:①Cl+O3→ClO+O2 ②O3→O+O2 ③ClO+O→Cl+O2。上列的反应的总反应式是_________,少量氟氯代烷能破坏大量臭氧的原因是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂离子电池的正极材料是含锂的钴酸锂(LiCoO2),充电时LiCoO2中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,用LiC6表示。电池反应为CoO2+LiC6![]() LiCoO2+C6,下列说法正确的是( )
LiCoO2+C6,下列说法正确的是( )
A.充电时,电池的负极反应为LiC6-e-=Li++C6
B.放电时,电池的正极反应为CoO2+Li++e-=LiCoO2
C.羧酸、醇等含活泼氢的有机物可用作锂离子电池的电解质
D.锂离子电池的比能量(单位质量释放的能量)低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液能大量共存的是
A.pH=1的溶液中:Fe2+、NO3-、SO42-、Na+
B.由水电离的c(H+)=1×10-14mol·L-1的溶液中:Ca2+、K+、Cl-、HCO3-
C.![]() =1012的溶液中:NH4+、Al3+、NO3-、Cl-
=1012的溶液中:NH4+、Al3+、NO3-、Cl-
D.c(Fe3+)=0.1 mol·L-1的溶液中:K+、ClO-、SO42-、SCN-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com