
【题目】一定量的KClO3中加入浓盐酸发生如下反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,其中氧化产物和还原产物的质量之比为
A. 1:6 B. 6:1 C. 5:1 D. 1:5
科目:高中化学 来源: 题型:
【题目】下列各组物质中,都是由极性键构成极性分子的一组是( )
A. NO2和CH4 B. NH3和H2O C. H2S和CCl4 D. HCl和C2H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】共价键、离子键、范德华力、氢键和金属键是构成物质粒子间的不同作用方式。下列物质中,只含有上述一种作用的是( )
A. 冰 B. 氢氧化钠 C. 铁 D. 石墨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.将适量的蔗糖放入烧杯中,加入少量水,搅拌均匀。然后加入适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。
(1)生成的黑色物质是_____(填化学式)。
(2)“体积膨胀,并放出有刺激性气味的气体”,写出对应的化学反应方程式:__________。
(3)上述实验表明,浓硫酸具有____(填序号)。
①酸性 ②吸水性 ③脱水性 ④强氧化性
Ⅱ.向80 mL浓硫酸中加入56 g铜片,并加热一段时间。当反应停止后,测得反应中共有13.44 L标准状况下的SO2生成,反应中转移的电子为_________ mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若已发现了116号元素则下列推断正确的是:①R是金属元素②R是非金属元素③其钠盐的化学式为Na2R④其最高价氧化物对应的水化物的酸性比硫酸强⑤最外电子层有6个电子
A. ①③④ B. ①③⑤ C. ②④⑤ D. ①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种钒-多卤化物电池结构示意图如图所示,电池和储液罐均存储有反应物和酸性电解质溶液。电池中发生的反应为2VCl2+BrCl2-![]() 2VCl3+Br-。
2VCl3+Br-。

下列说法正确的是
A. VCl2存储在正极储液罐内
B. 放电时H+从负极区移至正极区
C. 充电时电池的负极与电源的正极相连
D. 充电时阳极反应为Br-+2Cl--2e-=BrCl2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铁矿(主要成分为FeS2)的利用对资源和环境具有重要意义。
(1)工业上煅烧黄铁矿可制取SO2。已知下列热化学方程式
4FeS2(s)+11O2(g)=2Fe2O3(s)+8SO2(g) △H=akJ/mol
S(s)+O2(g)=SO2(g) △H=bkJ/mol
Fe(s)+2S(s)=FeS2(s) △H=ckJ/mol
则4Fe(s)+3O2(g)=2Fe2O3(s) △H=_____kJ/mol
(2)一种酸性条件下催化氧化黄铁矿的物质转化关系如图I所示。
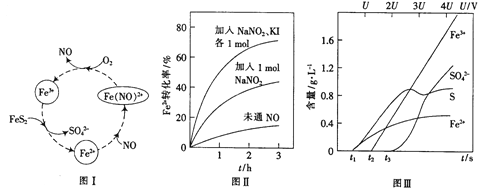
(1)写出如图中Fe3+与FeS2反应的离子方程式:______________。
(2)硝酸也可将FeS2氧化为Fe3+和SO42-,使用浓硝酸比使用稀硝酸反应速率慢,其原因是______________。
(3)控制Fe2+的浓度、溶液体积和通入O2的速率一定,图II所示为改变其他条件时Fe2+被氧化的转化率随时间的变化。
① 加入NaNO2发生反应:2H++3NO2-=NO3-+2NO+H2O。若1mol NaNO2完全反应则转移电子的数目为______mol。
② 加入NaNO2、KI发生反应:4H++2NO2-+2I-=2NO+I2+2H2O。解释图II中该条件下能进一步提高单位时间内Fe2+转化率的原因:______________。
(4)为研究FeS2作电极时的放电规律,以FeS2作阳极进行电解,由FeS2放电产生粒子的含量与时间、电压(U)的关系如图III所示。
①写出t1至t2间FeS2所发生的电极反应式:__________。
②当电压的值介于3U~4U之间,FeS2放电所得主要粒子为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H7N9型禽流感是全球首次发现的新亚型流感病毒,达菲(Tamiflu)是治疗该病毒的最佳药物.以莽草酸为原料,经多步反应可制得达菲和对羟基苯甲酸.达菲、莽草酸、对羟基苯甲酸的结构简式如下:

下列有关说法正确的是( )
A. 达菲、莽草酸、对羟基苯甲酸都属于芳香族化合物
B. 1mol莽草酸与NaOH溶液反应,最多消耗4mol NaOH
C. 对羟基苯甲酸较稳定,在空气中不易被氧化
D. 利用FeCl3溶液可区别莽草酸和对羟基苯甲酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com