
【题目】某无色溶液中含有H+、Al3+、Mg2+三种阳离子,逐滴加入0.1moLL﹣1NaOH溶液,消耗NaOH溶液体积(X轴)和生成沉淀(Y轴)之间的函数关系如图所示,则溶液中H+、Al3+、Mg2+三种阳离子的物质的量浓度之比为( ) 
A.1:1:1
B.2:2:1
C.2:1:1
D.1:1:2
【答案】B
【解析】解:假定NaOH溶液的浓度为cmol/L,则:
根据图象知,横坐标为0﹣10mL时发生的反应是:H++OH﹣=H2O,加入10mLNaOH溶液结合中和氢离子,n(H+)=n(NaOH)=0.01L×cmol/L=0.01cmol;
横坐标为50﹣60mL时,发生的化学反应是:Al(OH)3+OH﹣=AlO2﹣+2H2O,Al(OH)3完全溶解消耗消耗10mLNaOH溶液,由方程式可知n[Al(OH)3]=n(NaOH)=0.01L×cmol/L=0.01c,再根据铝元素守恒可知,n(Al3+)=n[Al(OH)3]=0.01cmol;
横坐标为10﹣50mL时发生的化学反应是:Mg2++2OH﹣=Mg(OH)2↓、Al3++3OH﹣=Al(OH)3↓,沉淀为最大值时,该阶段消耗40mLNaOH溶液,根据OH﹣守恒,2n[Mg(OH)2]+3n[Al(OH)3]=n(NaOH),故2n[Mg(OH)2]+0.03c=0.04L×cmol/L,故n[Mg(OH)2]=0.005cmol,
则溶液中H+、Al3+、Mg2+三种阳离子的物质的量浓度之比为0.01c:0.01c:0.005c=2:2:1,
故选B.


科目:高中化学 来源: 题型:
【题目】[选修2—化学与技术]
(1)Ⅰ、下列有关海水综合利用的说法正确的是( )
A.电解饱和食盐水可制得金属钠
B.海带提碘只涉及物理变化
C.海水提溴涉及到氧化还原反应
D.海水提镁涉及到复分解反应
(2)Ⅱ、铁在自然界分布广泛,在工业、农业和国防科技中有重要应用。
回答下列问题:
(1)用铁矿石(赤铁矿)冶炼生铁的高炉如图(a)所示。原料中除铁矿石和焦炭外含有 。除去铁矿石中脉石(主要成分为SiO2)的化学反应方程式为 ;高炉排出气体的主要成分有N2、CO2和 (填化学式)。
(2)已知:①Fe2O3(s)+3C(s)=2Fe(s)+3CO(g) △H=+494kJ/mol
②CO(g)+1/2O2(g)=CO2(g) △H=-283kJ/mol
③C(s)+1/2O2(g)=CO(g) △H=-110kJ/mol
则反应 Fe2O3(s)+3C(s)+3/2O2(g)=2Fe(s)+3CO2(g)的ΔH= kJ·mol-1。理论上反应 放出的热量足以供给反应 所需的热量(填上述方程式序号)
(3)有人设计出“二步熔融还原法”炼铁工艺,其流程如图(b)所示,其中,还原竖炉相当于高炉的 部分,主要反应的化学方程式为 ;熔融造气炉相当于高炉的 部分。
(4)铁矿石中常含有硫,使高炉气中混有 SO2污染空气,脱SO2的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知断裂1mol H2(g)中的H﹣H键需要吸收436.4KJ的能量,断裂1mol O2(g)中的共价键需要吸收498KJ的能量,生成H2O(g)中的1mol H﹣O键能放出462.8KJ的能量.下列说法正确的是( )
A.断裂1 mol H2O中的化学键需要吸收925.6 KJ的能量
B.2H2(g)+O2(g)═2H2O(g)△H=﹣480.4 KJ?mol﹣1
C.2H2O(l)═2H2(g)+O2(g)△H=471.6 KJ?mol﹣1
D.H2(g)+ ![]() O2(g)═H2O(l)△H=﹣240.2KJ?mol﹣1
O2(g)═H2O(l)△H=﹣240.2KJ?mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中铋元素的数据如图,下列说法正确的是( )
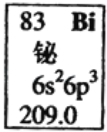
A. Bi元素的质量数是209
B. Bi元素的相对原子质量是209.0
C. Bi原子6p亚层有一个未成对电子
D. Bi原子最外层有5个能量相同的电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A.浓溶液一定是饱和溶液
B.析出晶体的溶液是饱和溶液
C.任何物质的饱和溶液,加热后都变成不饱和溶液
D.饱和溶液中,溶质的溶解速率大于结晶速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体的自动化检测中常常应用原电池原理的传感器.如图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号.下表列出了待测气体及敏感电极上部分反应产物.
待测气体 | 部分电极反应产物 |
NO2 | NO |
Cl2 | HCl |
CO | CO2 |
H2S | H2SO4 |
则下列说法中正确的是( )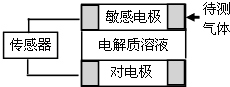
A.上述气体检测时,敏感电极均作电池正极
B.检测Cl2气体时,敏感电极的电极反应为:Cl2+2e﹣═2Cl﹣
C.检测H2S气体时,对电极充入空气,对电极上的电极反应式为O2+2H2O+4e﹣═4OH﹣
D.检测H2S和CO体积分数相同的两份空气样本时,传感器上产生的电流大小相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,元素W的一种单质是熔点高硬度大的宝石,Y的原子半径在所有短周期主族元素中最大。X和Z同主族,由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有刺激性气体产生。回答下列问题:
(1)Y元素位于周期表中的位置是_____________________。
(2)Z元素是______,由X和Z两种元素形成的化合物是______________。
(3)四种元素中的_______________元素是形成化合物最多的元素。
(4)某同学做同周期元素性质递变规律实验时,自己设计一套实验方案,并记录了有关实验现象如下表。

填写下列空格﹕
①实验目的:____________________________ 。
②与实验方案相对应的实验现象是:实验方案2对应的实验现象是___________(填上表中的符号A.......F);实验方案3对应的实验现象是__________________________。
③得出规律:同周期元素从左到右_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com