
【题目】将2 molX和2molY充入2L密闭容器中发生如下反应:X(气)+3Y(气)![]() 2Z(气)+aQ(气)2min达到平衡时生成0.8molZ,测得Q的浓度为0.4mol/L,下列叙述错误的是( )
2Z(气)+aQ(气)2min达到平衡时生成0.8molZ,测得Q的浓度为0.4mol/L,下列叙述错误的是( )
A.a的值为2
B.平衡时X的浓度为0.8mol/L
C.Y的转化率为60%
D.反应速率v(Y)=0.6mol/(L·min)
【答案】D
【解析】
试题分析:A.平衡时生成0.8mol Z,测得Q的浓度为0.4molL-1,则生成的n(Q)=0.4molL-1×2L=0.8mol,所以2:a=0.8mol:0.8mol,解得a=2,故A正确;B.平衡时生成0.8molZ,则参加反应的X的物质的量为0.8mol×=0.4mol,故平衡时X的物质的量为2mol-0.4mol=1.6mol,平衡时X的浓度为![]() =0.8mol/L,故B正确;C.平衡时生成0.8molZ,则参加反应的Y的物质的量为0.8mol×=1.2mol,故Y的转化率为
=0.8mol/L,故B正确;C.平衡时生成0.8molZ,则参加反应的Y的物质的量为0.8mol×=1.2mol,故Y的转化率为![]() ×100%=60%,故C正确;D.平衡时生成0.8molZ,则参加反应的Y的物质的量为0.8mol×=1.2mol,所以v(Y)=
×100%=60%,故C正确;D.平衡时生成0.8molZ,则参加反应的Y的物质的量为0.8mol×=1.2mol,所以v(Y)=![]() =
=![]() =0.3mol/(Lmin),故D错误,故选D。
=0.3mol/(Lmin),故D错误,故选D。


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】等体积的硫酸铝、硫酸锌、硫酸钠溶液分别与足量氯化钡溶液反应,若生成硫酸钡沉淀的质量比为1∶2∶3,则三种硫酸盐的物质的量浓度之比为( )
A. 1∶2∶3 B. 1∶6∶9 C. 1∶3∶3 D. 1∶3∶6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B两种烃,其相关信息如下:
A ①完全燃烧的产物中n(CO2):n(H2O)=2:1
②28<M (A)<60
③不能使溴的四氯化碳溶液褪色④一氯代物只有一种结构
B ①饱和链烃,通常情况下呈气态②有同分异构体
③二溴代物有三种
回答下列问题:
(1)烃A的实验式是 ;
(2)烃A的结构简式是 ;
(3)烃B的三种二溴代物的结构简式为 、 、 ;
(4)烃C为烃B的同系物,常温下为气态且只有一种一溴代物,则烃C的一溴代物的结构简式为 (填一种即可).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.76 g铜镁合金完全溶解于50 mL、密度为1. 40 g cm-3、质量分数为63%的浓硝酸中,得到NO2气体1 792 mL(标准状况),向反应后的溶液中加入适量的1.0 mol L-1的NaOH 溶液,恰使溶液中的金属离子全部沉淀。下列说法不正确的是
A. 该浓硝酸中的HNO3的物质的量浓度是14.0 mol L-1
B. 加入NaOH溶液的体积是50 mL
C. 浓硝酸在与合金的反应中起了酸性和氧化性的双重作用,且起氧化性的硝酸的物质的量为0.08 mol
D. 得到的金属氢氧化物的沉淀为3.12 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知W、Y、Z、T均为短周期元素,且原子半径依次增大。请填空:
(1)W、Z是形成化合物种类最多的两种元素,写出Z原子的核外电子排布图____;
(2)化合物YW3的水溶液能使酚酞变红,用方程式表示酚酞变红的原因_________;
(3)元素T的原子中电子共占据了7个轨道,则T在元素周期表____周期____族。T的化合物TY熔融时不导电,常用作砂轮及耐高温材料,由此推知,它属于_____.
a离子晶体 b.原子晶体 c.分子晶体 d.无法判断断
(4)YW3属于______(填“极性”、“非极性”)分子其中Y的化合价为______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是自然赐给人类的宝藏,海水的综合利用是全世界研究的重点。完成下列问题:
(1)粗盐中除了含有泥沙之外还含有Ca2+、Mg2+、SO42-等杂质,粗盐获得精盐一般步骤如下:

加入的试剂①、②分别是:_________、_________。
(2)某学生在实验室中模拟海水提取溴的步骤为:
取25 L除去悬浮杂质后的海水,浓缩至2L,向其中通入足量氯气。
① 氧化步骤中生成Br2的离子方程式为_______________________________。
② 将吹出的Br2(g)用纯碱溶液全部吸收,发生反应:3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2↑ ,产生的CO2通入足量澄清石灰水中,得到1g白色沉淀。计算海水中溴的浓度为_______g/L。
③实验室中若用CCl4提取少量的溴:向溴水中加入CCl4振荡、静置……得溴的四氯化碳溶液,该分离提纯溴的方法叫________;用到的主要仪器为_____________。
(3)实验证明金属制品在海水中更容易生锈,铜锈的化学式为: _____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是()
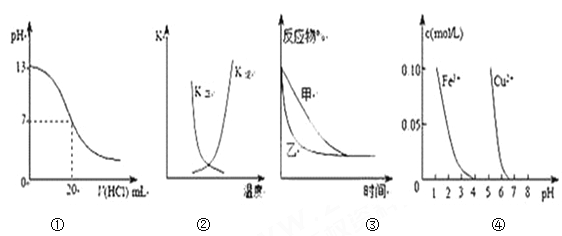
A. 图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1NaOH溶液,溶液的pH随加入酸体积的变化
B. 图②中曲线表示反应2A(g) + B(g)![]() 2C(g) ΔH > 0,正、逆反应的平衡常数K随温度的变化
2C(g) ΔH > 0,正、逆反应的平衡常数K随温度的变化
C. 图③表示压强对可逆反应2A(g)+2B(g) ![]() 3C(g)+D(s)的影响,乙压强比甲压强大
3C(g)+D(s)的影响,乙压强比甲压强大
D. 据图④若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在4左右。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g) ![]() Z(g)+W(s);△H>0下列叙述正确的是( )
Z(g)+W(s);△H>0下列叙述正确的是( )
A. 加入少量W,逆反应速率增大 B. 当容器中气体密度不变时,反应达到平衡
C. 升高温度,平衡逆向移动 D. 平衡后加入X,上述反应的△H增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com